




2022版高考化学选考山东专用一轮总复习课件:专题十化学能与热能 —应用篇
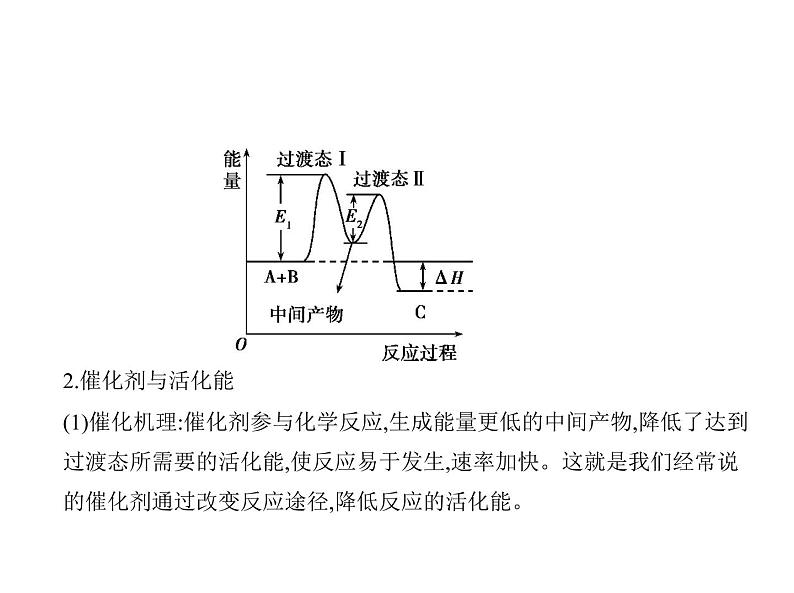
展开通过化学反应机理揭示化学反应变化的实质1.过渡态理论及活化能(1)过渡态理论认为,反应物分子并不只是通过简单碰撞直接形成产物,而 是必须经过一个形成活化络合物的过渡状态,并且达到这个过渡状态需 要一定的活化能。(2)大多数化学反应往往要经过多个反应步骤才能实现,其中的每一步反 应都称为基元反应,每一个基元反应都经历一个过渡态。下图是达到过 渡态所需要的活化能(如图E1、E2):
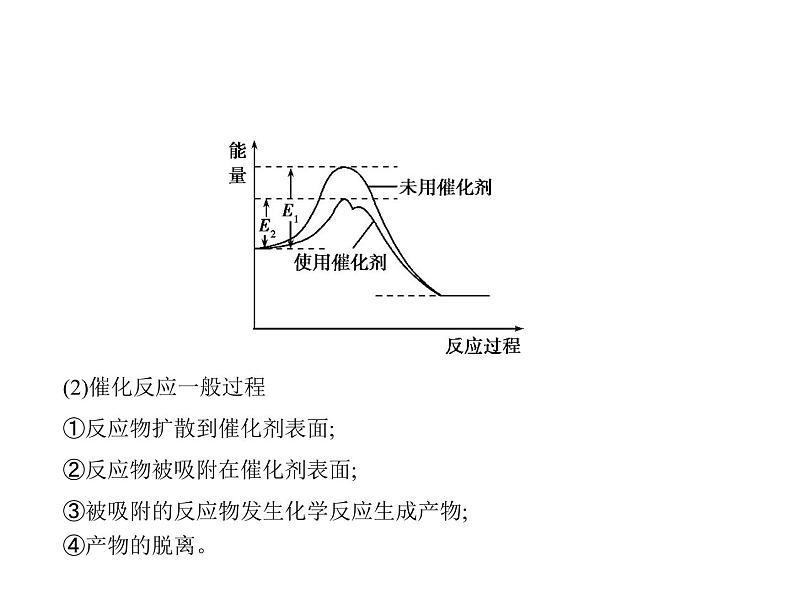
2.催化剂与活化能(1)催化机理:催化剂参与化学反应,生成能量更低的中间产物,降低了达到 过渡态所需要的活化能,使反应易于发生,速率加快。这就是我们经常说 的催化剂通过改变反应途径,降低反应的活化能。
(2)催化反应一般过程①反应物扩散到催化剂表面;②反应物被吸附在催化剂表面;③被吸附的反应物发生化学反应生成产物;
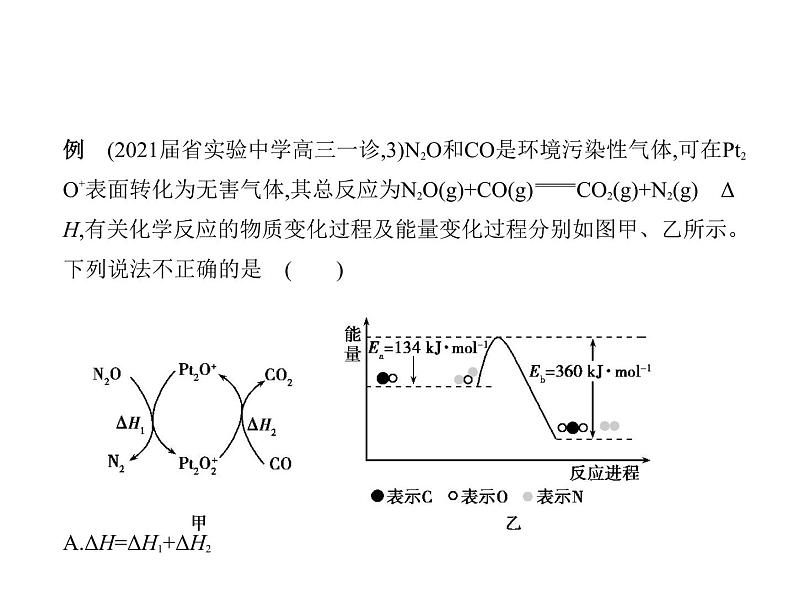
例 (2021届省实验中学高三一诊,3)N2O和CO是环境污染性气体,可在Pt2 O+表面转化为无害气体,其总反应为N2O(g)+CO(g) CO2(g)+N2(g) ΔH,有关化学反应的物质变化过程及能量变化过程分别如图甲、乙所示。 下列说法不正确的是 ( ) A.ΔH=ΔH1+ΔH2
B.ΔH=-226 kJ·ml-1C.由图乙知该反应正反应的活化能小于逆反应的活化能D.为了实现转化,需不断向反应器中补充Pt2O+和Pt2
解析 总反应方程式为N2O(g)+CO(g) CO2(g)+N2(g) ΔH,由①N2O(g)+Pt2O+(s) Pt2 (s)+N2(g) ΔH1和②Pt2 (s)+CO(g) Pt2O+(g)+CO2(s) ΔH2,可知①+②等于总反应方程式,则ΔH=ΔH1+ΔH2,A正确;ΔH=正反 应活化能Ea-逆反应活化能Eb=134 kJ·ml-1-360 kJ·ml-1=-226 kJ·ml-1,B正 确;由图乙可知,正反应活化能Ea小于逆反应活化能Eb,C正确;反应过程中 Pt2O+和Pt2 参与反应后又生成,不需要补充,D错误。
题目价值 本题是以环境污染性气体N2O和CO在Pt2O+表面转化为无害 气体为背景,分析物质发生的化学变化的反应机理及伴随的能量变化,考 查了盖斯定律的应用,体现了宏观辨识与微观探析、证据推理与模型认 知的学科核心素养。
物质转化历程与能量图像基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应。 大多数的化学反应不能一步完成,在微观上是分几步完成的,每一步反应 都是一个基元反应。基元反应过渡状态理论,有比简单碰撞理论更加鲜明的物理图像,理论的 重要部分是反应系统的势能面,刻画了反应所引起的能量变化,指出了反 应经历的可能途径。该理论认为,基元反应在从反应物到产物的变化过 程中要经历一个中间状态,这个状态称为过渡态。X+YZ [X…Y…Z] XY+Z反应物 过渡态 产物过渡态是处在反应过程中具有最高能量的一种分子构型,过渡态能量与
反应物的平均能量的差值相当于活化能。反应的历程与能量图像可以 表示为: 物质转化历程与能量图像常见类型有以下三种:
例1 (2015北京理综,9,6分)最新报道:科学家首次用X射线激光技术观察 到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下: 下列说法正确的是 ( )A.CO和O生成CO2是吸热反应B.在该过程中,CO断键形成C和OC.CO和O生成了具有极性共价键的CO2D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
命题分析 本题将微观、抽象的化学变化具体化为可视的示意图,需要 考生整合题干和图像信息,回答相关问题。
解析 A项,CO和O生成CO2是放热反应;B项,观察反应过程的示意图知, 该过程中,CO中的化学键没有断裂形成C和O;C项,图中CO和O生成的CO2 分子中含有极性共价键;D项,状态Ⅰ→状态Ⅲ表示CO与O反应的过程。
例2 已知:2H2O(l) 2H2(g)+O2(g) ΔH=+571.0 kJ/ml。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下: 过程Ⅰ:2Fe3O4(s) 6FeO(s)+O2(g) ΔH=+313.2 kJ/ml过程Ⅱ:……下列说法不正确的是 ( )
A.过程Ⅰ中每消耗232 g Fe3O4转移2 ml电子B.过程Ⅱ热化学方程式为3FeO(s)+H2O(l) H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mlC.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能D.铁氧化合物循环分解水制H2具有成本低、产物易分离等优点
命题分析 本题涉及氧化还原反应、盖斯定律的应用、能量的转化等 知识点,考查信息转化、应用及计算能力,体现证据推理与模型认知的学 科核心素养。
解析 A项,过程Ⅰ中每消耗232 g Fe3O4生成0.5 ml O2,转移2 ml电子;B 项,根据盖斯定律,由(总反应×1/2-过程Ⅰ×1/2)得过程Ⅱ热化学方程式:3 FeO(s)+H2O(l) H2(g)+Fe3O4(s) ΔH=+128.9 kJ/ml;C项,过程Ⅰ和过程Ⅱ都是吸热反应,不存在化学能→热能;D项,铁氧化合物循环分解水制 H2具有成本低的优点,氢气和氧气分步生成,具有产物易分离的优点。
例3 (2018海南单科,12,4分)炭黑是雾霾中的重要颗粒物,研究发现它可 以活化氧分子,生成活化氧。活化过程的能量变化模拟计算结果如图所 示。活化氧可以快速氧化二氧化硫。下列说法正确的是 ( )
A.每活化一个氧分子吸收0.29 eV的能量B.水可使氧分子活化反应的活化能降低0.42 eVC.氧分子的活化是O—O的断裂与C—O键的生成过程D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
命题分析 本题创设学术探索情境,考查催化剂参与的反应历程和能量 图像分析等知识,体现了证据推理与模型认知的核心素养,突出了基础 性、创新性的考查要求。反应历程中的基元反应的能量变化,“爬坡” 即为能垒。最大能垒步骤属于“慢反应”,决定整个反应速率。研究工 作的方向是寻找合适的催化剂,降低最大能垒步骤的能垒,提高反应速率, 提高生产效率。
2022版高考化学选考山东专用一轮总复习课件:专题四氧化还原反应 —应用篇: 这是一份2022版高考化学选考山东专用一轮总复习课件:专题四氧化还原反应 —应用篇,共11页。PPT课件主要包含了实践探究,答案D,答案C等内容,欢迎下载使用。
2022版高考化学选考山东专用一轮总复习课件:专题十一化学能与电能的转化 —应用篇: 这是一份2022版高考化学选考山东专用一轮总复习课件:专题十一化学能与电能的转化 —应用篇,共17页。
2022版高考化学选考山东专用一轮总复习课件:专题十四盐类水解和沉淀溶解平衡 —应用篇: 这是一份2022版高考化学选考山东专用一轮总复习课件:专题十四盐类水解和沉淀溶解平衡 —应用篇,共26页。












