




初中化学鲁教版 (五四制)九年级全册到实验室去:探究酸和碱的化学性质背景图ppt课件
展开【实验目的】 1.加深对酸和碱的主要性质的认识 2.通过实验解释生活中的一些现象
【实验用品】 试管、药匙、蒸发皿、玻璃棒。 稀盐酸、白醋、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末石蕊溶液、酚酞溶液、生锈的铁钉
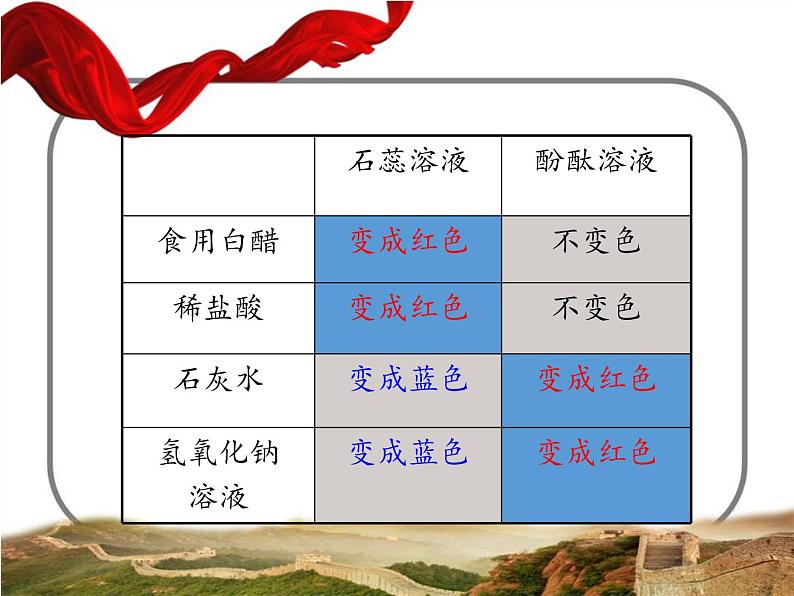
【实验步骤】 1.参考下图进行实验,比较酸和碱与指示剂的作用。
滴定板和试管一个道理优点:节约药品
实验二:取一根生锈的铁钉,大头朝下放入试管中,然后加入稀盐酸,使生锈的铁钉部分浸没在稀盐酸里,观察现象。当铁钉表面变得光亮后,铁钉表面开始出现什么现象?
想一想 将铁钉放入试管时应如何操作?
①锈钉表面的铁锈逐渐消失变得光亮,溶液变成黄色;②当铁钉变得光亮后,可观察到铁钉表面出现气泡。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
3.在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。然后再向试管中加入稀盐酸观察现象。(一、二组做)
4.在一烧杯里倒入少量氢氧化钠的稀溶液,滴几滴酚酞溶液,观察现象。然后边用滴管慢慢滴入稀盐酸,边不断震荡烧杯,至溶液颜色恰好变为无色为止。取一滴溶液在玻璃片上置于酒精灯火焰上烘烤,观察现象。(三、四组做)
5.取一小勺氢氧化钙放入一烧杯中,再将水注入盛有氢氧化钙的烧杯中,并用玻璃棒搅拌,观察现象。将石灰水置于两支试管中,分别滴入紫色石蕊溶液和无色酚酞溶液,观察现象。将适量(用药匙的柄把一端挑一点)的氢氧化钙粉末加入一只洁净的试管中,再用胶头滴管吸取稀盐酸加入这只试管中,震荡,观察现象。 (五、六组做)
①出现蓝色絮状沉淀,溶液变成无色②蓝色絮状沉淀溶解,溶液呈蓝绿色
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
Cu(OH)2+2HCl=CuCl2+2 H2O
②玻璃片出现白色固体。
氢氧化钠能使无色酚酞变红
HCl+NaOH=NaCl+H2O
②紫色石蕊溶液显示蓝色,无色酚酞 溶液显示红色。
③氢氧化钙粉末逐渐溶解形成无色溶液。
氢氧化钙不易溶于水,即微溶于水
氢氧化钙能使紫色石蕊变蓝,无色酚酞变红
Ca(OH)2+2HCl==CaCl2+2H2O
①酸溶液能跟酸碱指示剂起反应
②酸能跟多种活泼金属起反应,通常生成盐和氢气
③酸能跟金属氧化物反应生成盐和水:
⑤酸能跟某些盐反应生成新酸和新盐
④酸跟碱起中和反应生成盐和水:
①碱溶液能与酸碱指示剂反应
②碱能与酸发生反应,生成盐和水
③碱溶液能与盐反应,生成新碱和新盐
④碱溶液能与非金属氧化物反应,生成盐和水
化学鲁教版 (五四制)到实验室去:探究酸和碱的化学性质习题课件ppt: 这是一份化学鲁教版 (五四制)到实验室去:探究酸和碱的化学性质习题课件ppt
鲁教版 (五四制)九年级全册第二单元 常见的酸和碱到实验室去:探究酸和碱的化学性质教学演示课件ppt: 这是一份鲁教版 (五四制)九年级全册第二单元 常见的酸和碱到实验室去:探究酸和碱的化学性质教学演示课件ppt,共6页。
初中化学到实验室去:探究酸和碱的化学性质备课ppt课件: 这是一份初中化学到实验室去:探究酸和碱的化学性质备课ppt课件,共11页。PPT课件主要包含了科学探究的一般步骤,反思与评价,反应后物质成分的探究,CONCEPTON,解题思路,解题时注意的问题等内容,欢迎下载使用。













