




科粤版九年级下册7.3 溶液浓稀的表示教课内容课件ppt
展开药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木。
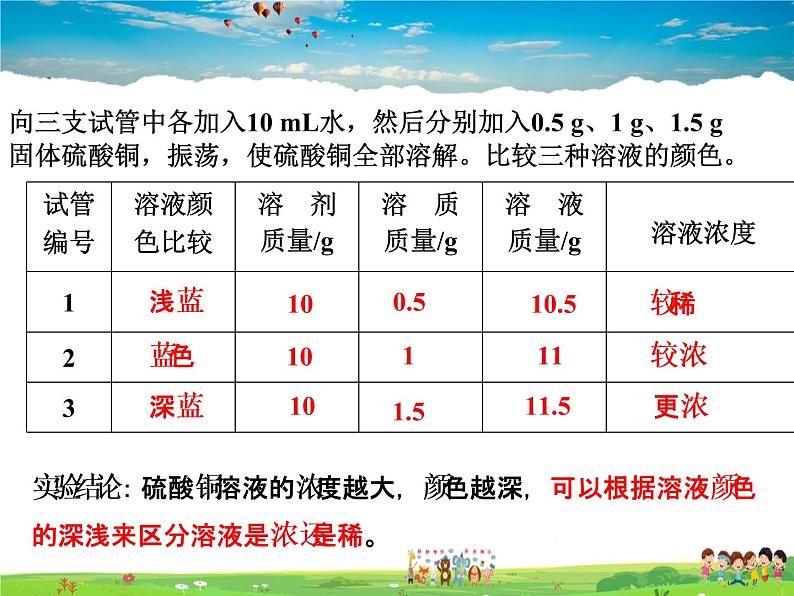
浅蓝 蓝色 深蓝
向三支试管中各加入10 mL水,然后分别加入0.5 g、1 g、1.5 g固体硫酸铜,振荡,使硫酸铜全部溶解。比较三种溶液的颜色。
实验结论:硫酸铜溶液的浓度越大,颜色越深,可以根据溶液颜色的深浅来区分溶液是浓还是稀。
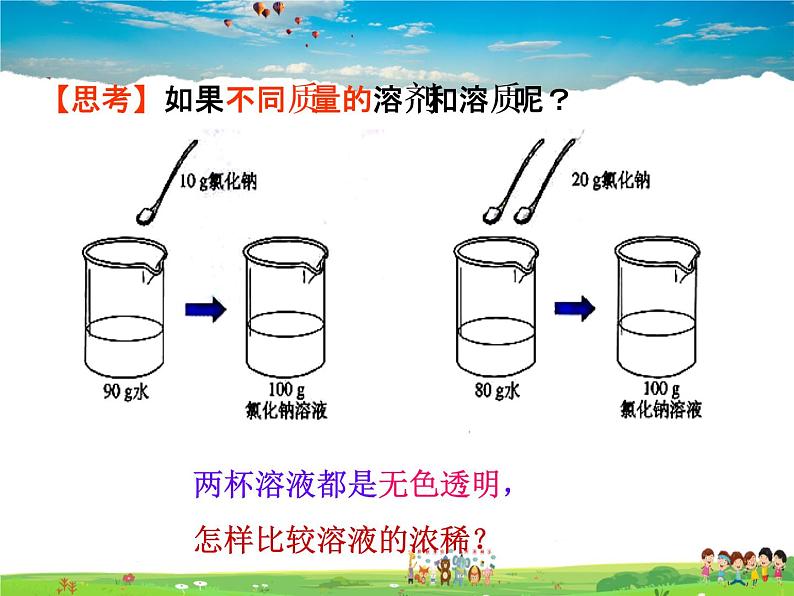
两杯溶液都是无色透明,怎样比较溶液的浓稀?
【思考】如果不同质量的溶剂和溶质呢?
有色溶液的颜色深浅,可粗略反映溶液的浓稀。要准确表示,就要用溶液的浓度来表示。
2.溶质的量分数:溶质质量与溶液质量之比。(通常以百分数表示)
注意:①溶质的质量:形成溶液的那部分溶质,没溶入溶液的不计。②溶液的质量 = 溶质的质量 + 溶剂的质量。 (必须分清溶质、溶剂与溶液)。 ③计算时上下质量单位要统一。④不要忘记乘以100%,最后得到百分数。
1.溶液的浓度:一定量的溶液中所含溶质的量叫溶液的浓度。
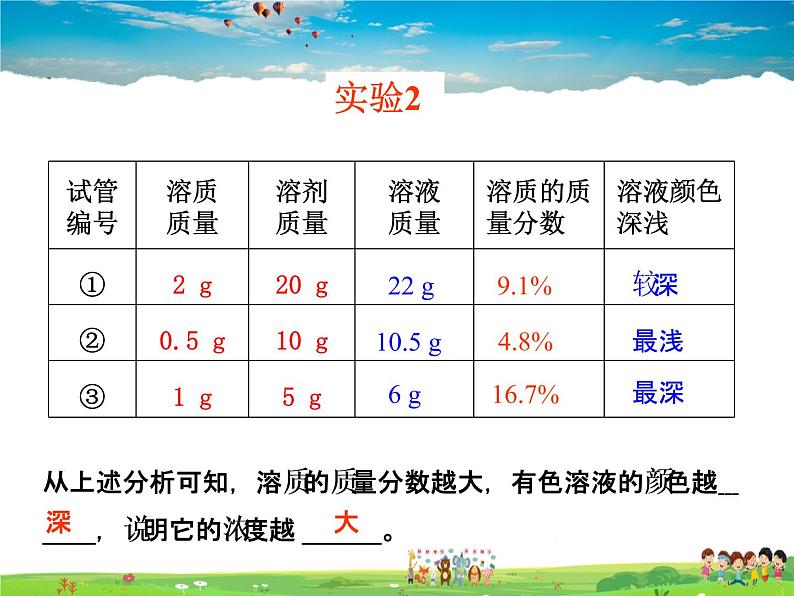
从上述分析可知,溶质的质量分数越大,有色溶液的颜色越 ____,说明它的浓度越 ______。
[题型一] 有关溶质、溶剂和溶液之间的换算
二、溶质质量分数的简单计算
溶液质量 = 溶质质量 + 溶剂质量
例题1:在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg这种溶液,需要氯化钠和水的质量各是多少?
答: 配制150 kg质量分数为16%的氯化钠溶液 需24 kg氯化钠和126 kg水。
向20%的某浓溶液中加水后,溶液、溶质和溶剂的质量如何变化?如何解决有关溶液稀释的计算?
[题型二] 有关溶液稀释或浓缩的计算
稀释前溶质质量 = 稀释后溶质质量
浓缩前溶质质量 = 浓缩后溶质质量
例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50 g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水?
【解】设稀释后溶液的质量为 x。
50 g 98% = x 20%
答:需要水的质量为195 g。
需要水的质量= 245 g– 50 g = 195 g。
注意点:溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。
例题3:100 g 9.8%硫酸跟多少克锌反应?同时生成多少克氢气?
【解】 100 g 9.8%硫酸中含纯硫酸的质量为:
100 g9.8%=9.8 g
设参加反应的锌质量为x,生成氢气的质量为y。
Zn + H2SO4 ==ZnSO4 + H2
65 98 2
x 9.8 g y
x =6.5 g, y =0.2 g。
[题型三]有关化学方程式的计算
[讨论] 20℃时,氯化钠溶解度为36克,
(1)若将36克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少? (2)若将38克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
从上面讨论中你得到什么启示?说明什么问题?
饱和溶液的溶质质量分数=
溶质的质量分数36% 是指:溶质t℃时溶解度36 g是指:
溶质质量分数与溶解度的比较
100 g溶液中含有36 g溶质。
在t℃ 时,100 g水最多溶解该溶质36 g。
表示溶液中溶质质量的多少
科粤版九年级下册7.3 溶液浓稀的表示教课内容ppt课件: 这是一份科粤版九年级下册<a href="/hx/tb_c12503_t3/?tag_id=26" target="_blank">7.3 溶液浓稀的表示教课内容ppt课件</a>,共16页。PPT课件主要包含了学习目标,新知学习,操作步骤,溶液中质量分数偏大,量取液体时俯视读数,称量的溶质偏大,溶液中质量分数偏小,物体中有杂质,配制溶液的烧杯中有水,量取液体时仰视读数等内容,欢迎下载使用。
初中化学科粤版九年级下册7.3 溶液浓稀的表示课文内容课件ppt: 这是一份初中化学科粤版九年级下册<a href="/hx/tb_c12503_t3/?tag_id=26" target="_blank">7.3 溶液浓稀的表示课文内容课件ppt</a>,共17页。PPT课件主要包含了溶液是浓还是稀,学习目标,新知学习,溶液的溶度,颜色越深浓度越大,溶质的质量分数,2计算公式,比较深,在一定的温度下,不受外界条件的影响等内容,欢迎下载使用。
科粤版7.3 溶液浓稀的表示说课ppt课件: 这是一份科粤版7.3 溶液浓稀的表示说课ppt课件,文件包含73溶液的浓稀表示第1课时课件pptx、73溶液的浓稀表示第1课时练习docx、73溶液的浓稀表示第1课时教案doc、73溶液的浓稀表示第1课时学案doc等4份课件配套教学资源,其中PPT共28页, 欢迎下载使用。













