





化学必修 第一册第三节 物质的量教课内容课件ppt
展开宏观 物质
4 g 32 g 36g
2个 1个 2个
4g氢气与32g氧气反应生成32g水中含有多少个水分子?
【联系生活】——数纽扣
思考与交流:现有一大包纽扣,如何可以快速估测这包纽扣的数目?
纽扣的总质量÷10枚纽扣的质量=n个这样的“集合体”n个这样的“集合体”×10=总的纽扣数
方案:先称取10枚纽扣(为一个集合体)的质量,再称取纽扣的总质量。
假如让10亿人来数一滴水里的水分子,每人每分钟数100个,日夜不停,需要 多年才能数清。
微观粒子不便以个数来计量!
1670000000000000000000
0.05ml水中有多少个水分子? (水的密度为1g/ml,一个水分子的质量约是3.00×10-23g)
表示一定数目粒子的集合体。
摩尔,简称摩,符号为ml。
(1)1 摩尔氧(2)1 摩尔 H(3)2 摩尔大米(4)硫酸的物质量为3 ml(5)0.5 ml CO2
1、4ml H2O 含有_____ml H,______ml O;2、4ml Na2SO3中含有_______ml Na+ ;
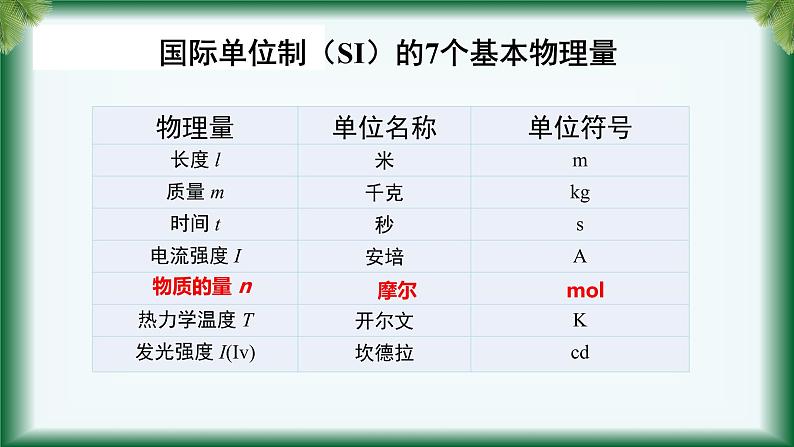
国际单位制(SI)的7个基本物理量
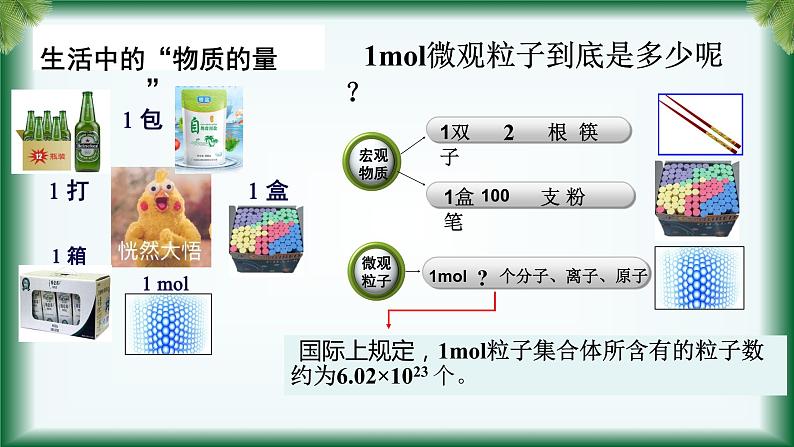
1双 根 筷子
1盒 支 粉笔
1ml微观粒子到底是多少呢?
国际上规定,1ml粒子集合体所含有的粒子数约为6.02×1023 个。
1 ml任何粒子的粒子数叫做阿伏加德罗常数。
NA≈6.02×1023ml-1
国际上规定1 ml粒子集合体所含的粒子数约为6.02×1023 ,
例如:1 ml CO2所含的分子数为6.02×1023
判断:1 ml CO2和H2的混合气体所含的分子数约为6.02×1023
正确,1 ml任何粒子集合体所含的粒子数约为6.02×1023,这里的粒子集合体可以是纯净物,也可以是混合物。
如果把6.02×1023个直径为2.5cm的硬币排成一行,可以来回于地球与太阳之间240.8亿次。
如果有 6.02×1023 粒米让全球60亿人吃,每人每天吃10斤,可吃1万4千年。
0.5 ml H2O含有水分子数约为_____________
例题:1ml H2O含有水分子数约为6.02×1023
2 ml H2O含有水分子数约为_____________
物质的量(n)、粒子数(N)与阿伏伽德罗常数(NA)的关系。
(1)摩尔是国际单位制中七个基本物理量之一。(2)摩尔是物质的质量单位。(3)物质的量是一个基本物理量,表示含有一定数目微粒的集合体。(4)1ml任何物质含有分子数约为6.02×1023个。
1、判断下列说法是否正确。
2、下列说法正确的是_______________________①1ml大米 ②1ml氢 ③1mlH ④1mlH2 ⑤1ml氢元素
(摩尔是物质的量的单位)
(物质可以由分子、离子或原子构成)
1ml 6.02×1023 ml-1 2ml 6.02×1023 ml-1 3ml 6.02×1023 ml-1
12.04×1023
18.06×1023
物质的量( n )、阿伏加德罗常数( NA )、微粒数目( N )的关系式 :
(1)0.5ml CO2中,含有______ml C;含有_________mlO;含有二氧化碳分子数约为________________;碳原子数为_____________;氧原子数为________________。(2)1ml Na2CO3中约含有_____ml Na+、______ml CO32-离子,共含有离子的个数为_________ 。(3)0.1ml NH4+中有 ml电子,有 ml质子。
3.01×1023
6.02×1023
1.806×1024
注意:区分整体与部分的关系
微粒 C H O H2SO4
12 1 16 98
1ml 物质的质量(g)在数值上等于其相对原子(分子)质量
l ml任何粒子或物质的质量以克为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等。
单位物质的量的物质所具有的质量
g/ml 或 kg/ml
摩尔质量 = 相对原子(分子)质量=1 ml 物质的质量
钠的相对原子质量为:钠的摩尔质量为: 1 ml 钠的质量为:
23 g/ml 0.023 kg/ml
23 g 0.023 kg
当摩尔质量、1 ml 物质的质量分别以g/ml、g为单位时,三者数值相等 。三者含义、单位不相同。
(1)Na的摩尔质量是__________, (2)KCl的摩尔质量是__________,(3)CH4的摩尔质量是___________,0.5mlCH4的质量是_________。(4)CO32-的摩尔质量是__________,2mlCO32-的质量是_______。
物质的量(n)、质量(m)、摩尔质量(M)之间有什么关系呢?
物质的量(n)、质量(m)、摩尔质量(M)之间的关系:
【例题1】26.5g Na2CO3的物质的量是多少?
【解】Na2CO3的相对分子质量为106,摩尔质量为106g/ml。
答:26.5gNa2CO3的物质的量是0.25ml。
物质的量是联系宏观世界与微观粒子的桥梁!
拓展应用:物质的量在化学反应方程式中应用:化学计量数(系数): 2 1 2 粒子数(个): 同时乘以NA(个) : 物质的量(n): 质量(m):
2个 1个 2个
2NA 1NA 2NA
2ml 1ml 2 ml
4g 32g 36g
结论:化学反应方程式中,各物质系数之比等于微粒个数比也等于物质的量之比
表示含有一定数目粒子的集合体,符号为n,单位为摩尔(ml),简称摩
1ml任何粒子的粒子数,符号为NA,单位是ml-1
1ml物质所具有的质量,符号为M,单位为g/ml(g·ml-1)
练习1、1.204×1024个CH4的质量是多少?
【分析】物质的量是联系宏观质量和微观粒子的桥梁,已知粒子数,求质量,应先求物质的量。
(1)质量相同的O2和O3,其物质的量之比为_________,其分子数之比为_________,原子数之比为__________。(2)0.5mlCO和N2的混合气体中含有原子数为_______,含有质子数为_______。
(3)在3Cl2 + 6KOH = KClO3 + 5KCl + 3H2O的反应中,氧化剂和还原剂物质的量之比为________。如果有3mlCl2参加反应,则反应中转移电子数为________。
3Cl2 + 6KOH = KClO3 + 5KCl + 3H2O
0 +5 -1
化合价升高,失去1×5e-,被氧化
化合价降低,得到5×e-,被还原
化学必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教案配套ppt课件: 这是一份化学必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教案配套ppt课件,共24页。PPT课件主要包含了物质的量浓度,容量瓶简介等内容,欢迎下载使用。
化学必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量背景图课件ppt: 这是一份化学必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量背景图课件ppt,共19页。PPT课件主要包含了课前回顾,物质的量,相互转化,课本P52,体积相同,体积不同,个乒乓球,决定物质体积的因素,个篮球,紧密堆积等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量完整版ppt课件: 这是一份人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量完整版ppt课件,文件包含23课时1物质的量的单位摩尔课件新教材人教版2019高中化学必修第一册ppt、23课时1物质的量的单位摩尔练习新教材人教版2019高中化学必修第一册docx等2份课件配套教学资源,其中PPT共26页, 欢迎下载使用。













