
高中化学人教版 (2019)必修 第一册第三节 化学键课时作业
展开
这是一份高中化学人教版 (2019)必修 第一册第三节 化学键课时作业,共5页。试卷主要包含了单选题,综合题等内容,欢迎下载使用。
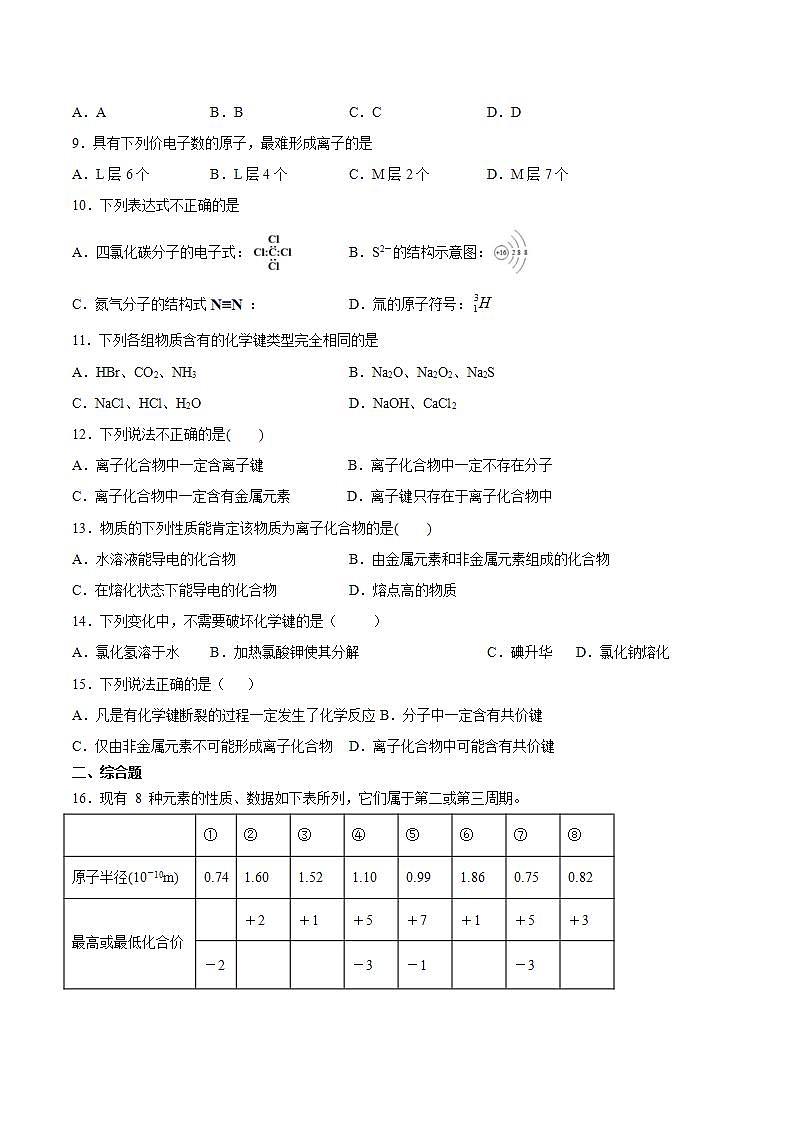
高一上学期化学人教版(2019)必修第一册第四章物质结构元素周期律第三节化学键检测卷一、单选题1.下列各组物质只含有离子键的是A.CaCl2 B.CO2 C.HCl D.NaOH2.下列分子中各原子都满足8电子稳定结构的化合物是( )A.C6H6 B.HCN C.CO2 D.N23.下列各组中的每种物质内既有离子键又有共价键的一组是( )A.NaOH、K2SO4、H2SO4 B.HCl、Al2O3、MgCl2C.Na2O2、NH4Cl、Na2SO4 D.MgO、Na2SO4、NH4HCO34.下列分子中所有原子都满足最外层8电子稳定结构的是( )A.BeCl2 B.CH4 C.BF3 D.PCl35.关于离子键、共价键的各种叙述中,下列说法中正确的是A.在离子化合物里,只存在离子键,没有共价键B.非极性键只存在于双原子的单质分子(如 Cl2)中C.原子序数为 11 与 9 的元素能够形成离子化合物,该化合物中存在离子键D.任何物质中都存在化学键6.下列选项中既含有离子晶体又含有原子晶体的是( )A.NaCl、SiO2 B.NH4Cl、CO2 C.HCl、H2O D.金刚石、SiO27.下列物质中是共价化合物的是( )A. B. C. D.8.下列对一些实验事实和理论解释正确的是选项实验事实理论解释AHCl气体溶于水,能导电HCl为离子化合物BHBr的酸性强于HCl的酸性Br的非金属性比Cl强C在熔融状态下能够导电中含有离子键DHF的沸点高于HClF的非金属性比Cl强A.A B.B C.C D.D9.具有下列价电子数的原子,最难形成离子的是A.L层6个 B.L层4个 C.M层2个 D.M层7个10.下列表达式不正确的是A.四氯化碳分子的电子式: B.S2-的结构示意图:C.氮气分子的结构式: D.氚的原子符号:11.下列各组物质含有的化学键类型完全相同的是A.HBr、CO2、NH3 B.Na2O、Na2O2、Na2SC.NaCl、HCl、H2O D.NaOH、CaCl212.下列说法不正确的是( )A.离子化合物中一定含离子键 B.离子化合物中一定不存在分子C.离子化合物中一定含有金属元素 D.离子键只存在于离子化合物中13.物质的下列性质能肯定该物质为离子化合物的是( )A.水溶液能导电的化合物 B.由金属元素和非金属元素组成的化合物C.在熔化状态下能导电的化合物 D.熔点高的物质14.下列变化中,不需要破坏化学键的是( )A.氯化氢溶于水 B.加热氯酸钾使其分解 C.碘升华 D.氯化钠熔化15.下列说法正确的是( )A.凡是有化学键断裂的过程一定发生了化学反应 B.分子中一定含有共价键C.仅由非金属元素不可能形成离子化合物 D.离子化合物中可能含有共价键二、综合题16.现有 8 种元素的性质、数据如下表所列,它们属于第二或第三周期。 ①②③④⑤⑥⑦⑧原子半径(10-10m)0.741.601.521.100.991.860.750.82最高或最低化合价 +2+1+5+7+1+5+3-2 -3-1 -3 回答下列问题:(1)④的元素名称是_____,⑧的元素符号是_____。②在元素周期表中的位置是(周期、族)_____ 。(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_____;名称是________; 碱性最强的化合物的电子式是:_________; 属_____化合物(填“离子”或“共价”)。(3)①的最简单氢化物的电子式为_____, ⑦的最简单氢化物的电子式为_____,结构式为_____。(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:_________________ 。(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:____________。17.五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是常用的食品调味剂。回答下列问题:(1)写出元素D在周期表中的位置____________________________________________。(2)五种元素中,原子半径最大的是________(填元素符号),非金属最强的是________(填元素符号)。(3)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是________(用化学式表示)。(4)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________,其中存在的化学键类型为_______________和________________。(5)单质E与水反应的离子方程式为____________________________________________18.A、B、C、D四种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。(1)B元素的名称___;B在周期表中的位置第___周期,第___族;(2)A、B形成的化合物的电子式___;(3)C的最高价氧化物的化学式___;(4)D2C的电子式:___。
参考答案1.A2.C3.C4.D5.C6.A7.B8.C9.B10.A11.A12.C13.C14.C15.D16.磷 B 第三周期IIA族 HClO4 高氯酸 离子 NH3+HNO3=NH4NO3 Mg(OH)2+2H+=Mg2++2H2O 17.第三周期 第ⅤA族 Na Cl PH3 NH4Cl 离子键 共价键 Cl2+H2O⇌H++Cl-+HClO 18.氮 二 ⅤA SO3
相关试卷
这是一份高中化学第三节 化学键课后练习题,共9页。试卷主要包含了下列叙述中正确的是,下列叙述不正确的是,下列物质中,含有离子键的是,下列关于化学键的说法,正确的是,下列化学用语描述正确的是等内容,欢迎下载使用。
这是一份第四章 物质结构与元素周期律 第三节化学键训练题-2021年高一上学期(29019人教版必修一),共13页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第三节 化学键课时训练,共4页。试卷主要包含了单选题,综合题等内容,欢迎下载使用。











