


第34讲 烃的含氧衍生物(讲)-2022年高考化学一轮复习讲练测
展开第十一章 有机化学基础
第34讲 烃的含氧衍生物(精讲)
【考情分析】
本讲内容在高考中常以选择题的形式对醇、醛、酸、酯(尤其是酚酯类)等物质的组成、化学性质进行考查,以非选择题常考查烃的衍生物结构、化学性质、同分异构体的分析等知识,且此类题目的信息多以框图的方式呈现出来,要求回答的内容有分子式、结构简式、化学名称、化学方程式的书写、有机反应类型的判断、有机合成路线的设计等。
【核心素养分析】
1.宏观辨识与微观探析:从不同角度认识醇、酚、醛、羧酸、酯的主要性质和应用。从组成、结构上探析烃的含氧生物的性质形成“结构决定性质”的观念。
2.证据推理与模型认知:领悟有机物的行变关系烯→醇→醛→酸→酯”转化模型,了解转化的原理。
【网络构建】
【知识梳理】
一、醇和酚
1.醇、酚的概念
(1)醇是羟基与链烃基或苯环侧链上的碳原子相连的化合物,饱和一元醇的分子通式为CnH2n+1OH(n≥1)。
(2)酚是羟基与苯环直接相连而形成的化合物,最简单的酚为苯酚或。
(3)醇的分类
(4)几种常见的醇
名称 | 甲醇 | 乙二醇 | 丙三醇 |
俗称 | 木精、木醇 |
| 甘油 |
结构简式 | CH3OH | ||
状态 | 液体 | 液体 | 液体 |
溶解性 | 与水和乙醇互溶 | ||
2.醇类、苯酚的物理性质
1)醇类物理性质的变化规律
(1)溶解性
低级脂肪醇易溶于水。
(2)密度
一元脂肪醇的密度一般小于1 g·cm-3。
(3)沸点
①直链饱和一元醇的沸点随着分子中碳原子数的递增而逐渐升高。
②醇分子间存在氢键,所以相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
【易错警示】醇羟基是亲水基,多羟基化合物如丙三醇等都易溶于水或与水以任意比例互溶。碳原子数多的一元醇水溶性差。
2)苯酚的物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,易被空气氧化呈粉红色。
(2)苯酚常温下在水中的溶解度不大,当温度高于65℃时,能与水混溶,苯酚易溶于酒精。
(3)苯酚有毒,对皮肤有强烈的腐蚀作用,如果不慎沾到皮肤上应立即用酒精洗涤。
3.醇、酚的命名
1)醇的命名
①选择含有与-OH相连的碳原子的最长碳链为主链,根据碳原子数目称某醇;
②从距离-OH最近的一端给主链碳原子依次编号;
③醇的名称前面要用阿拉伯数字标出羟基的位置;羟基的个数用“二”“三”等表示。
2)酚的命名
①去除酚羟基,留下苯环或苯的同系物,先命名上述名称,例如,甲(基)苯,乙(基)苯。
②加上酚羟基,看在苯环的什么位置,共有邻、间、对三个位置,例如甲苯,在除甲基外的正六边形上依次分别标上12345,共5个位置,其中15,24位置相同,则1位为邻位,2位为间位,3位为对位,那么酚羟基在哪个位置上,就叫X甲苯酚。以此类推。
【易错警示】(1)从物质分类看,石炭酸不属于羧酸。
(2)酚羟基的氢原子比醇羟基的氢原子易电离,是因为苯环对羟基产生影响。
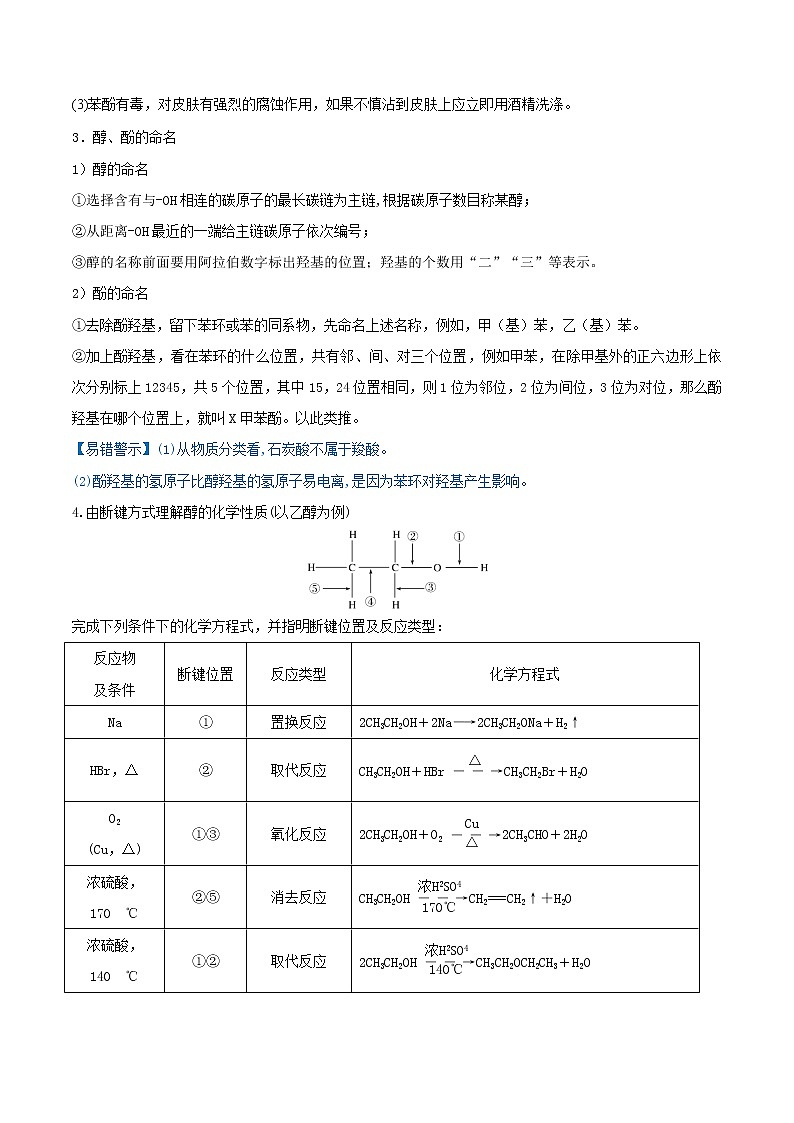
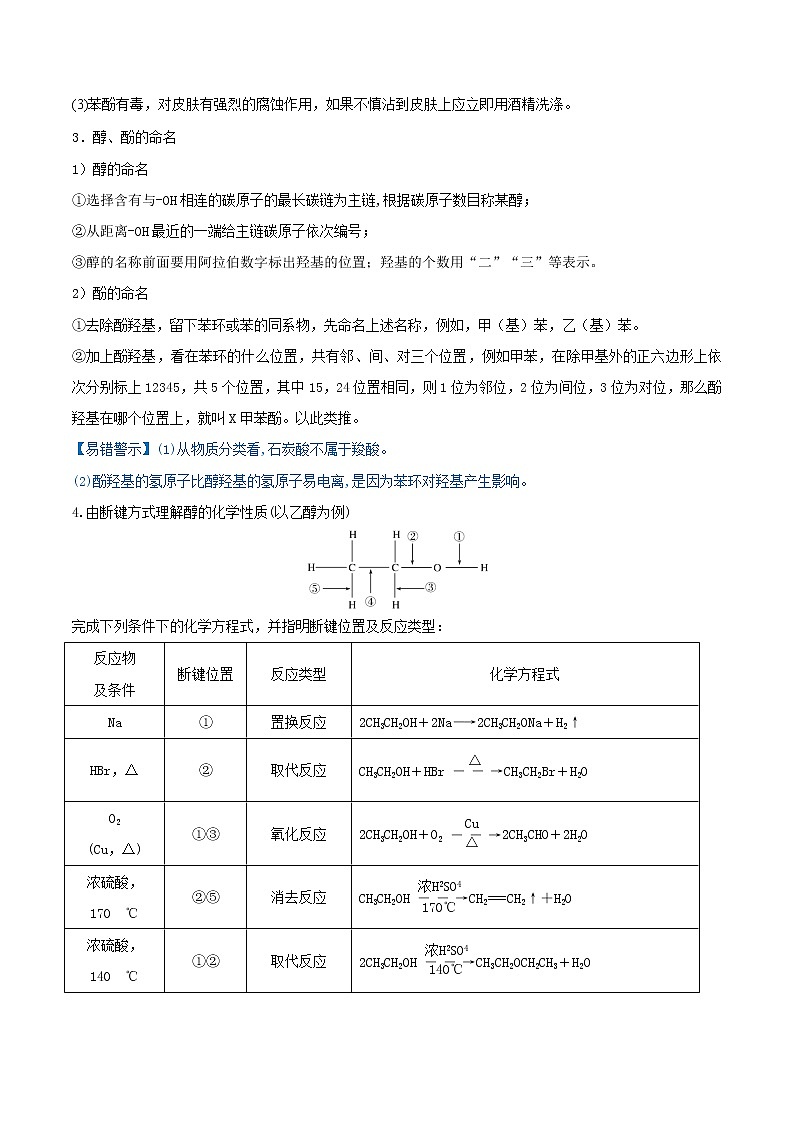
4.由断键方式理解醇的化学性质(以乙醇为例)
完成下列条件下的化学方程式,并指明断键位置及反应类型:
反应物 及条件 | 断键位置 | 反应类型 | 化学方程式 |
Na | ① | 置换反应 | 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ |
HBr,△ | ② | 取代反应 | CH3CH2OH+HBrCH3CH2Br+H2O |
O2 (Cu,△) | ①③ | 氧化反应 | 2CH3CH2OH+O22CH3CHO+2H2O |
浓硫酸, 170 ℃ | ②⑤ | 消去反应 | CH3CH2OHCH2===CH2↑+H2O |
浓硫酸, 140 ℃ | ①② | 取代反应 | 2CH3CH2OHCH3CH2OCH2CH3+H2O |
CH3COOH (浓硫酸) | ① | 酯化反应 | CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O |
5.由基团之间的相互影响理解酚的化学性质
(1)苯环对羟基的影响——弱酸性
由于苯环对羟基的影响,使酚羟基比醇羟基更活泼,可以发生电离。
①苯酚的电离方程式为C6H5OHC6H5O-+H+。苯酚俗称石炭酸,但酸性很弱,不能使石蕊溶液变红。
②与碱的反应:苯酚的浑浊液现象为液体变澄清现象为溶液又变浑浊。
该过程中发生反应的化学方程式分别为
。
。
③与活泼金属反应:
(2)羟基对苯环的影响——苯环上邻对位氢原子的取代反应
由于羟基对苯环的影响,使苯酚中苯环上的氢比苯分子中的氢活泼。苯酚稀溶液中滴入过量的浓溴水中产生现象为:产生白色沉淀。其化学方程式为:
。
【易错警示】①在苯酚与溴水的取代反应实验中,苯酚取少量,滴入的溴水要过量。这是因为生成的三溴苯酚易溶于苯酚等有机溶剂,使沉淀溶解,不利于观察实验现象。②苯酚分子中羟基邻对位的H原子易被取代,是因为羟基对苯环产生影响。
(3)显色反应:苯酚溶液中滴如FeCl3溶液,溶液变为紫色。
(4)氧化反应:苯酚易被空气中的氧气氧化而显粉红色,易被酸性KMnO4溶液氧化,易燃烧。
(5)缩聚反应:苯酚与甲醛在催化剂作用下,可发生缩聚反应,化学方程式是:
+(n-1)H2O。
【特别提醒】苯酚是重要的医用消毒剂和化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。酚类化合物均有毒,是重点控制的水污染物之一。
6.苯酚的用途和对环境的影响
苯酚是重要的医用消毒剂和化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。酚类化合物均有毒,是重点控制的水污染物之一。
7.醇和酚的性质比较
类别 | 脂肪醇 | 芳香醇 | 酚 |
实例 | CH3CH2OH | C6H5CH2CH2OH | C6H5OH |
官能团 | —OH | —OH | —OH |
结构特点 | —OH与链烃基相连 | —OH与芳香烃侧链上的碳原子相连 | —OH与苯环直接相连 |
主要化学性质 | (1)与钠反应;(2)取代反应;(3)脱水反应; (4)氧化反应;(5)酯化反应 | (1)弱酸性 (2)取代反应 (3)显色反应 | |
特性 | 将红热的铜丝插入醇中有刺激性气味产生(生成醛或酮) | 遇FeCl3溶液显紫色 | |
智能点二、醛、羧酸、酯
1.醛
(1)概念:由烃基或氢原子与醛基相连而构成的化合物,可表示为RCHO。甲醛是最简单的醛。饱和一元醛分子的通式为CnH2nO(n≥1)。
(2)甲醛、乙醛的物理性质
物质 | 颜色 | 气味 | 状态 | 密度 | 水溶性 |
甲醛 | 无色 | 刺激性气味 | 气体 |
| 易溶于水 |
乙醛 | 无色 | 刺激性气味 | 液体 | 比水小 | 与水互溶 |
(3)醛的化学性质
醛类物质既有氧化性又有还原性,其氧化、还原关系为
醇醛羧酸
以乙醛为例写出醛类反应的主要化学方程式:
Ⅰ.氧化反应
①银镜反应
CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O;
②与新制Cu(OH)2悬浊液的反应
CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O。
Ⅱ.还原反应(催化加氢)
CH3CHO+H2CH3CH2OH。
(4)特殊的醛——甲醛
①结构特点与化学性质
甲醛的分子式为CH2O,其分子可以看成含两个醛基,如图所示。
银镜反应的化学方程式为:HCHO+4Ag(NH3)2OH(NH4)2CO3+4Ag↓+6NH3+2H2O。
与新制Cu(OH)2悬浊液反应的化学方程式为:HCHO+4Cu(OH)2+2NaOHNa2CO3+2Cu2O↓+6H2O。
②用途及危害
用途:水溶液可用于浸制生物标本,用来生产酚醛树脂。
危害:引起人中毒。
(5)醛的应用和对环境、健康产生的影响
①醛是重要的化工原料,广泛应用于合成纤维、医药、染料等行业。
②35%~ 40%的甲醛水溶液俗称福尔马林;具有杀菌(用于种子杀菌)和防腐性
能(用于浸制生物标本)。
③劣质的装饰材料中挥发出的甲醛是室内主要污染物之一。
④甲醛与苯酚发生缩聚反应生成酚醛树脂。
【易错警示】①醛基只能写成—CHO或,不能写成—COH;②醛与新制的Cu(OH)2悬浊液反应时碱必须过量且应加热煮沸;③醛类使酸性KMnO4溶液或溴水褪色,二者均为氧化反应。
2.羧酸
(1)概念:由烃基或氢原子与羧基相连构成的有机化合物。官能团为—COOH。饱和一元羧酸分子的通式为CnH2nO2(n≥1)。
(2)羧酸的分类
(3)几种重要的羧酸
物质及名称 | 结构 | 类别 | 性质特点或用途 |
甲酸 (蚁酸) | 饱和一元 脂肪酸 | 酸性,还原性 (醛基) | |
乙二酸 (草酸) | 二元羧酸 | 酸性,还原性 (+3价碳) | |
苯甲酸 (安息香酸) | 芳香酸 | 防腐剂 | |
高级 脂肪酸 | RCOOH(R为碳原子数较多的烃基) | 饱和高级脂肪酸,常温呈固态; 油酸:C17H33COOH不饱和高级脂肪酸,常温呈液态 | |
(4)羧酸的代表物——乙酸
①分子组成和结构
分子式 | 结构式 | 结构简式 | 官能团 |
C2H4O2 | CH3COOH | —COOH |
②物理性质
俗名 | 颜色 | 状态 | 溶解性 | 气味 |
醋酸 | 无色 | 通常为液体,温度低于16.6 ℃时凝结成类似冰一样的晶体 | 易溶于水 | 刺激性 |
③化学性质
乙酸的性质取决于羧基,反应时的主要断键位置如图:
a.酸性
乙酸是一种常见的有机酸,具有酸的通性,其酸性强于碳酸,但仍属于弱酸,电离方程式为CH3COOHCH3COO-+H+。
乙酸表现酸性的主要现象及化学方程式如下:
b.酯化反应
醇和酸(羧酸或无机含氧酸)作用生成酯和水的反应叫酯化反应。如CH3COOH和CH3CHOH发生酯化反应的化学方程式为CH3COOH+CH3CHOHCH3CO18OCH2CH3+H2O。
④用途
乙酸是食醋的有效成分(普通食醋中含有质量分数为3%~5%的乙酸),在食品工业中乙酸常用作酸度调节剂。另外,乙酸稀溶液常用作除垢剂,用来除去容器内壁的碳酸钙等污垢。
(5)几种重要的羧酸
1)特殊的酸——甲酸
①分子组成和结构
分子式 | 结构简式 | 官能团 | 俗称 |
CH2O2 | HCOOH | —COOH | 蚁酸 |
②化学性质
甲酸结构式为,甲酸分子中既含有羧基,又含有醛基,因而甲酸既能表现出羧酸的性质,又能表现出醛的性质。如能发生酯化反应,又能发生银镜反应及与新制Cu(OH)2悬浊液反应。
银镜反应:HCOOH+2Ag(NH3)2OH(NH4)2CO3+2Ag↓+2NH3+H2O。
与新制Cu(OH)2悬浊液反应:HCOOH+2Cu(OH)2+2NaOHNa2CO3+Cu2O↓+4H2O。
与CH3OH发生酯化反应:HCOOH+CH3OHH2O+HCOOCH3。
2)乙二酸:俗名草酸(HOOC—COOH),草酸在浓硫酸的作用下脱水可制得CO,反应方
程式为CO↑+CO2↑+H2O。
3)苯甲酸:俗名安息香酸(),酸性比较(电离出H+的难易程度):草酸>甲酸>苯甲
酸>乙酸>碳酸>苯酚。
4)高级脂肪酸:
3.酯
(1)概念:羧酸分子羧基中的—OH被—OR′取代后的产物。可简写为RCOOR′,官能团为(酯基)。
(2)酯的物理性质
(3)酯的化学性质
以为例,写出酯发生反应的化学方程式:
①酸性水解
。
②碱性水解
。
无机酸只起催化作用,碱除起催化作用外,还能中和水解生成的酸,使水解程度增大。
【易错警示】对酯的水解反应的理解:酯的水解反应为取代反应;在酸性条件下为可逆反应;在碱性条件下,能中和产生的羧酸,酯的水解平衡右移,水解程度增大。
(4)酯在生产、生活中的应用
①日常生活中的饮料、糖果和糕点等常使用酯类香料。
②酯还是重要的化工原料。
4.酯化反应的五种常见类型总结
(1)一元羧酸与一元醇之间的酯化反应,如CH3COOH+HOC2H5CH3COOC2H5+H2O
(2)一元羧酸与多元醇之间的酯化反应,如2CH3COOH++2H2O
(3)多元羧酸与一元醇之间的酯化反应,如+2CH3CH2OH+2H2O
(4)多元羧酸与多元醇之间的酯化反应:此时反应有三种情形,可得普通酯、环酯和高聚酯。如
(5)既含羟基又含羧基的有机物自身的酯化反应:此时反应有三种情形,可得到普通酯、环酯和高聚酯。如
【典例剖析】
高频考点1、考查醇、酚的结构特点及性质
例1.1.下列关于醇与酚的比较中正确的是
A.醇和酚都能与氢氧化钠溶液反应
B.醇和酚都能与钠发生反应
C.醇、酚的水溶液都能使石蕊试纸变红
D.醇和酚都能与碳酸钠溶液反应
【解析】A项,醇没有酸性,醇不能与NaOH溶液反应,酚有弱酸性能与NaOH溶液反应,错误;B项,醇和酚中都有羟基,都能与Na反应放出H2,正确;C项,醇没有酸性,醇的水溶液不能使石蕊试纸变红,酚虽然有酸性,但由于酸性很弱,酚的水溶液也不能使石蕊试纸变红,错误;D项,醇与Na2CO3不反应,酚能与Na2CO3溶液反应,但不会放出CO2,错误;答案选B。
【答案】B
【名师点睛】(1)醇和酚中都有羟基,都能与Na反应放出H2;(2)醇没有酸性,酚中由于苯环对酚羟基的影响使酚羟基能微弱电离呈弱酸性,但酸性比H2CO3弱,酚的溶液几乎不能使石蕊试液变红,酚能与NaOH、Na2CO3反应(酚与Na2CO3反应不会放出CO2,生成NaHCO3),酚与NaHCO3不反应。
【变式训练】下列关于醇和酚的说法中,正确的是
A.含有羟基的化合物一定是醇
B.分子内有苯环和羟基的化合物一定是酚
C.羟基跟链烃基相连时,有机物为醇
D.酚和醇具有相同的官能团,因而具有相同的化学性质
【解析】A、含有羟基的化合物可能为醇、酚类或酸,故A错误;B、由于苯环直接连接羟基的属于酚类,所以分子内有苯环和羟基的化合物不一定是酚,如苯甲醇,故B错误;C、表示醇类的官能团是跟链烃基相连的羟基,故C正确;D、由于烃基结构不同,性质不同,如由于苯环的影响,酚羟基性质比醇羟基活泼,苯酚具有弱酸性,故D错误;故选C。
【答案】C
高频考点2、考查醇类氧化反应和消去反应规律
例2.下列醇既能发生消去反应,又能被氧化为醛的是( )
A.CH3OH B.
C. D.
【解析】A. CH3OH没有β-C所以不能发生消去反应;B. 的催化氧化产物是丙酮;C. ,β-C上没有H原子,不能发生消去反应;D. ,β-C上有H原子,能发生消去反应生成烯烃,α-C 上有2个H原子,能被氧化为醛。综上所述,既能发生消去反应,又能被氧化为醛的是D,故选D。
【答案】D
【规律总结】(1)醇的消去反应规律:醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,并且此相邻的碳原子上必须连有氢原子时,才可发生消去反应,生成不饱和键。表示为,如CH3OH、不能发生消去反应。
(2)醇的催化氧化反应规律:醇的催化氧化的反应情况与跟羟基(—OH)相连的碳原子上的氢原子的个数有关。
【变式训练】下列物质既能发生消去反应,又能氧化成酮的是
A.CH3CH2CH2OH B.(CH3)3CCH2OH
C. D.
【解析】A.CH3CH2CH2OH羟基所连碳的相邻碳上连有H,能发生消去反应生成烯烃,羟基相连的碳原子上有氢,能发生氧化反应生成醛,A项错误;B.(CH3)3CCH2OH中羟基相连的碳原子上无H,不能发生消去反应生成烯烃,羟基相连的碳原子上有氢,能发生氧化反应生成醛,B项错误;C.中羟基相连的碳原子上连有H,能发生消去反应生成烯烃,羟基相连的碳原子上无氢能发生氧化反应生成酮,C项正确;D.中羟基相连的碳原子上无H,不能发生消去反应生成烯烃,羟基相连的碳原子上有氢,能发生氧化反应生成醛,D项错误;答案选C。
【答案】C
高频考点3、考查醛、羧酸、酯的结构特点的理解
例3.由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH反应的有( )
①﹣OH ②﹣CH3 ③﹣COOH ④ ⑤﹣CHO.
A.2种 B.3种 C.4种 D.5种
【解析】将①~⑤两两进行组合,形成的化合物总共有10种,其中-OH与-COOH组合形成H2CO3不属于有机物;9种有机物中,能够与氢氧化钠反应的有机物有5种,分别为:C6H5OH、C6H5COOH、HCOOH、CH3COOH和OHCCOOH,答案选D。
【答案】D
【反思归纳】醛基官能团能被弱氧化剂氧化而碳碳双键不能被弱氧化剂氧化,只能被强氧化剂氧化,所以可以用银氨溶液或新制Cu(OH)2悬浊液检验醛基。而在—CHO与C==C都存在时,要检验C==C双键的存在,必须先用弱氧化剂将—CHO氧化后,再用强氧化剂检验C==C的存在。
【变式训练】某有机物的结构简式如图所示,下列说法正确的是
A.该有机物的分子式为
B.1mol有机物最多能与发生反应
C.1mol有机物最多能与1molNa发生反应
D.1mol有机物最多能与2molNaOH发生反应
【解析】A.该有机物的分子式为,故A错误;B.苯环和碳碳双键都能和氢气发生加成反应,则1mol有机物最多能与发生反应,故B正确;C.1个该有机物分子中含有1个羟基和1个羧基,则1mol该有机物最多能与2molNa发生反应,故C错误;D.1个该有机物分子中含有1个酯基和1个羧基,水解生成的酚也能和氢氧化钠反应,则1mol该有机物最多能与3molNaOH发生反应,故D错误;答案选B。
【答案】B
高频考点4、考查多官能团有机物的性质
例4.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
下列有关叙述不正确的是
A.贝诺酯分子中有2 种含氧官能团
B.可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚
C.1mol 乙酰水杨酸最多消耗3molNaOH
D.贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
【解析】A.贝诺酯分子中含-COOC-、-CONH-两种官能团,A正确;B.对乙酰氨基酚含酚-OH,可与氯化铁发生显色反应,则可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚,B正确;C.乙酰水杨酸含-COOH和酚羟基形成的酯基,lmol乙酰水杨酸最多消耗3molNaOH,C正确;D.贝诺酯与足量NaOH溶液共热,-COOC-、-CONH-均发生水解,不会生成乙酰水杨酸钠和对乙酰氨基酚,D错误;答案选D。
【答案】D
【方法归纳】确定多官能团有机物性质的三步骤
注意:有些官能团性质会交叉。例如,碳碳三键与醛基都能被溴水、酸性高锰酸钾溶液氧化,也能与氢气发生加成反应等。
【变式训练】(2020·山东学业水平等级考试,6)从中草药中提取的calebin A(结构简式如图)可用于治疗阿尔茨海默症。下列关于calebin A的说法错误的是( )
A.可与FeCl3溶液发生显色反应
B.其酸性水解的产物均可与Na2CO3溶液反应
C.苯环上氢原子发生氯代时,一氯代物有6种
D.1 mol该分子最多与8 mol H2发生加成反应
【解析】calebin A分子中含有酚羟基,能与FeCl3溶液发生显色反应,A项正确;calebin A的酸性水解产物(含羧基和酚羟基)和(含酚羟基)均可与Na2CO3溶液反应,B项正确;calebin A分子中含2个苯环,由于该分子不具有对称性,其苯环上的一氯代物共有6种,故C项正确;calebin A分子中苯环、碳碳双键、羰基均能与H2发生加成反应,即1 mol calebin A分子最多能与9 mol H2发生加成反应,D项错误。
【答案】D
高频考点5、考查烃的衍生物的转化及应用
例5.如图是几种常见有机物的转化关系,下列说法正确的是( )
A.反应①是加成反应,反应⑧是消去反应,其他所标明的反应都是取代反应
B.上述物质中能与NaOH溶液反应的只有乙酸
C.1,2二溴乙烷、乙烯、乙醇烃基上的氢原子被氯原子取代,其一氯取代产物都是一种
D.等物质的量的乙烯和乙醇与足量氧气反应时耗氧量相同
【解析】A项,反应①是乙烯与溴的加成反应,反应②是乙烯与水的加成反应,反应③是乙醇的催化氧化反应,反应⑧是乙醇的消去反应,错误;B项,图中物质中能与NaOH溶液反应的有乙酸、乙酸乙酯和1,2二溴乙烷,错误;C项,1,2二溴乙烷、乙烯上的氢原子被氯原子取代,其一氯取代产物都是一种,但乙醇烃基上的氢原子被氯原子取代,其一氯取代产物有2种,错误;D项,乙醇的化学式可看作C2H4·H2O,所以等物质的量的乙烯和乙醇与足量氧气反应时耗氧量相同,正确。
【答案】D
【练后反思】牢记常见烃的衍生物的转化关系:
【变式训练】(2020·湖北沙市综合检测)化合物Z是合成平喘药沙丁胺醇的中间体,可通过下列路线制得:
下列说法正确的是( )
A.1 mol Z最多能与2 mol NaOH反应
B.Y可以发生取代反应、氧化反应、消去反应
C.可用FeCl3溶液鉴别Y和Z
D.X分子中所有原子在同一平面上
【解析】A项,1 mol Z分子中含2 mol酯基,发生水解后,生成的2 mol羧基和1 mol酚羟基均能与NaOH发生反应,所以1 mol Z最多能与3 mol NaOH反应,错误;B项,Y分子中的氯原子可发生取代反应,酚羟基可被氧化,但该分子不能发生消去反应,错误;C项,含酚羟基的有机物遇FeCl3溶液会显紫色,因Y分子中含酚羟基,而Z中不含酚羟基,则可用FeCl3溶液鉴别Y和Z,正确;D项,X分子中含甲基,为四面体结构,所以X分子中所有原子不可能在同一平面上,错误。
【答案】C
高考化学一轮复习讲练 第11章 第34讲 烃的含氧衍生物 (含解析): 这是一份高考化学一轮复习讲练 第11章 第34讲 烃的含氧衍生物 (含解析),共27页。试卷主要包含了醇类、苯酚的物理性质,32 g等内容,欢迎下载使用。
第34讲 烃的含氧衍生物(精练)-2022年高考化学一轮复习讲练测: 这是一份第34讲 烃的含氧衍生物(精练)-2022年高考化学一轮复习讲练测,文件包含第34讲烃的含氧衍生物精练-2022年一轮复习讲练测原卷版docx、第34讲烃的含氧衍生物精练-2022年一轮复习讲练测解析版docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。
第29讲 化学综合实验(精讲)-2022年高考化学一轮复习讲练测: 这是一份第29讲 化学综合实验(精讲)-2022年高考化学一轮复习讲练测,文件包含第29讲化学综合实验精讲-2022年一轮复习讲练测原卷版docx、第29讲化学综合实验精讲-2022年一轮复习讲练测解析版docx等2份试卷配套教学资源,其中试卷共52页, 欢迎下载使用。












