
2022届高三化学每天练习20分钟——原电池原理及基于“桥和膜”的双液原电池
展开一、选择题:每小题只有一个选项符合题意。
1.一种光化学电池的结构如图所示,电池总反应式为AgCl(s)+Cu+(aq)===Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是( )
A.生成108 g银,转移电子个数为2NA
B.Cu+在负极发生氧化反应
C.Ag电极活泼,Ag失电子发生氧化反应
D.Cl-由负极迁移到正极
2.(2019·深圳调研)如图是一种正投入生产的大型蓄电系统,放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是( )
A.放电时,负极反应为3NaBr-2e-===NaBr3+2Na+
B.充电时,阳极反应为2Na2S2-2e-===Na2S4+2Na+
C.放电时,Na+经过离子交换膜,由b池移向a池
D.用该电池电解饱和食盐水,产生2.24 L H2时,b池生成17.40 g Na2S4
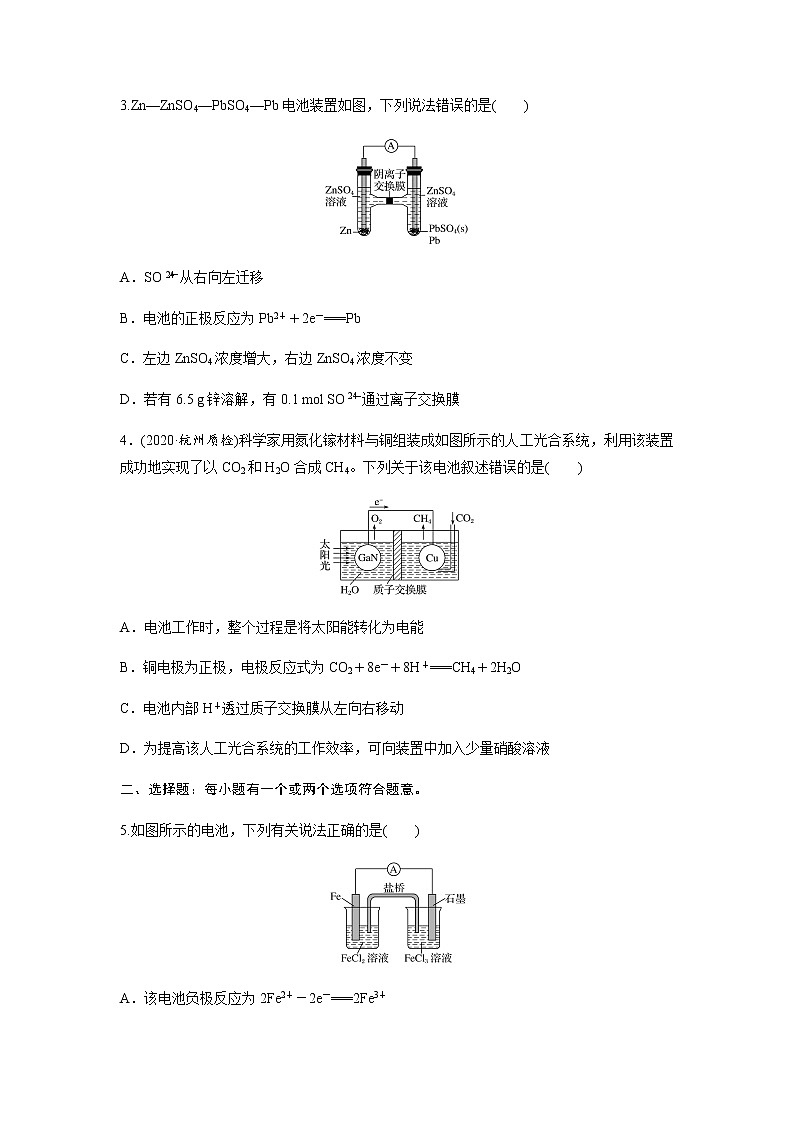
3.Zn—ZnSO4—PbSO4—Pb电池装置如图,下列说法错误的是( )
A.SOeq \\al(2-,4)从右向左迁移
B.电池的正极反应为Pb2++2e-===Pb
C.左边ZnSO4浓度增大,右边ZnSO4浓度不变
D.若有6.5 g锌溶解,有0.1 ml SOeq \\al(2-,4)通过离子交换膜
4.(2020·杭州质检)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。下列关于该电池叙述错误的是( )
A.电池工作时,整个过程是将太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+===CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
D.为提高该人工光合系统的工作效率,可向装置中加入少量硝酸溶液
二、选择题:每小题有一个或两个选项符合题意。
5.如图所示的电池,下列有关说法正确的是( )
A.该电池负极反应为2Fe2+-2e-===2Fe3+
B.当有6.02×1023个电子转移时,Fe电极减少56 g
C.石墨电极上发生氧化反应
D.盐桥中K+移向FeCl3溶液
6.(2019·咸阳质检)利用如图所示电池装置可以将温室气体CO2转化为可燃气体CO,其中含有的固体电解质能传导质子(H+)。下列说法正确的是( )
A.该过程中有两种形式的能量转化
B.a电极表面的反应为4OH--4e-===2H2O+O2↑
C.该装置工作时,H+从a电极区向b电极区移动
D.该装置中每生成2 ml CO,同时生成1 ml O2
三、非选择题
7.某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)____________________设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________ ml电子。
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为__________________,这是由于NH4Cl溶液显________________(填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的原因________________________________________________________,
用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式:____________________________________________________________________
______________________________________________________________________________,
然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeOeq \\al(2-,4),试写出该反应的离子方程式:__________________________________。
(3)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O3Zn(OH)2+2Fe(OH)3+4KOH
放电时正极附近溶液的碱性________(填“增强”“减小”或“不变”);放电时每转移3 ml电子,有________ ml K2FeO4被________(填“氧化”或“还原”)。
答案精析
1.B
2.C [结合图像和题给信息分析,放电时,负极反应为2Na2S2-2e-===Na2S4+2Na+,正极反应为NaBr3+2Na++2e-===3NaBr,A项错误;充电时,阳极反应和放电时原电池的正极反应互为逆过程,即充电时的阳极反应为3NaBr-2e-===NaBr3+2Na+,B项错误;放电时,原电池中阳离子移向正极,故Na+经过离子交换膜由b池移向a池,C项正确;用该电池电解饱和食盐水,整个过程得、失电子数目相等,但未指明是否在标准状况下,无法根据生成氢气的体积计算转移的电子数,D项错误。]
3.B 4.D
5.D [该原电池中,铁作负极,石墨作正极。负极上铁失电子发生氧化反应,电极反应式为Fe-2e-===Fe2+,A项错误;当有6.02×1023个电子转移时,Fe电极减少的质量为eq \f(6.02×1023,6.02×1023 ml-1)×eq \f(1,2)×56 g·ml-1=28 g,B项错误;石墨作正极,正极上Fe3+得电子发生还原反应,C项错误;盐桥中K+移向正极,即移向FeCl3溶液,D项正确。]
6.CD
7.(1)Fe+Cu2+===Fe2++Cu 0.2
(2)2H++2e-===H2↑ 酸性
NHeq \\al(+,4)+H2ONH3·H2O+H+
2Fe2++Cl2===2Fe3++2Cl-
2Fe3++3Cl2+8H2O===2FeOeq \\al(2-,4)+6Cl-+16H+
(3)增强 1 还原
人教版 (2019)选择性必修1第一节 原电池第一课时达标测试: 这是一份人教版 (2019)选择性必修1第一节 原电池第一课时达标测试,共10页。试卷主要包含了关于右图装置的叙述,正确的是,有关电化学知识的描述正确的是等内容,欢迎下载使用。
2022届高考化学一轮复习 微题型48 原电池原理及基于“桥和膜”的双液原电池(解析版): 这是一份2022届高考化学一轮复习 微题型48 原电池原理及基于“桥和膜”的双液原电池(解析版),共4页。试卷主要包含了某原电池装置如图所示等内容,欢迎下载使用。
高三化学每天练习20分钟——原电池原理及基于“桥和膜”的双液原电池(有答案和详细解析): 这是一份高三化学每天练习20分钟——原电池原理及基于“桥和膜”的双液原电池(有答案和详细解析),共4页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












