




高中化学苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物集体备课课件ppt
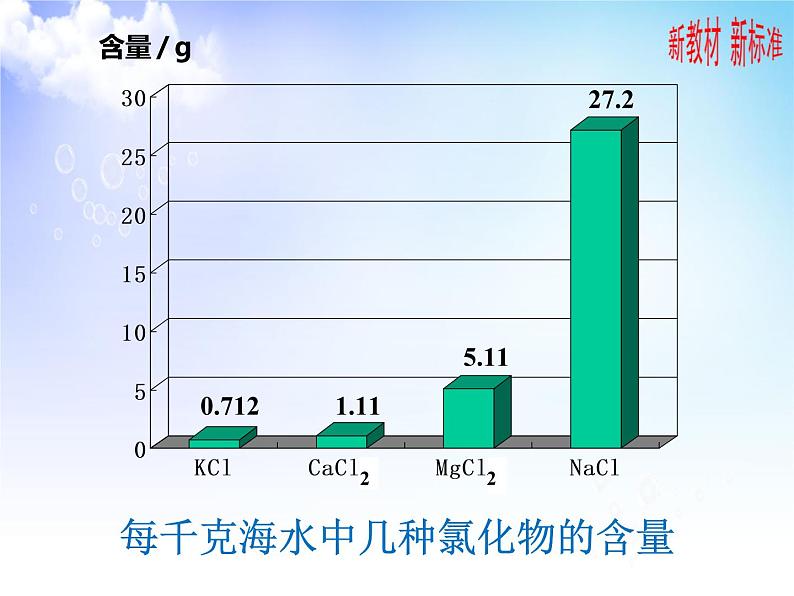
展开每千克海水中几种氯化物的含量
人们是如何从海水中获得氯化钠的?
NaCl俗名“食盐”,它有哪些用途呢?
医学:配成浓度为 0.9%的“生理盐水”。
生活:我们餐桌上的必需调味品。
工业:电解饱和食盐水制取氯气。
1774年,瑞典化学家舍勒把浓盐酸与软锰矿混在一起加热发现了氯气。
1810年,英国化学家戴维研究后得出这种气体仅由一种元素组成。我国早年译文将其译成“绿气”,后改为氯气。
(二)氯气的实验室制法
1、电解熔融氯化钠制取氯气和金属钠。
2、电解饱和食盐水制取氯气。
工业上是如何由氯化钠获得氯气的?
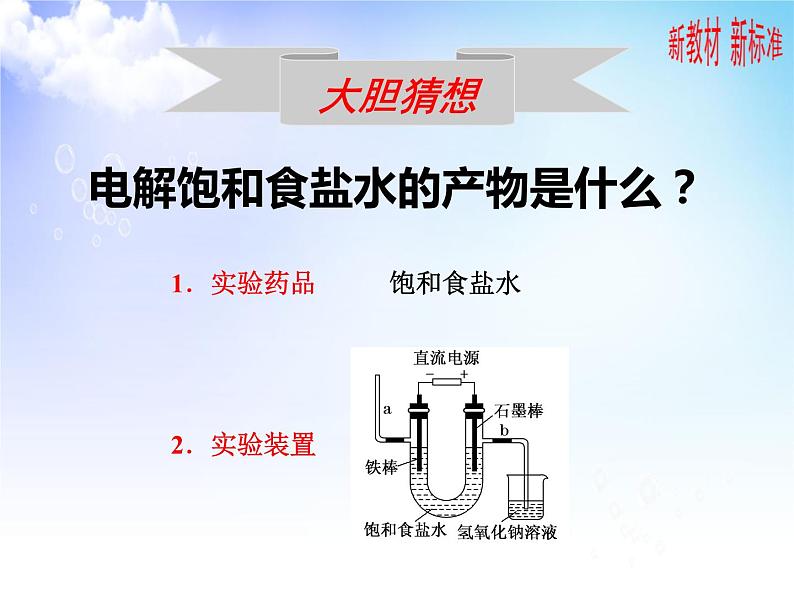
电解饱和食盐水的产物是什么?
1.实验药品 饱和食盐水
实验探究——电解饱和食盐水
观看实验视频,观察实验现象
提示:氯气的检验方法 使湿润的淀粉碘化钾试纸变蓝
黄绿色气体,遇湿润的淀粉碘化钾试纸变蓝
无色气体靠近火焰有爆鸣声
接通电源,两极均有气泡产生
1、以电解食盐水为基础制取氯气等产品的工业称为 ,电解饱和食盐水的化学方程式为 。 2、与电源正极相连的电极上产生 ,与电源负极相连的电极上产生 。
例1.图为教科书中电解饱和食盐水的 实验装置。据此,下列叙述不正 确的是 ( ) A.装置中,a管收集的是氢气 B.b管导出的是氯气 C.以食盐水为基础原料制取氯气等产品的工业称为 “氯碱工业” D.在石墨棒电极区域有NaOH产物
例2.氯化钠和水都是稳定的化合物,使它们发生分解 十分困难,电解饱和食盐水条件是 ( ) A.加热情况下 B.常温常压下 C.通直流电情况下 D.通交流电情况下
阅读下面资料,你能了解氯气的哪些性质?
1915年04月22日,在第一次世界大战的比利时战场上,德军正与英法联军对峙。忽然,从处于上风口的德军阵地上升起一股股黄绿色的云团,有强烈的刺激性气味,一直飘向处于下风口的英法阵地。毫无准备的英法士兵猝不及防,眼看着黄绿色的气体涌来,两万余名士兵先是咳嗽继而喘息,大多数士兵因中毒导致死亡。经统计,最终活下来的士兵大部分都是在黄绿色云团飘来时跑到了较高的山丘上才幸免于难,还有一些人是用湿手绢捂住了嘴才保住了性命,而这种使上万人丧命的气体就是氯气,而这场战争也作为战争史上第一次化学战记入了史册。
1. 黄绿色的气体2. 有刺激性气味3. 有毒4. 密度比空气大5. 易液化6. 能溶于水(常温下1体积的水中大约能溶解2体积的氯气)
1.实验药品: 二氧化锰 (固体)、浓盐酸 (液体)
1. 根据制取氯气原料的状态和反应条件,制取装置 有什么特点?
气体发生装置的选择是根据反应物的状态和反应条件来确定的。
2. 根据氯气密度比空气大,能溶于水而难溶于饱和 食盐水,收集装置有什么特点?
3. 氯气收集满了能任意排放吗?用什么试剂来吸收 多余氯气?
这样收集到的氯气纯净吗?
4. 此法制得的氯气纯净吗?可能存在哪些杂质气体? 用哪些试剂来除杂,有没有先后顺序?
一套完整的制取气体的实验装置
1、为什么用分液漏斗装盐酸?为什么让 盐酸缓慢地注入,而不是一次将浓盐 酸注入烧瓶里?
答:用分液漏斗可以控制液体的用量,避免 生成的氯气过多。
2、能否用其它试剂代替二氧化锰或浓盐 酸来制取氯气?
3、为什么用浓盐酸和二氧化锰制取氯气 时,要缓缓加热,不能强热 ?
答:浓盐酸有很强的挥发性,强热时能挥发 出大量的氯化氢气体和水蒸气,而使制 得的氯气中含有大量杂质;另一方面, 又降低了HCl的利用率。
4、如何检验氯气的生成?
答:1. 黄绿色、有刺激性气味的气体 (色、态、味); 2. 湿润的淀粉KI试纸 (变蓝); 3. 湿润的品红试纸 (褪色); 4. 浓氨水 (白烟)。
先验密,后实验;先固体,后液体;先撤管,后撤灯;先除HCl,后除H2O;先除杂,后收集。 验密: 向吸收尾气的烧杯中加水浸没长玻璃导管约 2cm,关闭分液漏斗活塞,点燃酒精灯,微热圆底烧瓶。若烧杯中有气泡产生,且停止加热后,导管中形成一段稳定的水柱,说明装置的气密性良好。
5、几项操作的先后顺序
同一种装置采用不同的操作方法,有不同的用途
请思考图示的装置都有哪些用途?
1. 从A口进气,从B口排出瓶内的空气,可收集O2、Cl2等比空气重的气体 —— 向上排空气法 2. 从B口进气,从A口排出瓶内的空气,可收集H2、NH3等比空气轻的气体 —— 向下排空气法 3.在瓶内充满水,从B口进气,将瓶内水从A口压出,可作为排水取气装置。
在瓶内加入适量液体净化剂,从A口进气,B口出气,可作为气体净化装置。
若要测定实验制得的少量O2的体积,应在瓶内先装满水,再将O2从B端通入,A端用长导管接入量筒中。
例3.实验室用KMnO4制氧气,为除去粘附在 试管壁上的MnO2,可用试剂是 ( ) A.汽油 B.水 C.稀盐酸 D.浓盐酸
例4.实验室制氯气时有如下操作,操作顺序正确的 是 ( ) ①.连接好装置,检查气密性 ②.缓缓加热,加快反应,使气体均匀逸出 ③.在烧瓶中加入二氧化锰粉末 ④.往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤.用向上排空气法收集氯气,尾气导入吸收剂中 A.①②③④⑤ B.④③①②⑤ C.①③④②⑤ D.①④③②⑤
例5.某学生设计如图实验装置用于制备纯净的Cl2
高中化学苏教版 (2019)必修 第一册专题3 从海水中获得的化学物质第一单元 氯气及氯的化合物精品ppt课件: 这是一份高中化学苏教版 (2019)必修 第一册专题3 从海水中获得的化学物质第一单元 氯气及氯的化合物精品ppt课件,共24页。PPT课件主要包含了含量g,海水中都有什么呢,学习目标,化学式Cl2,氯气的生产原理,一氯气的工业制法,电解饱和食盐水,实验原理,两极均产生气泡,有氢气生成等内容,欢迎下载使用。
高中化学苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物备课ppt课件: 这是一份高中化学苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物备课ppt课件,共40页。
苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物备课课件ppt: 这是一份苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物备课课件ppt,共46页。PPT课件主要包含了学业基础,NaCl+2H2O,电解装置,电解产物的验证,NaOH,实验装置,答案D,核心素养,淀粉KI溶液变蓝,除去Cl2中的氯化氢等内容,欢迎下载使用。













