

计算题集训2(解析版)
展开(1)写出你所选择酸(W)的化学式 。
(2)铜粉中混有铁粉的质量是 。
(3)计算你选择酸(W)的质量分数(写出计算过程)。
【答案】(1)H2SO4(或HCl)(2)0.98g(3)9.8%或7.3%(详见解析)
【解析】解:(1)铁的金属活动性排在氢的前面,会置换出硫酸或盐酸中的氢,所以所选择酸(W)的化学式是:H2SO4(或HCl);
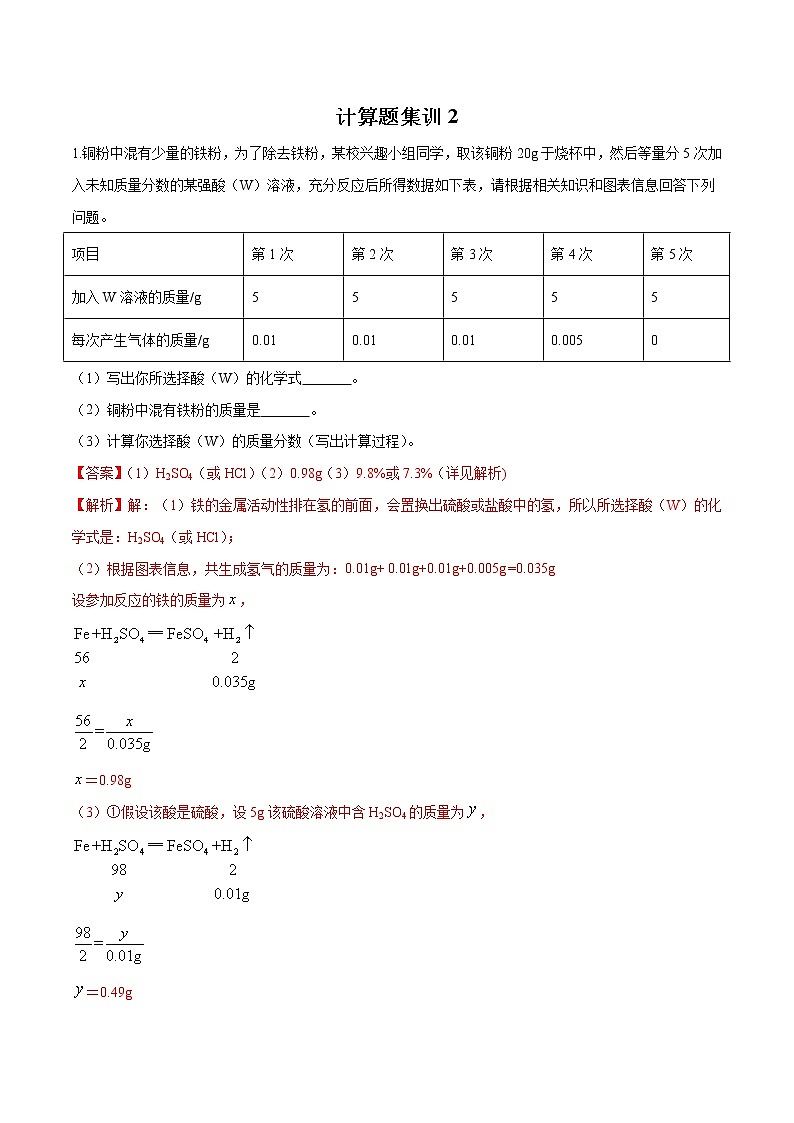
(2)根据图表信息,共生成氢气的质量为:0.01g+ 0.01g+0.01g+0.005g =0.035g
设参加反应的铁的质量为,
=0.98g
(3)①假设该酸是硫酸,设5g该硫酸溶液中含H2SO4的质量为,
=0.49g
该硫酸溶液中溶质的质量分数为×100%=9.8%;
答:该硫酸溶液中溶质的质量分数为9.8%。
②假设该酸是盐酸,设5g该盐酸溶液中含HCl的质量为,
=0.365g
该盐酸溶液中溶质的质量分数为×100%=7.3%。
答:若选择的酸为硫酸,该硫酸溶液中溶质的质量分数为9.8%;
若选择的酸为盐酸,则质量分数为7.3%。
2.某潜水艇上有 100 人,如果每人每分钟耗氧气为 0.001kg,假如所需要的氧气全部由 Na2O2 与 CO2 反应来提供, 则一天消耗 O2 的质量为 ,该潜水艇一天所需要 Na2O2 的质量是多少?(提示:)
【答案】144kg;702kg
【解析】解: 100 人一天消耗 O2 的质量为:100×0.001kg×60×24=144kg。
设潜水艇一天所需要 Na2O2 的质量是x。
,解得x=702kg
3.“二氧化碳的实验室制取与性质”实验活动产生的废液中含稀盐酸,需先测定其溶质质量分数后进行处理。(杂质不参加反应)
(1)实验时需配制50g5%的氢氧化钠溶液,若用氢氧化钠固体和水来配制,则需称量氢氧化钠固体的质量为_____g。
(2)取20g废液样品于烧杯中,向其中逐滴加入5%的氢氧化钠溶液,恰好完全反应时共消耗氢氧化钠溶液16g。计算废液中盐酸的溶质质量分数。(写出计算过程)
(3)恰好完全反应时烧杯中的溶液所含粒子数目关系:Na+_____Cl-。(填“>”、“=”或“<”)
【答案】(1)2.5;(2)3.65%(过程见解析);(3)<
【解析】(1)氢氧化钠质量:50g×5%=2.5g,故填:2.5。
(2)设:盐酸溶质质量分数为x。
答:废液中盐酸的溶质质量分数3.65%。
(3)实验室用稀盐酸和石灰石或大理石制取二氧化碳,废液中还有氯化钙,故氯离子数目大于钠离子数目,故填:<。
4.为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
【答案】(1)80%(2)8.8g(详见解析)(3)不能,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止
【解析】由图可以看固体减少了20g即碳酸钙的质量为20g,根据碳酸钙的质量和对应的化学方程式求算氯化钙和二氧化碳的质量,进而求算对应的质量分数。
(1)由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为;
(2)设恰好反应时,产生二氧化碳的质量为x
x=8.8g
(3)本实验不可以用稀硫酸代替稀盐酸完成实验,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止。
年12月,网上报道某公司非法使用草甘膦转基因大豆。草甘膦(化学式为C3H8NO5P)是一种有机磷除草剂,白色结晶,易溶于水、乙醇等,不可燃,常温下稳定。计算:
(1)草甘膦中碳元素与氧元素的质量比为_________________。
(2)草甘膦中磷元素的质量分数为_________________。(精确到0.1%)
(3)33.8克草甘膦中含有多少克磷元素?(写出计算步骤,精确到小数点后一位)____
【答案】9:20 18.3% 6.2g
【解析】(1)分子中含3个碳原子和5个氧原子,草甘膦分子中碳元素与氧元素的质量比为
(2)草甘膦的相对分子质量为,所以磷元素的质量分数为
(3)33.8克草甘膦中含有磷元素的质量为
6.化肥对提高农作物的产量具有重要作用。硝酸铵(NH4NO3)是一种常见的氮肥。计算
(1)硝酸铵由 种元素组成(填数字);
(2)硝酸铵中氮元素和氧元素的质量比为 (填最简比);
(3)若硝酸铵中含有2.8g氮元素,则该硝酸铵质量为 g。
【答案】(1)3 (2)7:12 (3)8
【解析】 化合物中各元素的质量比为相对原子质量乘以原子个数之比。
(1)硝酸铵的化学式为NH4NO3,硝酸铵由氮元素、氢元素、氧元素共3种元素组成。
(2)硝酸铵的化学式为NH4NO3,硝酸铵中氮元素和氧元素的质量比为。
(3)若硝酸铵中含有2.8g氮元素,则该硝酸铵的质量为。
7.丙氨酸(化学式为C3H7NO2)是构成蛋白质的一种氨基酸。请计算:
(1)丙氨酸中碳、氢、氮、氧原子的个数比为 。
(2)丙氨酸中质量分数最大的元素是 。
(3)178g丙氨酸中氧元素的质量为________g。
【答案】(1)3:7:1:2(2)碳(或C)(3)64
【解析】(1)化学式中元素符号右下角的数字为一个分子中原子的个数,丙氨酸中碳、氢、氮、氧原子的个数比为3:7:1:2;
(2)丙氨酸中碳、氢、氮、氧元素的质量比为:(3×12):(7×1):(1×14):(2×16),=36:7:14:32,碳元素的质量分数最大;
(3)178g丙氨酸中氧元素的质量为:178g×=64g。
8.新冠肺炎疫情期间,为了做好自我保护,可用酒精溶液消毒。乙醇俗称酒精(化学式为C2H5OH),请回答下列问题:
(1)乙醇的相对分子质量为多少。
(2)乙醇分子中C、H、O原子个数比为多少。
(3)92g乙醇中碳元素的质量为多少g。
【答案】(1)46(2)2:6:1(3)48
【解析】 相对分子质量是指化学式中各个原子的相对原子质量的总和。
(1)乙醇的化学式为C2H5OH,故乙醇的相对分子质量为。
(2)乙醇的化学式为C2H5OH,则1个乙醇分子由2个碳原子,6个氢原子,1个氧原子,故乙醇分子中C、H、O原子个数比为。
(3)92g乙醇中碳元素的质量为。
【点睛】
9.合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
【答案】0.2;6.5;16.1%
【解析】(1)根据质量守恒定律,加入稀硫酸恰好完全反应后,烧杯内物质总质量减少质量即为生成氢气的质量,故生成氢气的质量为10g+93.7g-103.5g=0.2g;设黄铜中锌的质量为x,则
解得x=6.5g;
故黄铜中锌的质量为6.5g。
(2)样品中锌与加入的稀硫酸恰好完全反应,设生成硫酸锌的质量为y,则
解得y=16.1g;
根据质量守恒定律,所得溶液质量为6.5g+93.7g-0.2g=100g,故过滤后所得溶液的溶质质量分数为。
10.将20.0g NaOH、Ca(OH)2、NaCl组成的固体混合物溶于水配成溶液,向混合液中缓慢通入CO2气体(气体的溶解忽略不计),生成沉淀的质量与通入CO2气体的质量关系如图所示,请根据题意回答问题:
已知:Na2CO3+CO2+H2O═2NaHCO3
NaHCO3+NaOH═Na2CO3+H2O
(1)经分析,A点溶液中所含溶质为 (填化学式)。
(2)在B点时,溶液里碳元素均存在于NaHCO3中,若B点后继续通入足量的CO2气体,请将图象补充完整。
(3)该混合物中NaCl的质量分数为多少?(写出计算过程,计算结果精确至0.1%)
【答案】(1)NaOH、NaCl (2) (3)35%(详见解析)
【解析】(1)根据二氧化碳与氢氧化钙的反应分析A点溶液中所含溶质;
(2)根据碳酸钙与二氧化碳的反应画出B点后继续通入足量的CO2气体与沉淀的关系;
(3)根据碳酸钙沉淀的质量可计算出氢氧化钙的质量,根据与氢氧化钠反应二氧化碳的质量计算出氢氧化钠的质量可计算出氢氧化钠的质量,即可计算出混合物中NaCl的质量及质量分数。
【详解】(1)向NaOH、Ca(OH)2、NaCl的混合溶液缓慢通入CO2气体,A点时二氧化碳与氢氧化钙恰好反应,溶液中所含溶质为:NaOH、NaCl;
(2)设与碳酸钙反应的二氧化碳的质量为x
解得:x=4.4g
所以消耗二氧化碳的总质量为10.56g+4.4g=15g。所以若B点后继续通入足量的CO2气体,将图象补充完整如下:
。
(3)设氢氧化钙的质量为y
解得:y=7.4g
由图示可知,与氢氧化钠反应转化为碳酸氢钠的二氧化碳的质量为:10.56g﹣4.4g=6.16g。
设氢氧化钠的质量为z,
解得:z=5.6g
该混合物中NaCl的质量分数为:=35%。
答:该混合物中NaCl的质量分数为35%。
项目
第1次
第2次
第3次
第4次
第5次
加入W溶液的质量/g
5
5
5
5
5
每次产生气体的质量/g
0.01
0.01
0.01
0.005
0
计算题集训1(解析版): 这是一份计算题集训1(解析版),共8页。试卷主要包含了下列说法中正确的是,8%,取6等内容,欢迎下载使用。
实验题集训之创新实验(解析版): 这是一份实验题集训之创新实验(解析版),共22页。
实验题集训之重点实验汇编(解析版): 这是一份实验题集训之重点实验汇编(解析版),共10页。试卷主要包含了下列实验方案合理的是,下列实验方案设计合理的是,下列实验方案设计正确的是等内容,欢迎下载使用。












