
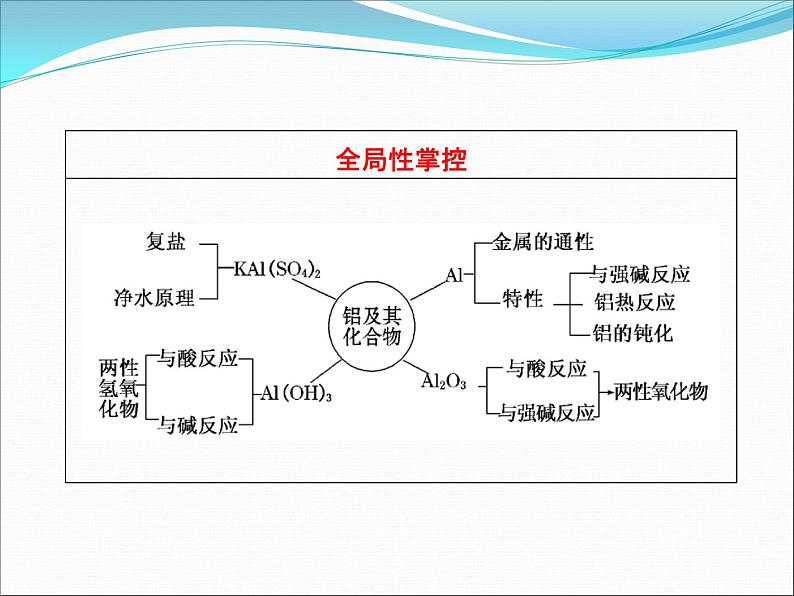




高考化学第一轮复习课件:铝及其化合物
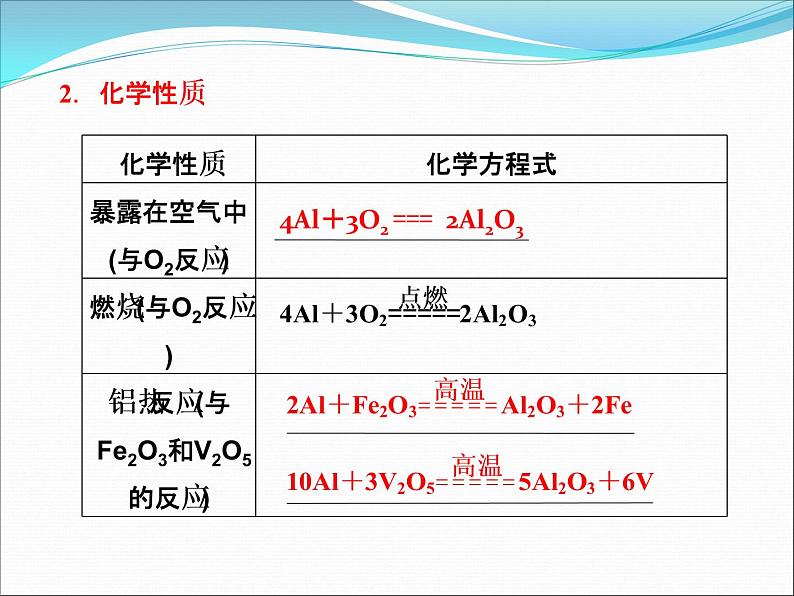
展开一、铝的性质1.物理性质铝是 色的轻金属,熔点 ,硬度 ,有良好的导电、导热性.
4Al+3O2 === 2Al2O3
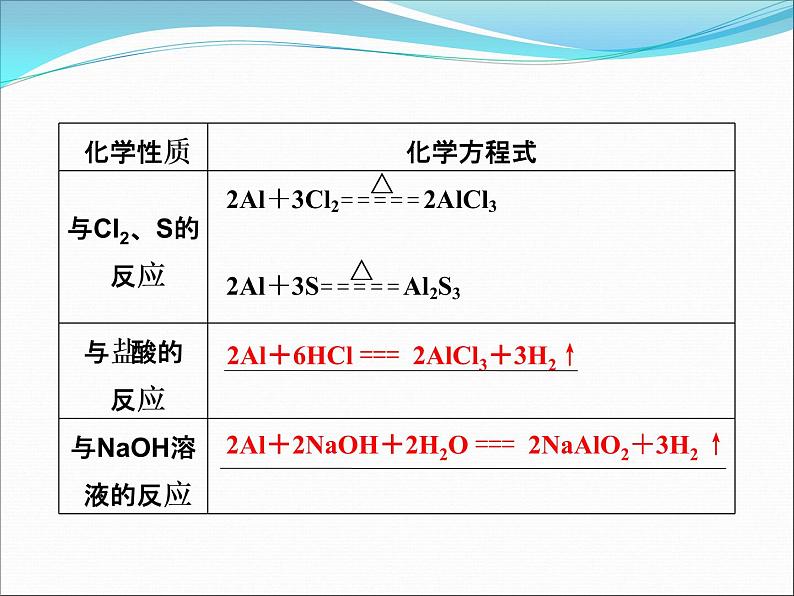
2Al+6HCl === 2AlCl3+3H2↑
2Al+2NaOH+2H2O === 2NaAlO2+3H2 ↑
1.如何除去铁粉中的铝粉?
提示:加入过量NaOH溶液,然后过滤、洗涤、干燥.
二、铝的重要化合物1.氧化铝(1)化学性质(用离子方程式表示)
(2)用途熔点很高,是一种较好的 ,还可制作各种宝石.
2.氢氧化铝(1)化学性质
②受热分解: .
2.既能与酸反应又能与碱反应的物质有哪些?
提示: ①Al、②Al2O3、③Al(OH)3、④弱酸的铵盐,如:(NH4)2CO3、CH3COONH4、⑤弱酸的酸式盐,如:NaHCO3、NaHSO3、NaHS等
(2)制备①向铝盐溶液中加入氨水②向偏铝酸盐溶液中通入足量CO2 .
3.明矾明矾的化学式:净水原理涉及的反应: .
KAl(SO4)2·12H2O
Al3++3H2O === Al(OH)3
1.下列有关金属铝及其化合物的叙述正确的是 ( )A.铝在常温下不能与氧气反应 B.铝不能与氯气反应C.铝既能溶于酸,又能溶于碱D.氧化铝只能与酸反应,不能与碱反应
2.(2011·东北名校二模)铝是一种低毒金属元素,它并非人体需要的微量元素,不会导致急性中毒,但食品中铝的含量超过国家标准就会对人体造成危害.下列关于铝元素的说法正确的是 ( )A.铝在空气中不易氧化是因为性质不活泼B.氢氧化铝可与胃酸反应,常用作中和胃酸的药物C.明矾可用于饮用水的杀菌消毒D.硫酸铝铵常用作面粉膨化剂,该物质不溶于水
3.将表面已完全钝化的铝条插入下列溶液中,不会发生反应的是 ( )A.稀硝酸 B.稀盐酸C.硝酸铜 D.氢氧化钠
4.(2011·聊城联考)用含有少量Mg的Al片制取纯净的Al(OH)3,下列操作中最恰当的组合是 ( )①加入盐酸溶解 ②加NaOH溶液 ③过滤 ④通入过量CO2生成Al(OH)3 ⑤加盐酸生成Al(OH)3 ⑥加过量氨水生成Al(OH)3A.①⑥③ B.①③⑥③C.②③④③ D.②③⑤③
5.某校化学兴趣小组用如下图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失.
[例1] (2009·上海高考)镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图.反应中镁和铝的( )A.物质的量之比为3∶2B.质量之比为3∶2C.摩尔质量之比为2∶3D.反应速率之比为2∶3
金属与酸或碱反应的实质是金属失电子,金属失去的电子数等于生成H2中的氢原子数,常用的方法有守恒法和平均值法(即求混合金属的平均相对原子质量).
1.将5.4 g Al投入200.0 mL 2.0 ml·L-1的某溶液中有氢气产生,充分反应后有金属剩余,该溶液可能为 ( )A.HNO3溶液 B.Ba(OH)2溶液C.H2SO4溶液 D.HCl溶液
2.有两种金属的混合物7 g,与足量稀盐酸反应后放出标准状况下H2 5.6 L,则混合物不可能的组合是 ( )A.Zn、Fe B.Fe、MgC.Mg、Zn D.Mg、Al
1.“铝三角”是指Al3+、Al(OH)3和AlO 相互转化的三角关系(如下图)
[例2] 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比( )
A.6∶1 B.3∶1C.2∶1 D.1∶2
3.向含有a ml氯化铝的溶液中加入含有b ml氢氧化钠的溶液,生成沉淀的量可能是 ( )①a ml ②b ml ③a/3 ml ④b/3 ml ⑤0⑥(4a-b)mlA.①②③④⑤⑥ B.①②④⑤⑥C.①④⑤⑥ D.①③⑤
高考化学一轮复习课件8 铝、镁及其化合物(含解析): 这是一份高考化学一轮复习课件8 铝、镁及其化合物(含解析),共44页。PPT课件主要包含了镁及其化合物,铝的性质,铝的结构和存在,第三周期第ⅢA族,金属铝的物理性质,银白色,金属铝的化学性质,形成致密的氧化膜,铝的用途,补充铝热反应等内容,欢迎下载使用。
人教版高考化学一轮复习3.3铜铝及其化合物金属资源课件: 这是一份人教版高考化学一轮复习3.3铜铝及其化合物金属资源课件
高考化学一轮复习第3章金属及其化合物第2节镁铝及其化合物课件: 这是一份高考化学一轮复习第3章金属及其化合物第2节镁铝及其化合物课件,共60页。PPT课件主要包含了必备知识·关键能力,考点一考点二,第三周期ⅢA族,H2↑,AlOH3胶体,拓展链接·素养提升,拓展1,真题验收·新题预测,真题验收新题预测等内容,欢迎下载使用。












