






高中化学人教版 (新课标)选修6 实验化学课题二 物质的制备说课课件ppt
展开实验2-4 硫酸亚铁铵的制备P25
江西省鹰潭市第一中学 桂耀荣
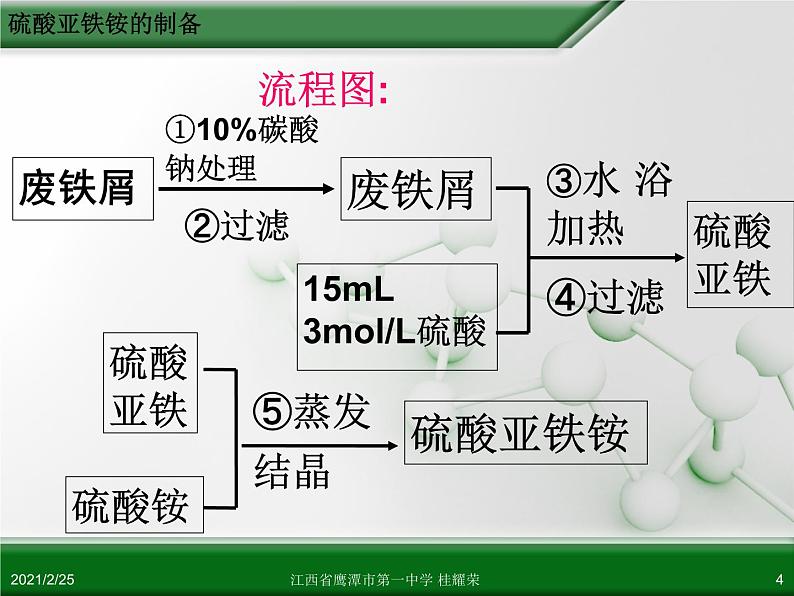
亚铁盐在空气中易被氧化,但形成复盐硫酸亚铁铵FeSO4·(NH4)2SO4·6H2O后可稳定存在。 FeSO4 + (NH4)2SO4 + 6H2O = FeSO4·(NH4)2SO4·6H2O而硫酸亚铁可由铁屑和稀硫酸反应制得。 Fe + H2SO4 = FeSO4 + H2↑
15mL 3ml/L硫酸
计算产率:计算得理论产量应为为19.6g。实际称得产品约12.2g 。产率约为62% 。不过因为产品是用滤纸压干,会混有水份,实际产率应更低些。
实验体会: 1. 制备硫酸亚铁时要保持铁过量,水浴加热。2. 硫酸亚铁铵的制备:加入硫酸铵后,应使其充分溶解后再往下进行。这样有利于保证产品的纯度。蒸发时要缓缓加热,以防局部过热。
3. 实验过程中应保持足够的酸度。如果溶液的酸性减弱,则亚铁盐(或铁盐)中Fe2+与水作用的程度将会增大。在制备(NH4)2SO4·FeSO4·6H2O过程中,为了使Fe2+ 不与水作用,溶液需要保持足够的酸度。
资料:加快过滤速度的一种方法—— 减压过滤(抽滤)P27
高中化学人教版 (新课标)选修6 实验化学课题二 物质的制备示范课ppt课件: 这是一份高中化学人教版 (新课标)选修6 实验化学课题二 物质的制备示范课ppt课件,共10页。PPT课件主要包含了实验记录表等内容,欢迎下载使用。
化学选修6 实验化学第二单元 物质的获取课题二 物质的制备授课课件ppt: 这是一份化学选修6 实验化学第二单元 物质的获取课题二 物质的制备授课课件ppt,共22页。PPT课件主要包含了问题探讨等内容,欢迎下载使用。
高中化学人教版 (新课标)选修6 实验化学课题二 化学实验的绿色追求评课ppt课件: 这是一份高中化学人教版 (新课标)选修6 实验化学课题二 化学实验的绿色追求评课ppt课件,共13页。PPT课件主要包含了本节学习目标,化学实验的绿色追求,什么是绿色化学,绿色化学的最大特点,阅读资料,思考与练习,实践活动,思考与交流等内容,欢迎下载使用。













