高中化学人教版 (新课标)必修2第二节 来自石油和煤的两种基本化工原料精品第1课时同步测试题
展开第二节 元素周期律 第1课时 原子核外电子的排布
一、核外电子的分层排布
1.电子的能量
(1)在多电子原子里,电子的能量________。
(2)在离核较近的区域内运动的电子的能量________,在离核较远的区域内运动的电子的
能量________。
2.电子层
(1)概念:在多电子的原子里,电子运动的________的区域简化为________的壳层,称作
电子层。
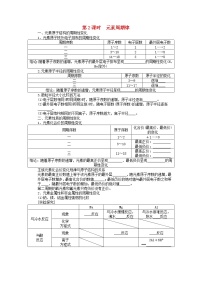
(2)不同电子层的表示方法及能量关系
电子层序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | …… |
电子层符号 | K | L | M | N | O | P | Q | …… |
电子离核距离 |
|
|
|
|
|
|
|
|
电子能量 |
|
|
|
|
|
|
|
|
3.电子层的排布原理
核外电子的排布一般总是尽先从________排起,当一层________后再填充下一层。
4.核外电子的排布规律
分析下表和课本表1-2,填写下列空白:
稀有气体元素原子的核外电子排布
| 各电子层的电子数 | |||||
| K | L | M | N | O | P |
2He(氦) | 2 |
|
|
|
|
|
10Ne(氖) | 2 | 8 |
|
|
|
|
18Ar(氩) | 2 | 8 | 8 |
|
|
|
36Kr(氪) | 2 | 8 | 18 | 8 |
|
|
54Xe(氙) | 2 | 8 | 18 | 18 | 8 |
|
86Rn(氡) | 2 | 8 | 18 | 32 | 18 | 8 |
(1)观察上表可知:除氦元素外,各稀有气体元素原子中最外电子层所能容纳的电子数最
多是____;次外层所能容纳的电子数最多是____;K、L、M、N各电子层所能容纳的电
子数最多依次是____、____、____、____。
(2)在元素周期表中,随着元素核电荷数的增加,在____族元素之后,增加了新的电子层
并出现了新的周期,该元素最外层电子数是____。
研究各元素原子核外电子排布(课本表1-2)可以发现,稀有气体元素的原子各电子层电
子数已达到最多所能容纳的电子数。原子核外各电子层最多容纳的电子数(电子层数为
n)是______。
5.核外电子的分层运动,又叫核外电子的分层排布,其主要规律:
(1)原子核外电子总是先排能量________的电子层,然后由____向____,依次排布在能量
____________的电子层即排满了____层才排____层,排满了____层才排____层。
(2)原子核外每个电子层最多容纳______个电子。
(3)原子最外层电子数不超过____个电子(K层为最外层不能超过_____个电子)。
(4)原子次外层电子数不超过____个电子(K层为次外层不能超过____个电子。)
二、核外电子排布的表示方法——结构示意图
1.原子结构示意图
用小圆圈表示原子核,圆圈内的数字表示核内质子数,弧线表示各电子层,弧线上的数
字表示该电子层上的电子数,这样的图示称为原子结构示意图。例如,钠原子的结构示
意图为:
2.离子结构示意图
离子结构示意图与原子结构示意图写法相同,只是在原子结构示意图中,核内质子数等
于____________;离子结构示意图中,二者____相等。
请写出Mg2+、Cl-的结构示意图:
三、电子的排布与元素性质的关系
1.最外层电子数排满____个(He为____个)形成稳定结构,____________得失电子,化
学性质______。
2.最外层电子较少的(<4)易______电子,达到稳定结构,表现出________;最外层电
子较多的(>4)________电子或形成共用电子对,从而形成稳定结构,表现_____。
3.通常,我们把最外层8个电子(只有K层时为2个电子)的结构,称为相对稳定结构,
一般______其他物质发生化学反应。当元素原子的最外层电子数小于8(K层时小于2)时,
是__________结构。在化学反应中,具有__________结构的原子;总是“想方设法”通
过各种方式使自己的结构趋向于________结构。
知识点一 原子核外电子的能量和运动区域
1.下面关于多电子原子的核外电子的运动规律的叙述正确的是( )
A.核外电子是分层运动的,像卫星一样有确定的轨道
B.所有电子在同一区域里运动
C.能量高的电子在离核近的区域运动
D.能量低的电子在离核近的区域运动
2.下列叙述中不正确的是( )
A.两原子,如果核外电子数相同,则一定属于同种元素
B.不存在两种质子数和电子数均相同的阳离子和阴离子
C.在多电子的原子里不同电子层的核外电子的能量是不相同的
D.两种微粒,若核外电子数相同,则其化学性质一定相同
知识点二 核外电子排布的一般规律
3.在第n电子层中,当它作为原子的最外电子层时,容纳电子数最多与(n-1)层相同,
当它作为原子的次外层时,其电子数比(n+1)层最多能多容纳10个电子,则此电子层是
( )
A.K层 B.L层 C.M层 D.N层
4.有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子
数恰好为A原子L层电子数的2倍。则A、B分别是( )
A.硅原子和钠原子 B.硼原子和氦原子
C.氯原子和碳原子 D.碳原子和铝原子
知识点三 对电子层的考查
5.有两种气态单质Am和Bn,已知2.4 g Am和2.1 g Bn所含的原子个数相等,而分子数
之比为2∶3。又知A和B的原子核内质子数都等于中子数,且A原子L层电子数是K
层的3倍,试推断:
(1)A、B的元素符号分别为____________,____________;
(2)Am中的m值为________。
6.今有甲、乙、丙、丁四种元素,已知:甲元素是地壳中含量最高的元素;乙元素是金
属元素,它的原子核外K、L层电子数之和等于M、N层电子数之和;丙元素的单质及
其化合物的焰色反应都显黄色,氢气在丁元素单质中燃烧火焰呈苍白色。
(1)试推断并写出甲、乙、丙、丁四种元素的名称和符号。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
(2)写出上述元素两两化合生成的化合物的化学式。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
练基础落实
1.核电荷数分别是16和4的元素原子相比较,前者的下列数据是后者4倍的是( )
①质子数 ②最外层电子数 ③电子层数 ④电子总数
A.①② B.①④ C.②③ D.③④
2.两种元素原子的核外电子层数之比与最外层电子数之比相等,则在元素周期表的前
10号元素中,满足上述关系的元素共有( )
A.1对 B.2对 C.3对 D.4对
3.短周期元素中,A元素原子最外层电子数是次外层电子数的2倍;B元素原子最外层
电子数是其内层电子总数的3倍;C元素原子M层电子数等于其L层电子数的一半;D
元素原子最外层有1个电子,D的阳离子与B的阴离子电子层结构相同,则4种元素原
子序数关系中正确的是( )
A.C>D>B>A B.D>B>A>C
C.A>D>C>B D.B>A>C>D
4.根据教材所附元素周期表判断,下列叙述不正确的是( )
A.K层电子为奇数的所有主族元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有主族元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
练方法技巧——判断原子结构示意图技巧
5.下列三种微粒可以归为一类,请选择一项可以归入此类的结构示意图( )
A. B.
C. D.
6.在下列所表示的微粒中,得电子能力最强的是( )
7.A、B为两短周期元素,A元素原子的L层比B元素原子的L层少3个电子,B原子
核外电子总数比A原子核外电子总数多5,则A和B 形成的化合物的化学式为( )
A.A2B3 B.BA2 C.AB4 D.B3A2
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
答案 |
|
|
|
|
|
|
|
练综合拓展
8.有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,其中C、E
是金属元素;A和E元素原子的最外电子层都只有一个电子;B和D元素原子的最外层
电子数相同,且B元素原子L层电子数是K层电子数的3倍;C元素原子的最外层电子
数是D元素原子最外层电子数的一半。
(1)据此推断这五种元素的元素符号。
A.________;B.________;C.________;D.________;
E.________。
(2)分别写出C的最高价氧化物对应水化物与D、E最高价氧化物对应水化物反应的离子
方程式:
________________________________________________________________________、
________________________________________________________________________。
9.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请
你根据下面的提示做出自己的判断。
(1)该微粒是中性微粒,这种微粒的符号是________________________。
(2)该微粒的盐溶液能使溴水褪色,并出现浑浊,这种微粒的符号是__________。
(3)该微粒的氧化性很弱,得到1个电子后变为原子,原子的还原性很强,这种微粒的符
号是__________。
(4)该微粒的还原性很弱,失去1个电子后变为原子,原子的氧化性很强,这种微粒的符
号是_______________________________________________。
第二节 元素周期律
第1课时 原子核外电子的排布
基础落实
一、
1.(1)不同 (2)较低 较高
2.(1)不同 不连续 (2)从上到下:近→远 低→高
3.内层 排满
4.(1)8 18 2 8 18 32 (2)0 1 2n2
5.(1)最低 里 外 逐步升高 K L L M (2)2n2 (3)8 2 (4)18 2
二、
1.
2.核外电子数 不 Mg2+: Cl-:
三、
1.8 2 不易 稳定
2.失去 金属性 易得 非金属性
3.不与 不稳定 不稳定 稳定
对点训练
1.D
2.D [如O2与S电子数相同,但O2分子与S原子化学性质不同。]
3.C 4.D
5.(1)O N (2)3
解析 设B核内质子数为x,则B的质量数为2x,A核外电子数=核内质子数=3×2+2=8,所以A的质量数为16,则·m=·n,得x=7,B为N。
又因为÷= 得n∶m=2∶3,因为N2只有双原子分子,所以m=3,A单质为O3。
6.(1)甲:氧元素O,乙:钙元素Ca,丙:钠元素Na,丁:氯元素Cl。
(2)两两化合形成的化合物的化学式为Na2O、Na2O2、CaO、NaCl、CaCl2。
课后作业
1.B [写出二者的原子结构示意图、对比可知,①④正确。]
2.B [题中的两种元素不可能在同一周期,前10号元素只在前两个周期中,符合条件的只有2对。]
3.A [根据原子核外电子排布规律可知:A元素只有两个电子层,且最外层电子数为4,则A为6号元素;同理B为8号元素。C元素的最外层为M层,且电子数为4,可推知其原子序数为14;B元素形成的阴离子核外电子数为10,故D元素的核电荷数为11。故原子序数的大小顺序为C>D>B>A。]
4.C [逐项判断。A项:K层电子数为奇数,只能是1,这是氢元素所独有,它确实属于ⅠA族,叙述正确;B项:L层电子数为奇数者,可以是1、3、5、7,对应于Li、B、N、F,它们确实属于ⅠA、ⅢA、ⅤA和ⅦA族,叙述也正确;C项:L层电子数为偶数者,可以是2、4、6、8,它们当然可以是Be、C、O、Ne,但8电子填满后,还可以在M层上填充1~8个电子,这是题目未曾界定的,它们可以属于Na、Mg、Al、Si、P、S、Cl等的ⅠA~ⅦA各族,所以本项叙述不正确;D项:M层电子数为奇数的情况,类似于B项中L层电子数为奇数的情况,也是正确的。]
5.C [题给三种微粒的结构示意图均表示阳离子,即核电荷数大于核外电子数,符合此特点的只有C项。]
6.B [四个选项的示意图分别表示碳原子、氟原子、钠离子、铝离子。钠离子和铝离子都形成最外电子层为8个电子的稳定结构,则它们很难得到电子。氟原子比碳原子的核电荷数大,最外层电子数多,原子半径小,原子核对核外电子的吸引力大,因此氟原子比碳原子更易得电子。]
7.D [由题意知:A元素原子的L层比B元素原子的L层少3个电子,A原子核外电子总数比B原子核外电子总数少5个,那么肯定是B原子M层上多了2个电子,而且A元素原子的L层未排满,所以得两者的原子结构示意图为
A:、B:,即A为N,B为Mg,A、B构成Mg3N2,即B3A2。]
8.(1)A:H B:O C:Al D:S E:K
(2)Al(OH)3+3H+===Al3++3H2O
Al(OH)3+OH-===AlO+2H2O
解析 由B元素原子L层电子数是K层电子数的3倍,知B为O,D为S;它们的核电荷数依次增大,C元素原子的最外层电子数是D元素原子最外层电子数的一半,知C为Al;A和E元素原子的最外电子层都只有一个电子,且核电荷数都小于20,知A为H,E为K。根据各元素的性质可解决(2)题。
9.(1)Ar (2)S2- (3)K+ (4)Cl-
解析 (1)该微粒为中性微粒,即核电荷数等于核外电子数,为18号元素氩。(2)该微粒能使溴水褪色,即为还原性微粒,且出现浑浊,即有难溶性的非金属单质生成。符合条件的为硫元素。(3)该微粒得到一个电子可变成原子,故为19号元素钾。(4)该微粒失去一个电子可变成原子,故为17号元素氯。
化学必修2第二节 元素周期律第4课时课时作业: 这是一份化学必修2第二节 元素周期律第4课时课时作业,共5页。试卷主要包含了原子,元素,元素周期表的结构,元素周,现有下列短周期元素性质的数据等内容,欢迎下载使用。
高中化学人教版 (新课标)必修2第二节 元素周期律第1课时课堂检测: 这是一份高中化学人教版 (新课标)必修2第二节 元素周期律第1课时课堂检测,共6页。试卷主要包含了核外电子的分层排布,电子的排布与元素性质的关系等内容,欢迎下载使用。
化学必修2第二节 来自石油和煤的两种基本化工原料第4课时课后测评: 这是一份化学必修2第二节 来自石油和煤的两种基本化工原料第4课时课后测评,共5页。试卷主要包含了原子,元素,元素周期表的结构,元素周,现有下列短周期元素性质的数据等内容,欢迎下载使用。