
粤教版九年级上册第四章 生命之源——水综合与测试课后测评
展开第四章《生命之源--水》单元测试卷
可能用到的相对原子质量:K:39 Cl:35.5 H-1 C-12 O-16
一、选择题(每题只有一个正确选项,每题2分,共40分)
1、水是宝贵的自然资源,下列净化水的方法中,净化程度最高的是( )
- 蒸馏 B. 沉淀 C. 过滤 D. 吸附
2、北京是极度缺水的城市之一,所以我们在生产、生活中不仅要节约用水,也要防止水被污染。下列做法正确的是 ( )
- 使用节水型洗衣机 B.使用含磷洗衣粉
C.任意施用农药、化肥 D.使用工业废水喷灌草地
3、下列措施能使硬水转化为软水的是( )
A.过滤 B.煮沸 C.静置沉淀 D.用活性炭吸附
4.蒸发时,不需要的仪器是( )
A.酒精灯 B.玻璃棒 C.铁架台[ D.烧杯
5、下列有关水的组成的说法中正确的是( )
A. 水是由氢气和氧气组成的纯净物 B. 水是由氢气和氧气组成的混合物
C. 水是由氢元素和氧元素组成的化合物 D. 水是由氢元素和氧元素组成的单质
6、 下列关于电解水实验的叙述正确的是( )
A.实验说明水是由氢分子和氧原子构成的
B.乙试管连接的是电源的正极。
C.甲试管内产生的气体能使带火星的木条复燃
D.甲、乙两试管产生的气体质量之比为1∶27.
7、下列叙述完全符合质量守恒定律的是 ( )
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水
D.1.2g碳与3.2 g氧气反应可生成4.4g二氧化碳
8、.根据化学方程式不能获得的信息是( )
A. 化学反应的快慢 B. 该反应中的反应物和生成物
C. 反应发生所需要的条件 D. 各反应物和生成物的质量比
9、电解水的过程中,反应物和生成物的量随时间的变化关系正确的是( )
A. B.
C. D.
10、在细菌作用下,可以用氨气处理含有甲醇(CH3OH)的工业废水,有关反应的化学方程式为5CH3OH+12O2+6NH3═3N2+5X+19H2O,则X的化学式为( )
A. NO B. CO2 C. H2 D. CO
11、目前有关部门做出决定,司机酒后驾车会受到严惩。交警常用一种“酒精检测仪”检查司机是否酒后驾车。其反应原理为C2H5OH+4CrO3+6H2SO4═2X+2CO2↑+9H2O,反应中红色的CrO3转变为绿色的化合物X,则X的化学式为( )
A. Cr2O3 B. CrSO3 C. Cr2(SO4)3 D. Cr2S3
12、一定质量的硫粉密闭容器中充分燃烧,下列图中能正确反映反应前后有关的量随时间变化关系的是( )
13、 现将20gA和足量B混合加热,A和B发生反应,20gA完全反应后生成16gC和9gD,则参加反应的A与B的质量比为 ( )
A.1:1 B.2:1 C.4:1 D.5:1
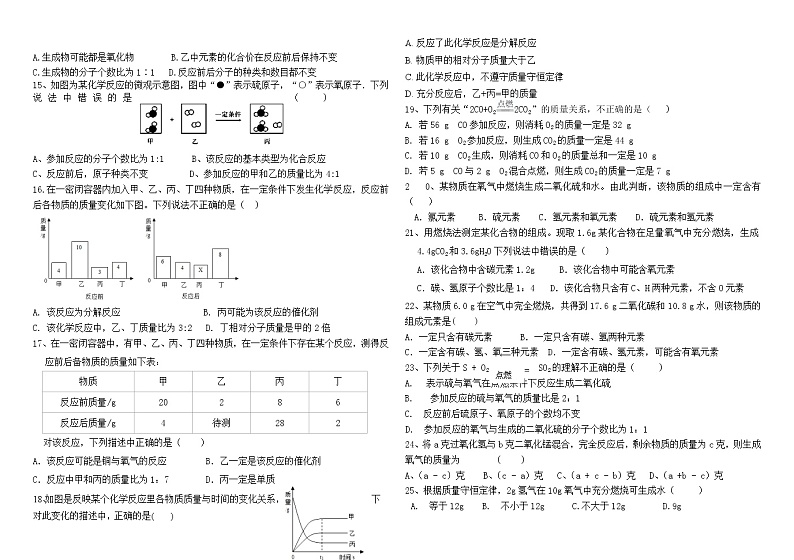
14、 下图为某反应的微观示意图,其中不同的球代表不同元素的原子,下列说法错误的是( )
A.生成物可能都是氧化物 B.乙中元素的化合价在反应前后保持不变
C.生成物的分子个数比为1∶1 D.反应前后分子的种类和数目都不变
15、如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子.下列说法中错误的是( )
A、参加反应的分子个数比为1:1 B、该反应的基本类型为化合反应
C、反应前后,原子种类不变 D、参加反应的甲和乙的质量比为4:1
16.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如下图。下列说法不正确的是( )
A. 该反应为分解反应 B. 丙可能为该反应的催化剂
C. 该化学反应中,乙、丁质量比为3:2 D. 丁相对分子质量是甲的2倍
17、在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后备物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 20 | 2 | 8 | 6 |
反应后质量/g | 4 | 待测 | 28 | 2 |
对该反应,下列描述中正确的是( )
A.该反应可能是铜与氧气的反应 B.乙一定是该反应的催化剂
C.反应中甲和丙的质量比为1:7 D.丙一定是单质
18、如图是反映某个化学反应里各物质质量与时间的变化关系,下对此变化的描述中,正确的是( )
A. 反应了此化学反应是分解反应
B. 物质甲的相对分子质量大于乙
C. 此化学反应中,不遵守质量守恒定律
D. 充分反应后,乙+丙=甲的质量
19、下列有关“2CO+O22CO2”的质量关系,不正确的是( )
A. 若56 g CO参加反应,则消耗O2的质量一定是32 g
B. 若16 g O2参加反应,则生成CO2的质量一定是44 g
C. 若10 g CO2生成,则消耗CO和O2的质量总和一定是10 g
D. 若5 g CO与2 g O2混合点燃,则生成CO2的质量一定是7 g
20、某物质在氧气中燃烧生成二氧化硫和水。由此判断,该物质的组成中一定含有( )
A.氯元素 B.硫元素 C.氢元素和氧元素 D.硫元素和氢元素
21、用燃烧法测定某化合物的组成。现取1.6g某化合物在足量氧气中充分燃烧,生成4.4gCO2和3.6gH2O下列说法中错误的是( )
A.该化合物中含碳元素1.2g B.该化合物中可能含氧元素
C.碳、氢原子个数比是1:4 D.该化合物只含有C、H两种元素,不含O元素
22、某物质6.0 g在空气中完全燃烧,共得到17.6 g二氧化碳和 10.8 g水,则该物质的组成元素是( )
A.一定只含有碳元素 B.一定只含有碳、氢两种元素
C.一定含有碳、氢、氧三种元素 D.一定含有碳、氢元素,可能含有氧元素
23、下列关于S + O2 =========== SO2的理解不正确的是( )
- 表示硫与氧气在点燃条件下反应生成二氧化硫
- 参加反应的硫与氧气的质量比是2:1
C. 反应前后硫原子、氧原子的个数均不变
D. 参加反应的氧气与生成的二氧化硫的分子个数比为1:1
24、将a克过氧化氢与b克二氧化锰混合,完全反应后,剩余物质的质量为c克,则生成氧气的质量为 ( )
A、(a - c)克 B、(c - a)克 C、(a + c - b)克 D、(a +b - c)克
25、根据质量守恒定律,2g氢气在10g氧气中充分燃烧可生成水( )
A. 等于12g B. 不小于12g C.不大于12g D.9g
二、填空题(化学方程式2分,其余每空1分,共20分)
26.爱护环境,防止水污染,刻不容缓.为此,某中学探究性学习小组对某河的水质状况进行有关检测.
(1)检验河水是软水还是硬水可以用 ,如果是硬水,应该出现的现象
是 。
(2)除去水中难溶性固体杂质的操作是 .
(3)将河水进行净化后,为了检验是否是纯水,需要做水的蒸发实验,其中玻璃棒的做用是 。
27 写出下列反应的化学方程式并填空。
(1)实验室利用高锰酸钾制取氧气的方程式为
该反应属于 (填反应类型)。
(2)用镁粉制作照明弹,主要利用镁 ,
方程式为 ,该反应属于 (填反应类型)。
(3)铁丝在氧气中燃烧的化学方程式为 ,实验时的现象为 _。
28.2013年3月22日是“世界水日”,水与人类的生活和生产密切相关.
(1)保护水资源、珍爱水资源是每个公民应尽的责任和义务。下列做法有利于、保护水资源的是 (填序号)。
A.大量使用化肥、农药 B.生活污水直接排放
C.使用含磷洗衣粉 D.工业废水处理达标后排放
(2)在水蒸发的过程中,下列说法正确的是____________(填序号)。
A.水分子分解成氢原子和氧原子 B.水分子可以保持水的物理性质
C.水分子不断运动 D.水分子之间间隔不变
(3)如图4-2是简易净水装置,该净水装置能否将河水变成纯水 (填“能”或“不能”)。活性炭的作用是 。
图4-2 图4-3
(4)图4-3是某反应过程的微观示意图,“”与“”分别表示不同元素的原子。图中X处的粒子示意图为 ,参加反应的两种分子的个数比为 。
三、实验探究题(化学方程式2分,其余每空1分,共13分)
29、化学反应都遵守质量守恒定律,请根据质量守恒定律的相关知识完成下列问题:
(1)在化学反应前后,下列各项中①原子的数目,②分子的数目,③原子的种类④物质的组成⑤分子的种类,⑥物质的质量总和 ⑦元素的种类,肯定不会改变的是 ;肯定会改变的是 ;可能改变也可能不变的是 。
(2)应用质量守恒定律配平化学方程式:___C2H4+____O2 ====___CO2+____H2O
(3) 实验室常用图4-3所示实验验证质量守恒定律.四位同学设计了如图4的A、B、C、D四个实验,并按实验操作来验证质量守恒定律,实验中观察到 实验(填序号)前后天平依然保持平衡,某同学认为这两个实验都能验证质量守恒定律,你认为他的说法 (填“是”或“否”)正确;理由是
(4)而另两个实验天平不平衡,选其中一个实验说明天平不平衡的原因是
。
提示:C中发生反应的化学方程式为Fe + CuSO4=FeSO4+Cu
D中发生反应的化学方程式为Na2CO3 +2HCl=2NaCl + H2O + CO2↑
30、右图为电解水的实验装置图,接通电源观察到两电极都有气泡产生。
(1)通电一段时间后,玻璃管a收集到的气体是________,
b、a两玻璃管收集的气体体积比约为________。质量比为
(2)下图为水分解过程的微观示意图:
①水分子的分解过程中,不发生变化的微粒是__________。
②结合实验现象,写出水通电分解的化学方程式:_________________________。
31、为了研究质量守恒定律,设计了下图“白磷燃烧前后质量测定”的实验,(装置气密性良好)请分析有关问题:
(1)装置:锥形瓶的底部铺有一层细沙,其作用是________ .
(2)燃烧前称量,锥形瓶的总质量为27.6g,则右图托盘天平中游码的读数为________ g.
(3)白磷燃烧:白磷燃烧过程中看到的现象是________ .
(4)燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是 ________
(5)反思:白磷燃烧________ (填“遵守”或“不遵守”)质量守恒定律,理由是 ________ .
四、计算题
32.氯酸钾和二氧化锰的混合物6.40g,充分加热后,剩下固体4.48g. 求
⑴根据质量守恒定律,可制得氧气 g;
⑵原混合物中二氧化锰的质量是多少?
粤教版九年级上册第一章 大家都来学化学综合与测试测试题: 这是一份粤教版九年级上册第一章 大家都来学化学综合与测试测试题,共3页。试卷主要包含了选择题等内容,欢迎下载使用。
初中粤教版第三章 维持生命之气——氧气综合与测试课时练习: 这是一份初中粤教版第三章 维持生命之气——氧气综合与测试课时练习,共5页。
化学九年级下册第七章 溶液综合与测试同步测试题: 这是一份化学九年级下册第七章 溶液综合与测试同步测试题,共5页。试卷主要包含了选择题,填空题,综合题等内容,欢迎下载使用。













