



初中化学人教版九年级上册第二单元 我们周围的空气课题1 空气多媒体教学课件ppt
展开
这是一份初中化学人教版九年级上册第二单元 我们周围的空气课题1 空气多媒体教学课件ppt,共34页。PPT课件主要包含了学习目标,知识与技能,第一课时,学习重点,不带电,数目相等电性相反,P53表格,答不一定,原子结构示意图,原子核等内容,欢迎下载使用。
1.了解原子是由质子、中子和电子构成的。2.知道原子核外电子是分层排布的。3.进行世界的物质性、物质的可分性的辩证唯物主义观点教育。
1.原子的构成。2.原子核外电子的排布。
1964年10月16日我国成功爆炸第一颗原子弹。原子弹爆炸的威力非常惊人。
为什么原子弹爆炸会产生如此巨大的能量呢?我们这节课一起来学习原子结构的奥秘。
知识点1 原子的构成
原子是化学变化中的最小粒子。
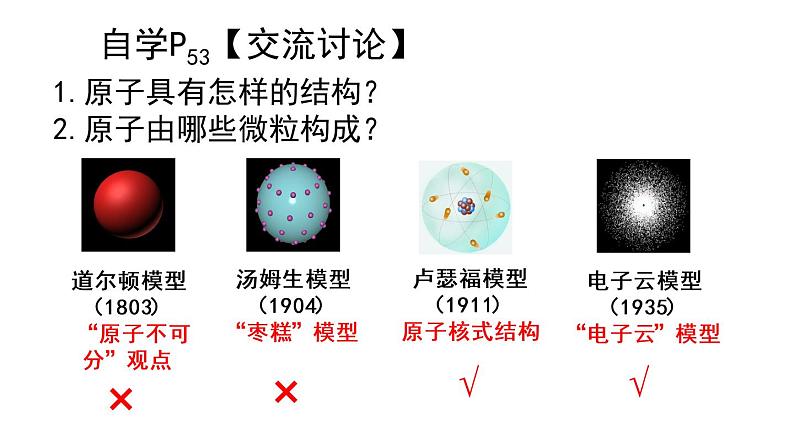
自学P53【交流讨论】
1.原子具有怎样的结构?2.原子由哪些微粒构成?
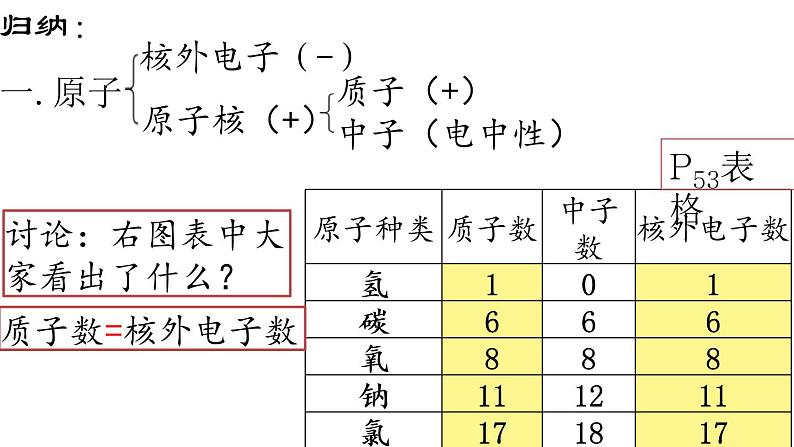
讨论:右图表中大家看出了什么?
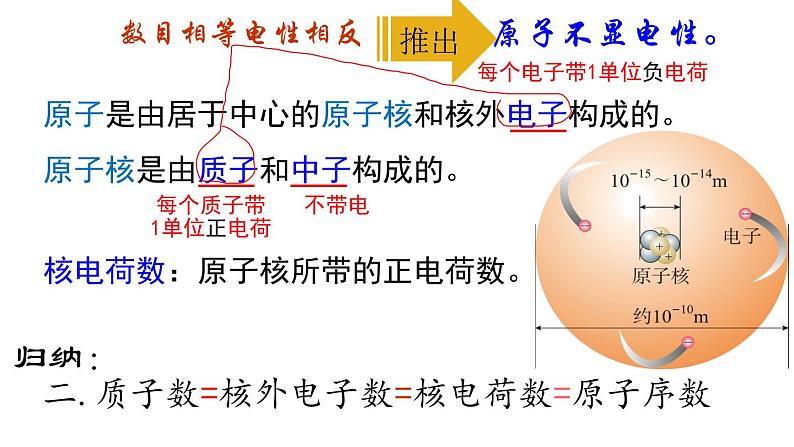
原子是由居于中心的原子核和核外电子构成的。原子核是由质子和中子构成的。
每个电子带1单位负电荷
每个质子带1单位正电荷
核电荷数:原子核所带的正电荷数。
二.质子数=核外电子数=核电荷数=原子序数
【小组讨论】1.是不是所有的原子核都是由质子和中子构成的?
答:不是,在氢原子核中只有质子,没有中子。
2.在原子中,质子数一定等于电子数吗?
答:在原子中,质子数一定等于电子数
3.在原子中,质子数一定等于中子数吗?
例 下列关于原子结构的叙述正确的是( )A.一切原子的原子核都由质子和中子构成B.在原子中,核电荷数一定等于质子数或核外电子数C.原子核内质子数一定等于中子数D.原子是不能再分的粒子
知识点2 原子核外电子的排布特点
与原子相比,原子核的体积更小。
1.核外电子的排布特点
普通氢原子核外只有一个电子,这一电子围绕氢的原子核在核外的“巨大”空间里高速运动。
在具有多个电子的原子中,电子是如何运动的呢?他们会不会相撞而产生巨大能量?
核外电子的运动有自己的特点,它不像行星绕太阳旋转有固定的轨道,但却有经常出现的区域。科学家把这些区域称为电子层。核外电子是在不同的电子层内运动的,人们又把这种现象叫做核外电子的分层排布。
【归纳】核外电子排布规律: 三. 每层最多2n2个核外电子排布 次外层最多18个 最外层最多8个(氦He2个) (每层排满为稳定结构)
用原子结构示意图可以简明、方便地表示核外电子的分层排布。
分别代表第一层、第二层电子层
代表各层电子数,且2+6=8
练习:画出下列原子的结构示意图(每层排满为稳定结构)
原子序数 11 17 18 19 20 元素 Na Cl Ar K Ca
1.了解离子的形成,初步认识离子是构成物质的一种粒子,及化学性质与最外层电子数的关系。 2.初步了解相对原子质量的概念,并会查相对原子质量表。 3.了解原子结构示意图的含义及原子最外层电子数与元素性质的关系。
1.离子的形成过程。2.相对原子质量的意义。
我们已经知道,原子是由原子核和核外电子构成的。原子核的体积仅占原子体积的几千亿分之一,相对来讲,原子核外空间很大,电子在这个空间里作高速运动。 那么,物质中电子是怎样存在的呢?氯化镁的化学式为MgCl2,为什么不写成MgCl3?这就是这节课研究的重点
物质有趋于稳定状态的特点,原子也不例外,有趋于稳定结构的特点。 稳定结构:像稀有气体元素原子这样的结构叫8电子稳定结构。(若只有一个电子层,则2电子是稳定结构)
知识点1 离子的形成
练习:画出Cl Mg 的原子结构示意图
【归纳】根据P54原子结构示意图自学P55上四.元素化学性质与最外层电子数关系密切
1.金属元素最外层电子数
相关课件
这是一份初中化学北京课改版九年级上册第3章 构成物质的微粒第二节 原子核外电子的排布 离子授课课件ppt,共15页。PPT课件主要包含了导入新课,学习目标,讲授新课,原子结构示意图,原子核,核电核数,电子层,该电子层上电子数,个He为2个,比较稳定等内容,欢迎下载使用。
这是一份2021学年第二节 原子核外电子的排布 离子教课内容ppt课件,共20页。PPT课件主要包含了原子核外电子排布图,补充讨论,能力提高,原子和离子的比较,阳离子,原子简化结构示意图,离子符号的意义,数字“2”的意义,例O2-,只表示3个氧离子等内容,欢迎下载使用。
这是一份人教版九年级上册课题2 原子的结构说课课件ppt,共19页。PPT课件主要包含了一个单位正电荷,一个单位负电荷,难得失,易失去,不稳定,易得到,ABD,原子中子,改变了原来的,运动方向等内容,欢迎下载使用。










