

【化学】辽宁师大附中2018-2019学年高二下学期期末考试
展开辽宁师大附中2018-2019学年高二下学期期末考试
考试时间:90分钟 满分:100分
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 Mg-24 P-31 S-32
Cl-35.5 K-39 Fe-56 Cu-64
第Ⅰ卷(选择题50分)
一、选择题(本题包括20个小题,1-10每小题2分,11-20每小题3分,每小题只有一个选项符合题意)
1.《中国诗词大会》不仅弘扬了中国传统文化,还蕴含着许多化学知识,下列诗词分析不正确的是
A.诗句“煮豆燃豆萁,豆在釜中泣”,这里的能量变化主要是化学能转化为热能
B.诗句“千淘万漉虽辛苦,吹尽狂沙始到金”,金性质稳定可通过物理方法得到
C.诗句“爆竹声中一岁除,春风送暖入屠苏”,爆竹的燃放涉及氧化还原反应
D.诗句“日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华的现象
2.化学与生产生活、社会发展息息相关,下列说法不正确的是
A.“爆竹一声除旧岁”涉及到的焰色反应为物理变化
B.碘酒、“84”消毒液、75%的酒精、生理盐水都可用于消毒
C.铝及其合金具有广泛的应用,通常用电解氧化铝的方法制取铝
D.采取“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
3.下列有关说法不正确的是
A.明矾、高铁酸钾都是水处理剂,功能不完全相同
B.瓷坩埚不能熔融碱类物质,因为能发生化学反应
C.氯气、氨气易液化,均可用作制冷剂
D.SO2可以用来漂白纸浆、毛、丝、草帽辫等,还可以用于杀菌,消毒
4.下列关于物质应用和组成的说法正确的是
A.P2O5可用于干燥Cl2和NH3
B.“可燃冰”的主要成分是甲烷和水
C.硅胶干燥吸水过程发生了化学变化
D.Si和SiO2都用于制造光导纤维
5.下列反应的离子方程式书写正确的是:
A.氢氧化铁溶液与氢碘酸反应:Fe(OH)3+3H+ == Fe3+ + 3H2O
B.氨水中通入过量二氧化硫:2NH3·H2O + SO2 == 2NH+ SO+ H2O
C.将2mol/LAlCl3溶液和7mol/LNaOH溶液等体积混合:
2Al3++7OH- == Al(OH)3↓+ AlO+2H2O
D.次氯酸钙溶液中通入二氧化硫:Ca2++2ClO-+SO2+H2O CaSO3↓+2HClO
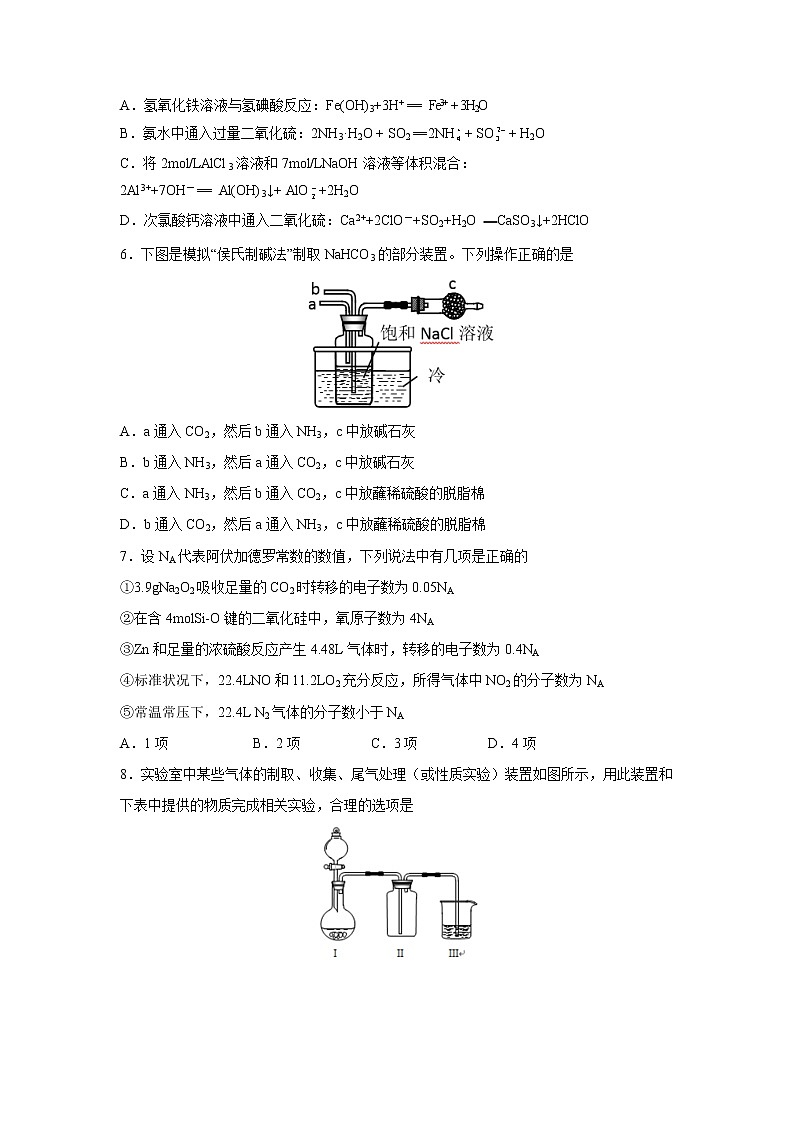
6.下图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是
A.a通入CO2,然后b通入NH3,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
7.设NA代表阿伏加德罗常数的数值,下列说法中有几项是正确的
①3.9gNa2O2吸收足量的CO2时转移的电子数为0.05NA
②在含4molSi-O键的二氧化硅中,氧原子数为4NA
③Zn和足量的浓硫酸反应产生4.48L气体时,转移的电子数为0.4NA
④标准状况下,22.4LNO和11.2LO2充分反应,所得气体中NO2的分子数为NA
⑤常温常压下,22.4L N2气体的分子数小于NA
A.1项 B.2项 C.3项 D.4项
8.实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和下表中提供的物质完成相关实验,合理的选项是
选项 | I中的物质 | II中收集的气体 | III中的物质 |
A. | Cu和稀硝酸 | NO | NaOH溶液 |
B. | 浓盐酸和MnO2 | Cl2 | NaOH溶液 |
C. | 亚硫酸钠和浓硫酸 | SO2 | 品红溶液 |
D. | 浓氨水和CaO | NH3 | 酚酞溶液 |
9.向含0.2mol NaOH和0.1mol Ca(OH)2的混合溶液中持续稳定地通入CO2气体,当通入气体为6.72L(标况)时立即停止,则这一过程中,溶液中离子物质的量和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计)
A. B. C. D.
10.固体NH5属于离子晶体。它与水反应的化学方程式为:NH5+H2O→NH3·H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气。下列有关NH5叙述正确的是
A.与水反应时,水作氧化剂
B.NH5中N元素的化合价为+5价
C.1molNH5中含有5NA个N—H键
D.与乙醇反应时,NH5被还原
11.下列叙述I和II均正确并有因果关系的是
选项 | 叙述I | 叙述II |
A. | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
B. | BaSO4难溶于酸 | 用盐酸和BaCl2溶液检验SO42- |
C. | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
D. | Ca(OH)2能制成澄清石灰水 | 可配制2.0 mol∙L-1的Ca(OH)2溶液 |
12.下列装置能达到相应实验目的的是
甲 乙 丙 丁
A.甲制取干燥的 NH3
B.乙用来蒸干MgCl2饱和溶液制备MgCl2·6H2O晶体
C.丙收集NO2并防止其污染环境
D.丁验证浓硫酸具有强氧化性
13.海水资源开发利用的部分过程如下图所示(苦卤中主要含K+、Mg2+、Br-等)。下列说法不正确的是
A.通过蒸馏法将海水转化为可饮用水,但该法成本很高
B.向苦卤中通入Cl2时溴离子被还原为Br2
C.Br2+SO2+2H2O=2Br-+4H++SO 可用于溴的富集
D.工业选用的沉淀剂通常经煅烧碳酸钙获得而不是电解食盐水
14.白磷(正四面体结构)与过量氢氧化钾在一定条件下可以发生反应:P4+3KOH+3H2O = PH3 ↑+3KH2PO2。若用NA表示阿伏加德罗常数的值。下列说法不正确的是
A.31g白磷所含分子的数目为0.25 NA
B.28 g KOH 参加反应转移的电子数为 0.5 NA
C.KH2PO2为正盐,且0.1 mol该固体物质中含离子数目为0.2 NA
D.10 mL pH = 11的 KOH溶液稀释100倍,水电离的OH-的数目约为10-5 NA
15.雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl- 。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如下的实验:
已知:3NO3-+ 8Al + 5OH- + 2H2O3NH3↑+ 8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是
A.试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B.试样中一定不含Al3+
C.试样中可能存在Na+、Cl-
D.该雾霾中可能存在NaNO3 、NH4Cl和MgSO4
16.将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,能证明SO2与FeCl3溶液发生氧化还原反应的是
| 操作 | 现象 |
A. | 加入NaOH溶液 | 有红褐色沉淀 |
B. | 加入Ba (NO3)2溶液 | 有白色沉淀 |
C. | 加入酸性KMnO4溶液 | 紫色褪去 |
D. | 加入K3[Fe(CN)6](铁氰化钾)溶液 | 有蓝色沉淀 |
17.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列物质参与反应的先后顺序正确的是
A.含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
B.含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+、Fe2+
C.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:OH-、AlO2-、CO32-
D.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
18.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时得到2.54g沉淀,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2︰1
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C.NO2和N2O4 的混合气体中,NO2 的体积分数是80%
D.得到2.54沉淀时,加入NaOH溶液的体积是600mL
19.有4.8gCuO、Fe2O3混合物跟足量CO充分反应后固体减少1.28g,反应后全部气体用0.6mol/LBa(OH)2溶液100mL吸收。下列有关叙述中正确的是
A.原混合物中CuO与Fe2O3物质的量的比为l:2
B.原混合物中CuO与Fe2O3质量比为2:1
C.吸收CO2后溶液中一定有Ba(HCO3)2
D.反应中生成的CO2体积为1.792L
20.在15 g铁和氧化铁混合物中,加入稀硫酸150 mL,能放出H2 1.68 L(标准状况)。同时铁和氧化铁均无剩余,向反应后的溶液中滴入KSCN溶液,未见颜色变化。为了中和过量的H2SO4,且使Fe2+完全转化成Fe(OH)2,共消耗3 mol·L-1的NaOH溶液200 mL,则原硫酸的物质的量浓度是
A.1.5 mol·L-1 B.2 mol·L-1 C.2.5 mol·L-1 D.3 mol·L-1
第II卷(非选择题50分)
21.(12分)硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革的还原剂,它受热、遇酸易分解。工业上可用反应:2Na2S + Na2CO3 + 4SO2 == 3Na2S2O3 + CO2 制得,实验室模拟该工业过程的装置如图所示,
回答下列问题:
(1)b中反应的离子方程式为_______________________________,c中试剂为__________。
(2)反应开始后,c中先有浑浊产生,后又变为澄清,此浑浊物是___________________。
(3)d中的试剂为__________________。
(4)实验中要控制SO2生成速率,可采取的措施有___________、___________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入SO2不能过量,原因是___________________。
22.(12分)镁的化合物在化工生产和药物合成上有重要用途。某兴趣小组以一种工业废渣(主要成分为MgCO3、MgSiO3和少量Fe的氧化物)为原料制备MgCO3·3H2O。实验过程如下:
(1)滤渣的成分为 (填化学式),酸溶也可用盐酸来代替,用盐酸溶解时温度不能过高的原因是: 。
(2)加入H2O2一段时间后,溶液中有气泡出现并放热,分析产生气泡的原因:
(用文字解释)。
(3)萃取分液的目的是 (填字母)。
A.除去水溶液中的铁离子 B.增加镁离子在水中的溶解度 C.富集铁元素,可回收利用
(4)萃取后得到的水溶液制备MgCO3·3H2O的实验操作:边搅拌边向溶液中滴加Na2CO3溶液至有大量沉淀生成,静置后,进行操作: ,确定沉淀完全后,再通过过滤、洗涤、 得到MgCO3·3H2O。
(5)若工业废渣起始投料500kg,最终得到产品MgCO3·3H2O为276kg,过滤得到滤渣后灼烧并称重为60kg。废渣中的碳酸镁的质量分数为 %。(保留1位小数)
23.(13分)水合肼(N2H4·H2O)又名水合联氨,无色透明,是具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl。
实验一:制备NaClO溶液。(实验装置如图1所示)
(1)实验室可以用高锰酸钾固体和浓盐酸混合制取氯气,写出反应的离子方程式 ,为提高NaClO溶液的浓度,生成的氯气需净化后通入锥形瓶,净化时所需的试剂是 。
实验二:制取水合肼。(实验装置如图2所示)
(2)①仪器B的名称为 。
②反应过程中需控制反应温度,同时将长颈漏斗中溶液缓慢加入A中,如果加入过快则会导致产品产率降低,同时产生大量氮气,写出该过程的化学方程式: ,故加入长颈漏斗中的溶液可能是 。 (填字母)。
A.CO(NH2)2溶液 B.NaOH和NaClO溶液
③充分反应后,加热蒸馏A内的溶液,收集108~114℃馏分,即可得到水合肼的粗产品。
(3)联氨(肼)为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______________(已知:N2H4+H+N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为______________。
24.(13分)叠氮化钠(NaN3)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原
理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220 ℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为____________,装置C的主要作用是______________________。
(2)步骤①中先加热通氨气的目的是_____________________________________,步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为_______________________________,步骤③中最适宜的加热方式为 ___________(填“水浴加热”,“油浴加热”)。
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)___________。
(4)生成NaN3的化学方程式为_________________________________________________。
(5)步骤④中用乙醚洗涤的主要目的是__________________________________________。
参考答案
1-5: DBCBC 6-10: CBCAA
11-15: BABDB 16-20: DCDCB
21.(12分)
(1)SO32-+2H+=SO2↑+H2O或HSO3-+H+=SO2↑+H2O (2分)
硫化钠和碳酸钠混合溶液 (2分)(少溶液二字不给分)
(2)硫 (2分)(写元素符号S给分)
(3)NaOH溶液 (2分)(少溶液二字不给分)
(4)控制反应温度、调节酸的滴加速度(或调节酸浓度)(2分)(每个1分,合理即给分)
(5)若SO2过量,溶液显酸性,产物分解 (2分)(表达意思正确即给分)
22.(12分)
(1)H2SiO3(1分) 温度过高,盐酸挥发(1分)
(2)Fe3+催化H2O2分解(2分)
(3) AC(2分)(错选不给分,少选给一分)
(4)取少许上层清液,滴加Na2CO3溶液,若没有白色沉淀生成(2分)(表达合理给分,但要规范表达,语言逻辑不通不给分) 低温干燥(2分)(少低温二字不给分)
(5)16.8 (2分)
23.(13分)
(1)2MnO4-+16H++10Cl-=Mn2++5Cl2↑+8H2O(2分) (化学方程式不给分)
饱和食盐水(2分)(错别字不给分,比如饱合;只答食盐水不给分)
(2)①直形冷凝管(1分)(错别字直型不给分;只答冷凝管不给分)
②CO(NH2)2 + 2NaOH + 3NaClO = N2↑+Na2CO3 + 3NaCl + 3H2O
或N2H4·H2O + 2NaClO = N2↑+2NaCl + 3H2O
或N2H4+ 2NaClO = N2↑+2NaCl + 2H2O(2分)
B(2分)
(3)8.7×10-7 (2分) N2H6(HSO4)2(2分)
24.(13 分)
(1)碱石灰(或氢氧化钠固体)(1 分) 冷凝分离出水(2分)
(2)排尽装置中的空气(1 分) 2Na+2NH3 2NaNH2+H2(2分)(少反应条件得1分)
油浴加热(1 分)
(3)I、IV(2 分)(错选不给分,少选给一分)
(4)NaNH2+N2O NaN3+H2O(2 分)(少反应条件得1分)
(5)减少产品NaN3溶解损失,乙醚易挥发利于产品快速干燥(2分)(减少溶解损失1分,快速干燥1分,答案意思正确给分)








