

【化学】广东省汕头市金山中学2018-2019学年高一下学期第一次月考试题
展开广东省汕头市金山中学2018-2019学年高一下学期第一次月考试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cl-35.5 S-32 Fe-56 Cu-64 Zn-65
一.单选题(本题包括15小题,每小题3分,共45分。)
1.化学与科学、技术、社会、环境密切相关,下列说法正确的个数是( )
①PM2.5(指直径小于或等于2.5×10-6 m的细小颗粒)在空气中一定能形成气溶胶
②碘酸钾具有较强的氧化性,在食盐中加入适量碘酸钾,可抗人体氧化
③二氧化硫具有氧化性,可以用于漂白纸浆
④ “光化学烟雾”、“硝酸酸雨”的形成都与氮氧化物有关
⑤双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境没有污染
⑥王水是浓盐酸和浓硝酸按体积比1︰3配成的混合物,可以溶解Au、Pt
⑦酸雨是指pH﹤7的雨水
A.1个 B.3个 C.5个 D.7个
2.二氧化硫体现还原性的反应是( )
A.SO2+Na2CO3=Na2SO3+CO2 B.SO2+2H2S=2H2O+3S↓
C.SO2+2NaOH=Na2SO3+H2O D.SO2+2H2O+Cl2=H2SO4+2HCl
3.13C−NMR(核磁共振)、15N−NMR可用于测定蛋白质、核酸等生物大分子的空间结构,这项研究曾获诺贝尔化学奖。下面有关叙述正确的是( )
A.15N的核外电子数比中子数少1 B.14N与14C互为同位素
C.15N 与14N 为同一种核素 D.13C与15N有相同的中子数
4.下列反应中,调节反应物用量或浓度,不会改变反应产物的是( )
A.硫酸中加入锌粉 B.二氧化硫通入澄清石灰水
C.HNO3与Cu反应 D.铁在硫蒸气中燃烧
5.下列反应的离子方程式正确的是( )
A.氨水中通入少量的SO2气体: SO2+ OH- == HSO3-
B.氯气与水的反应: Cl2+H2O2H++Cl-+ClO-
C.氯化钙溶液中通入CO2气体: Ca2++H2O+CO2== CaCO3↓+2H+
D.二氧化锰跟浓盐酸共热制Cl2:MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
6.下列溶液中,所给离子一定能大量共存的是( )
A.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-
B.使酚酞变红的溶液:Na+、Ca2+、SO42-、CO32-
C.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl-
D.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
7.用NA表示阿伏伽德罗常数值,下列叙述中正确的是( )
A.5.6g铁在足量的O2中燃烧,转移的电子数为0.3NA
B.18g H218O和D2O的混合物中,所含中子数为9NA
C.1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2 NA
D.0.4 mol NH3与0.6 mol O2在催化剂的作用下充分反应,得到NO的分子数为0.4NA
8.以下物质间的转化通过一步反应都能实现的是( )
A.Si→SiO2→H2SiO3→Na2SiO3
B.HCl→Cl2→HClO→NaClO
C. S→SO3→H2SO4→Al2(SO4)3
D. NH3→NO2→HNO3→NaNO3
9.在一定条件下,氯气与碘单质以等物质的量进行反应,可得到一种红棕色液体ICl,ICl有很强的氧化性,ICl跟Zn、H2O反应的化学方程式如下: 2IC1+2Zn=ZnCl2+ZnI2,IC1+H2O=HC1+HIO,下列关于ICl性质的叙述正确的是( )
A.ZnCl2是氧化产物,又是还原产物
B.ZnI2既是氧化产物,又是还原产物
C.ICl跟H2O的反应,ICl是氧化剂,H2O是还原剂
D.反应6.5gZn,转移电子0.1mol
10.喷泉是一种常见的自然现象,如左下图是化学教材中常用的喷泉实验装置,在烧瓶中充满干燥气体,而胶头滴管及烧杯中分别盛有液体。下列气体和液体的组合中不可能形成喷泉的是( )
A.HCl和H2O B.CO2和NaOH溶液 C.NH3和H2O D.O2和H2O
11.如图表示第ⅠA族金属(即碱金属)的某些性质与核电荷数的变化关系,则下列各性质中不符合图示关系的是( )
A.金属性 B.与水反应的剧烈程度 C.阳离子的氧化性 D.原子半径
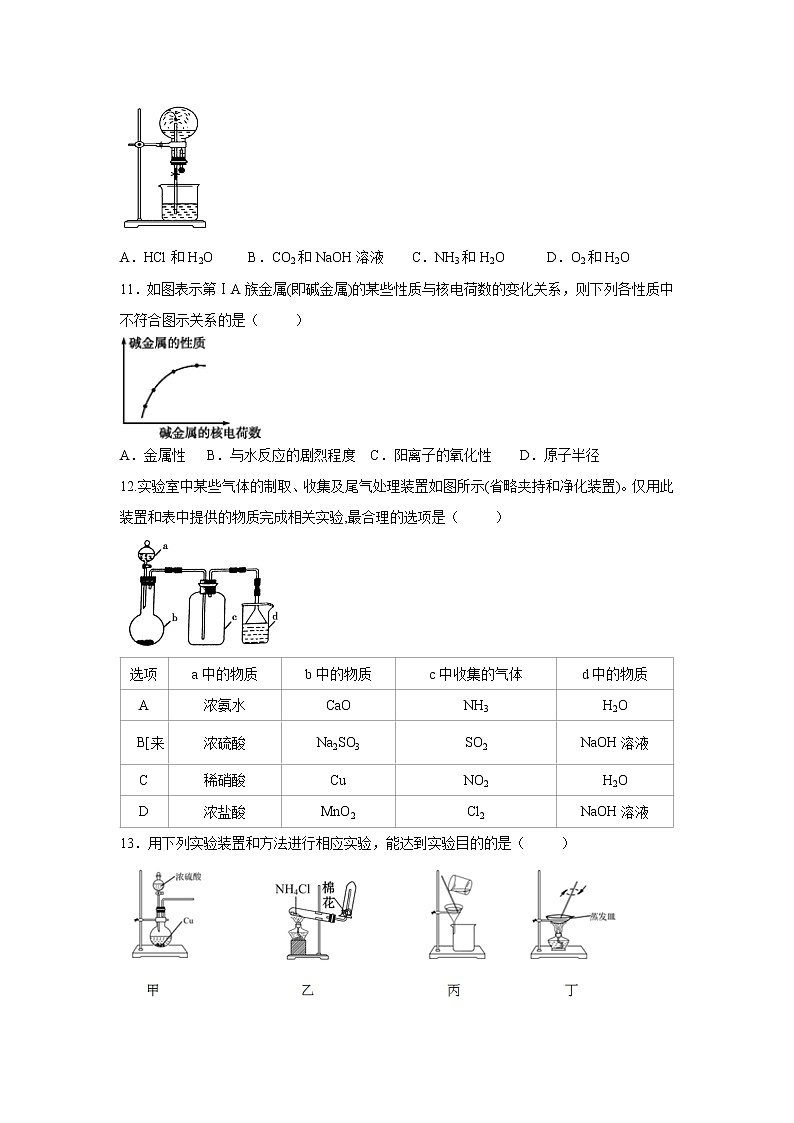
12.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B[来 | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
13.用下列实验装置和方法进行相应实验,能达到实验目的的是( )
A.用装置甲制备SO2
B.用装置乙制备氨气
C.用装置丙除去粗盐溶液中混有的沙子
D.用装置丁蒸干溶液获得(NH4)2CO3晶体
14.已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是( )
A.甲是浓氨水,乙是浓硫酸
B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸
D.甲是浓硫酸,乙是浓氨水
15.1.92g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积可能是( )
A.504mL B.168mL C.224mL D.336mL
二.非选择题(本题共3道题,共55分。)
16. (本题15分,每道3分)按要求完成下列方程式
(1)磁性氧化铁与足量的稀硝酸反应的离子方程式:____________________________
(2)铜与硫共热的化学方程式:___________________________________________
(3)二氧化氮通入水中的化学方程式:________________________
(4)氨的催化氧化的化学方程式:__________________________________________
(5)往Ba(OH)2溶液中滴加NaHSO4溶液使溶液呈中性的离子方程式:______________________
17.(本题20分,每空2分)氮家族化合物繁多,某校研究性学习小组对其进行研究。
研究1:选用下图装置组装制备纯净干燥的NH3并探究NH3与CuO发生的反应,同时检验和收集非固态产物(提示:每个装置只使用一次)。请回答下列问题:
(1)完成实验所需装置按气流方向从左到右的连接顺序为A-( )-( )-( )-G-B-( )
(2)装置A中发生反应的化学方程式为__________________________________。
(3)D中盛放碱石灰的仪器名称是________________,E装置的作用是___________________。
(4)通过进一步检测发现F中收集到的气体是一种常见的单质气体,硬质玻璃管中得到一种固体单质。试描述该小组同学还能观察到的其它现象为:①C中___________________________;
②E中 ;C中反应的化学方程式为:__________________________________
研究2:将32g铜与150mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L,请回答:
(5)在标况下,NO的体积为______L,NO2的体积为______L。
(6)若将产生的气体全部释放后,向溶液中加入VmLamol•L﹣1的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为____mol•L﹣1。(用含a和V的式子表示)
18.(本题20分,每空2分)土法酿造葡萄酒(只加糖的纯天然酿酒法)容易出问题,有报道说,喝了自制葡萄酒差点失明。主要原因是发酵过程产生的菌种多达百种,难以控制,而产生对神经有毒的甲醇等物质。科学酿酒加SO2等辅料,我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。
(1)葡萄酒中添加SO2的作用可能是________。A.氧化细菌 B.抗氧化 C.漂白 D.增酸作用
I.实验方案一
利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或H2SO3。设计如图1的实验:
图2
(2)甲同学得出的实验结论是干白葡萄酒中不含SO2或H2SO3。这个结论________(填“成立”或“不成立”),理由是
Ⅱ.实验方案二
(3) 用图2(右上图)实验装置探究二氧化硫的氧化性。
充入气体前的操作为 ,关闭旋塞1和2;按图2充入气体,连接装置。打开旋塞1,可观察到的主要现象是 ;若A瓶和B瓶的体积相等,恢复到常温,打开旋塞2,可观察到的现象是 ,此时A瓶中可能发生反应的化学方程式为 。
(4)从环保角度,利用图2装置设计探究二氧化硫既有氧化性又有还原性的最佳方案。
实验方案 | 预期现象 |
将烧杯中的氢氧化钠溶液换成 溶液 (填化学式), 操作如(3) | 说明SO2具有还原性的现象为 对应的离子方程式为: |
【参考答案】
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
答案 | A | D | A | D | D | C | B | B |
题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
|
答案 | B | D | C | B | C | C | D |
|
16、(本题15分)
(1)3Fe3O4+28H++NO3-=9Fe3++14H2O+NO↑(2)2Cu+SCu2S
(3)3NO2+ H2O =2HNO3+NO
(4)4NH3+5O24NO+6H2O
(5)2H++2OH-+SO42+Ba2+===BaSO4↓+2H2O
17、(本题20分,每空2分)
(1)DCEF
(2)2NH4C1+Ca(OH)2 CaCl2+2H2O+ 2NH3↑
(3)球形干燥管检验NH3 与CuO反应的产物中是否有水生成
(4)①C中黑色固体逐渐变红,试管壁上有液珠产生;②E中白色固体逐渐变蓝;2NH3+3CuO3Cu+3H2O+ N2
(5)5.6;5.6;
(6)(aV×10-3+0.5)/0.15(其他合理答案也可)
18、(本题20分,每空2分)
(1)BD
(2)不成立,实验对比说明浓度低的亚硫酸不能使品红褪色,葡萄酒中的SO2含量很低,所以也不能使品红褪色
(3)检査装置气密性;B瓶内壁有黄色固体和小水珠生成;
NaOH溶液倒吸到A瓶、B瓶中;SO2+NaOH NaHSO3或SO2+2NaOH Na2SO3+H2O
(4)KMnO4 ;A瓶中酸性KMnO4溶液褪色; 2MnO4-+5SO2+2H2O ===2Mn2++5SO42-+4H+
(也可以换成Br2,A瓶中溴水褪色;Br2+SO2+2H2O ===2Br-+SO42-+4H+)








