

【化学】江苏省东台市2019-2020学年高一上学期期中考试试题
展开江苏省东台市2019-2020学年高一上学期期中考试试题
可能用到的相对原子质量:H 1 He 4 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Zn 65
一、单项选择题:本题共15小题,每小题2分,共30分.每小题只有一个选项符合题意.
1.2019年新学期初,市教育局在全市中小学开展了“节约用水用电,倡导绿色简约生活”的活动。下列做法不应该提倡的是( )
A.路远的同学可乘公交车上学 B.作业不要使用修正带或涂改液
C.将化学实验室的废水直接排入水池 D.养成随手关水关灯的习惯
2.碳酸钠俗称苏打或纯碱,它属于( )
A.酸 B.碱 C.氧化物 D.盐
3.胶体区别于其它分散系的本质特征是( )
A.胶体分散质粒子直径介于1nm~100nm之间 B.胶体能产生丁达尔现象
C.胶体是一种澄清透明的分散系 D.胶体可用于净水
4.2017年9月3日朝鲜又进行了核试验,引起国际社会的极大关注。235 92U是一种重要的核燃料,这里的“235”是指该原子的( )
A.质子数 B.电子数 C.质量数 D. 中子数
5.下列物质属于电解质的是( )
A.食盐水 B.Cu C.NaOH固体 D.葡萄糖
6.下列过程属于物理变化的是( )
A.蜡烛燃烧 B.漂白粉消毒 C.食物腐败 D.干冰升华
7.关于容量瓶的使用,下列说法中错误的是( )
A.容量瓶不能用于溶解固体
B.容量瓶不能用于加热
C.容量瓶可以用来长期存放溶液
D.容量瓶可以用于配制溶液
8.NA表示阿伏加德罗常数,其近似值为6.02×1023mol-1,则下列叙述正确的是 ( )
A.1mol H2SO4的质量为98g•mol﹣1
B.3.01×1023个CO2分子的物质的量为0.5mol
C.NaCl的摩尔质量为58.5g
D.标准状况下,1mol任何物质体积均为22.4L
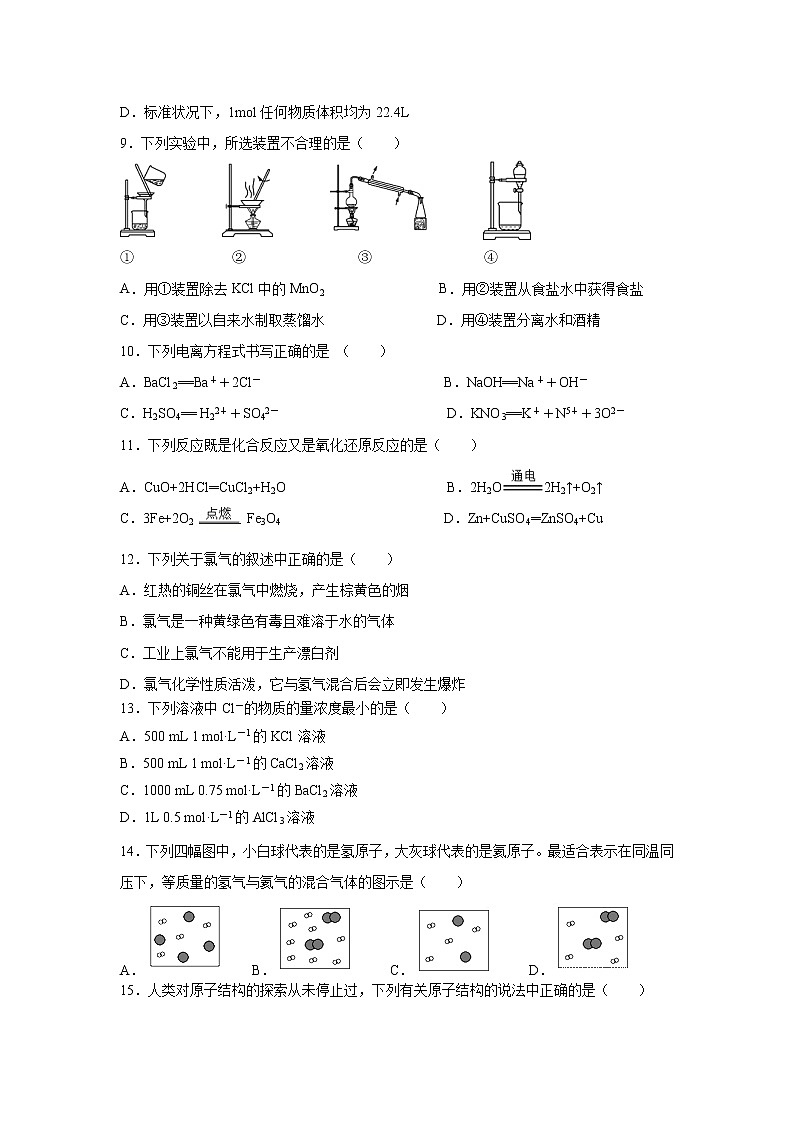
9.下列实验中,所选装置不合理的是( )
① ② ③ ④
A.用①装置除去KCl中的MnO2 B.用②装置从食盐水中获得食盐
C.用③装置以自来水制取蒸馏水 D.用④装置分离水和酒精
10.下列电离方程式书写正确的是 ( )
A.BaCl2==Ba++2Cl- B.NaOH==Na++OH-
C.H2SO4== H22++SO42- D.KNO3==K++N5++3O2-
11.下列反应既是化合反应又是氧化还原反应的是( )
A.CuO+2HCl═CuCl2+H2O B.2H2O2H2↑+O2↑
C.3Fe+2O2 Fe3O4 D.Zn+CuSO4═ZnSO4+Cu
12.下列关于氯气的叙述中正确的是( )
A.红热的铜丝在氯气中燃烧,产生棕黄色的烟
B.氯气是一种黄绿色有毒且难溶于水的气体
C.工业上氯气不能用于生产漂白剂
D.氯气化学性质活泼,它与氢气混合后会立即发生爆炸
13.下列溶液中Cl-的物质的量浓度最小的是( )
A.500 mL 1 mol·L-1的KCl溶液
B.500 mL 1 mol·L-1的CaCl2溶液
C.1000 mL 0.75 mol·L-1的BaCl2溶液
D.1L 0.5 mol·L-1的AlCl3溶液
14.下列四幅图中,小白球代表的是氢原子,大灰球代表的是氦原子。最适合表示在同温同压下,等质量的氢气与氦气的混合气体的图示是( )
A. B. C. D.
15.人类对原子结构的探索从未停止过,下列有关原子结构的说法中正确的是( )
A.所有的原子都含有质子、中子和电子
B.科学家汤姆生首先发现了电子并提出了“葡萄干面包式”的原子结构模型
C.在化学反应过程中,原子核和原子的最外层电子数都一定会发生变化
D.电子在原子核外一定不是分层排布的
二、不定项选择题:本题共5小题,每小题4分,共20分.每小题有一到两个选项符合题意.全部选对的得4分,选对但不全的得2分,错选或不答的得0分.
16.对于某些离子的检验及结论正确的是( )
A.用铂丝蘸取某溶液在酒精灯火焰上灼烧,火焰呈黄色,说明原溶液中一定不含K+
B.加入氯化钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,说明该溶液中一定含有SO42-
C.加入稀盐酸产生无色气体,再将气体通入澄清石灰水中,溶液变浑浊,则该溶液中可能含有CO32-
D.向待测液中加入较浓的氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,说明该待测液中一定含有NH4+
17.以下物质间的转化不能通过一步反应实现的是( )
A.MgSO4→Mg(OH)2 B.Cu→Cu(OH)2
C.CO2→CaCO3 D.Cl2→NaCl
18.氮化铝(AlN)是一种耐高温、抗冲击、导电性好的优良工业材料。现通过反应:
Al2O3+3C+N22AlN+3CO来制取,下列有关该反应的说法中正确的是( )
A.Al2O3中Al元素化合价没有发生变化 B.N2是氧化剂
C.CO作还原剂 D.反应物C发生还原反应
19.某校化学兴趣小组在探究新制饱和氯水成分的实验中,根据实验现象推测的有关结论中错误的是( )
A.向氯水中滴入紫色石蕊溶液看到其先变红后褪色,推测氯水中含有Cl2分子
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,推测氯水中可能含有Cl-
C.向氯水中加入碳酸钠粉末,有气泡产生,推测氯水中含有H+
D.氯水放置一周后pH将变大,说明氯水中含有ClO-
20.下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)( )
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | NaCl(Na2CO3) | CaCl2溶液 | 分液 |
B | CO2(CO) | O2 | 点燃 |
C | Fe(Cu) | 稀盐酸 | 过滤 |
D | Cl2(HCl) | 饱和氯化钠溶液、浓硫酸 | 洗气 |
三、简答题:本题共3小题,共40分.将解答填写在答题卡上相应的位置.
21.(12分)
(1)阳离子共有m个电子,则中子数N= 。
(2)某金属氯化物MCl240.5g,含有0.6mol Cl-,则该氯化物的摩尔质量是 。
(3)KClO2属于钾盐,其中氯元素的化合价为 ;KClO2在水溶液中完全电离,则其电离方程式为: 。
(4)写出分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)两种互溶液体的方法
,写出从碘水中提取碘单质的方法 。
22.(14分)某校化学实验小组设计下图装置制备氯气,图中涉及气体发生、除杂、干燥、收集及尾气处理装置。
(1)上述装置中,错误的是 (选填字母)。
A.①②④ B.②③④ C.①③④ D.①②③
(2)写出装置①中发生反应的化学方程式是 ,将收集到的纯净氯气通入到碘化钾溶液中,再向其中加入四氯化碳振荡后静置,最终的实验现象是 ,发生反应的化学方程式是 。
(3)生产氯气的工业称为“氯碱工业”,写出化学方程式 。
(4)久置氯水的漂白作用会失效,写出发生该反应的化学方程式 。
(5)工业上用氯气生产漂白粉的化学反应方程式为 。
23.(14分)化学实验室使用的浓盐酸的溶质的质量分数通常为36.5%,密度为1.25g/ml。
(1)该盐酸的物质的量浓度为 mol/L。
(2)现有一种0.2mol/L的稀盐酸的含义是 (选填字母)。
A.1L水中含有0.2mol HCl
B.1L溶液中含有0.1mol H+
C.将7.1gHCl溶于1L水所配成的溶液
D.从100mL该溶液中取出10mL,剩余溶液的物质的量浓度仍为0.2mol/L
(3)用上述实验室的浓盐酸来配制500mL1 mol/L的稀盐酸,请在下列操作步骤中填写有关的空格:
①用量筒量取 mL的浓盐酸;(精确到小数点后一位)
②向盛有少量蒸馏水的烧杯中,沿 慢慢注入浓盐酸;
③将已冷却至室温的盐酸溶液沿玻璃棒注入 mL的容量瓶中;
④用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
⑤继续向容量瓶中加蒸馏水,直至液面接近刻度线1~2cm处;
⑥改用 逐滴加蒸馏水,使溶液凹液面恰好与刻度线相切;
⑦盖好容量瓶塞,反复颠倒,摇匀;
⑧将配好的稀硫酸倒入试剂瓶中,贴好标签。
(4)由于操作不当,会引起实验误差。下列情况对所配制的盐酸溶液的物质的量浓度有何影响?(用“偏高”、“偏低”、“无影响”填空)
①容量瓶用蒸馏水洗涤后残留有少量的水 ;
②定容时,某同学观察液面的情况如图所示 ;
③摇匀后,发现溶液的液面低于刻度线,又加水至刻度线 。
四、计算题:本题共1小题,共10分.解答写出必要的文字说明、方程式和重要的演算步骤.只写出最后答案的不能得分.
24.(10分)将标准状况下6.72L HCl溶于水配成100mL溶液,现用此盐酸与19.5g 锌粒反应制取氢气。试计算:(写出计算过程)
(1)此盐酸的物质的量浓度。
(2)若要使锌完全反应,则所需盐酸的最小体积。
(3)当锌粒完全反应时,制得标准状况下氢气的体积。
【参考答案】
1-15为单项选择题,每题2分;16-20为不定项选择题,每题4分
1.C 2.D 3.A 4.C 5.C 6.D 7.C 8.B 9.D 10.B 11.C 12.A
13.A 14.C 15.B 16.CD 17.B 18.AB 19.AD 20.D
21.(12分,每空2分)
(1)A-m-n
(2)135g/mol (单位不写扣1分)
(3)+3 KClO2=K++ ClO2−
(4)蒸馏 萃取和分液 (只写萃取的不扣分,但只写分液的得1分)
22.(14分,每空2分)
(1)B
(2)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,
溶液分层,上层为无色的水层,下层为紫红色的油层
Cl2+2KI=2KCl+I2
(3)2NaCl+2H2OCl2↑+ H2↑+2NaOH (通电或电解不写的扣2分)
光照
(4)2HClO = 2HCl+O2↑
(5)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
23.(14分)
(1)12.5(2分)
(2)D(2分)
(3)①40.0 (若写成40没有小数点的,该题得0分)
②烧杯内壁
③500
⑥胶头滴管(该题共4空,每空1分,共4分)
(4)①无影响 ②偏高 ③偏低(该题共3空,每空2分,共6分)
24.(10分)
(1)nHCl=6.72L/22.4L·mol=0.3mol (1分)
C HCl=0.3mol/0.1L=3mol/L (2分)
(2)据题意,nZn =19.5g/65g·mol=0.3mol (1分)
金属Zn过量,盐酸不够,要使Zn全部反应,根据化学方程式
Zn+ 2HCl = ZnCl2 + H2↑
1mol 2mol
0.3mol nHCl nHCl(至少)=0.6mol (1分)
所以VHCl(至少)=0.6mol/3 mol·L=0.2L=200mL (2分)
(3) Zn+ 2HCl = ZnCl2 + H2↑
1mol 22.4L
0.3mol V H2 V H2=6.72L (3分)
注:
1.计算题如果有其他合理解法,也可给分。但要按步骤给分,只有最终结果而无解题过程的,一律不给分。
2.化学方程式书写,若化学式书写错误则全部扣除该题的分数;若配平错误或反应条件或气体符号不写的,扣该题分数的一半。








