

2026年黄冈市中考二模化学试题(含答案解析)
展开 这是一份2026年黄冈市中考二模化学试题(含答案解析),共12页。试卷主要包含了答题时请按要求用笔等内容,欢迎下载使用。
1.答题前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在条形码区域内。
2.答题时请按要求用笔。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试卷上答题无效。
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
5.保持卡面清洁,不要折暴、不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
一、选择题(本题包括12个小题,每小题3分,共36分.每小题只有一个选项符合题意)
1.化学在生产、生活中应用广泛。下列过程不涉及化学变化的是
A.木炭燃烧B.裁切玻璃
C.铁钉生锈D.醋除水垢
2.下列实验现象描述正确的是
A.在加热的条件下,一氧化碳还原氧化铜时黑色粉末逐渐变为红色
B.电解水一段时间后,正负极产生气体的质量比约为1:2
C.打开盛有浓盐酸的瓶盖,在瓶口出现大量白烟
D.二氧化碳能使干燥的紫色石蕊纸花变红
3.下列有关实验现象描述正确的是( )
A.打开盛有浓盐酸试剂瓶的瓶塞,瓶口出现大量白烟
B.将一氧化碳通入装有灼热氧化铜的玻璃管,生成铜和二氧化碳
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.向蒸馏水中加入适量肥皂水搅拌,产生大量泡沫
4.下列各组离子能在碳酸钠溶液中大量共存的是
A.Na+、SO42-、OH-B.K+、Cu2+、OH-
C.Zn2+、Na+、Cl-D.Ba2+、H+、NO3—
5.下列各种铜矿石的主要成分中,含元素种类最多的是
A.赤铜矿(Cu2O)
B.辉铜矿(Cu2S)
C.斑铜矿(Cu5FeS4)
D.孔雀石[ Cu2 (OH)2CO3]
6.为减缓化学反应速率,下列做法合理的是
A.面团发酵时放在温热处B.在食品密封包装时充入氮气
C.煤燃烧时向煤炉中鼓入空气D.用食醋除水垢时使用浓度高的食醋
7.如图所示,甲是溴(Br)的原子结构示意图,乙摘自元素周期表。下列说法正确的是
A.甲元素属于金属元素
B.甲、乙两种元素形成化合物的化学式是NaBr
C.乙原子的核内中子数为11
D.甲原子核外共有5个电子层
8.a、b、c三种固体物质的溶解度曲线如图,下列说法错误的是( )
A.t1℃时等质量的a、c饱和溶液中,所含水的质量相等
B.t1℃时a、b、c饱和溶液升温至t2℃,所得溶液的溶质质量分数大小关系是a=b>c
C.要从含有少量b的a饱和溶液中获得a,最好的方法是降温结晶
D.c物质可能是熟石灰
9.下列事例不能用分子运动相关知识解释的是( )
A.品红溶解B.篮球充气
C.酒精挥发D.柳絮飞扬
10.现有甲、乙、丙三种金属,如果把甲和乙分别放入稀硫酸中,甲溶解并产生氢气,乙不反应;如果把乙和丙分别放入硝酸银溶液中,过一会儿,在乙的表面有银析出,而丙没有变化,根据以上事实,则甲、乙、丙的金属活动性由强到弱的顺序是
A.甲>乙>丙 B.乙>甲>丙 C.乙>丙>甲 D.丙>乙>甲
11.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
A.待测值为0.6
B.此反应可表示为:丙+丁→甲
C.反应中甲和丁变化的质量比为1:2
D.甲一定是化合物
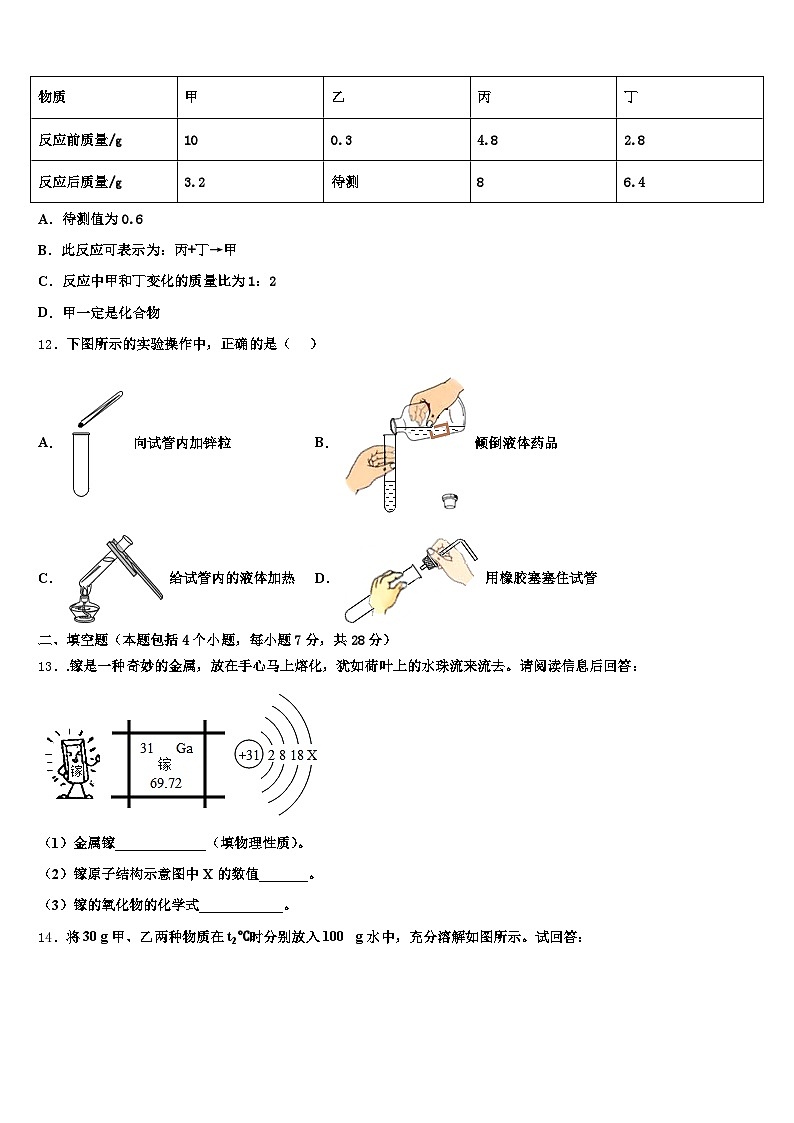
12.下图所示的实验操作中,正确的是( )
A.向试管内加锌粒B.倾倒液体药品
C.给试管内的液体加热D.用橡胶塞塞住试管
二、填空题(本题包括4个小题,每小题7分,共28分)
13..镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。请阅读信息后回答:
(1)金属镓_____________(填物理性质)。
(2)镓原子结构示意图中X的数值_______。
(3)镓的氧化物的化学式____________。
14.将30 g甲、乙两种物质在t2℃时分别放入100 g水中,充分溶解如图所示。试回答:
A试管中放的物质是_____(填“甲”或“乙”),此时另一支试管中的溶液是_____(填“饱和”或“不饱和”),该溶液中溶质质量分数是_____(保留1位小数),若将温度降至t1℃时,试管 B中的现象是_____。在t2℃时,若要让试管A中的固体全部溶解,可向烧杯的水中加入_____(填序号)。
①硝酸铵 ②氢氧化钠 ③氯化钠
15.实验室有一瓶未知浓度的氯化钠溶液,小丽要测定其溶质的质量分数。小丽取出100克氯化钠溶液,放在蒸发皿中加热蒸干。在加热的过程中,当观察到有较多固体析出时,小丽的正确操作是_________。冷却后,小丽将蒸发皿中的氯化钠放在天平上称量:小丽加了一个砝码,待天平静止时,出现如图所示的情况,小丽接下来的操作是:_____,读数,得到氯化钠的质量。
小丽发现有少量氯化钠粘在蒸发皿上,这对结果有何影响?_________________。
16.SO2和CO2具有相似的化学性质,实验室里做硫燃烧实验时,可在集气瓶中加入NaOH溶液来吸收SO2,图中小球分别表示NaOH溶液及吸收SO2后所得溶液中溶质的微粒。该反应的化学方程式为_____;反应前后不变的微粒是_____(填“分子”或“原子”):其中“●”、“”分别表示的微粒符号是_____。
三、实验题(本题包括2个小题,每小题7分,共14分)
17.根据下列装置图,回答有关问题:
仪器①的名称是__。从节能环保方面考虑,实验室制取较纯净的O2, 应选择的发生与收集装置是__(填序号),发生反应的化学方程式为___,反应物中氧元素的化合价为___。组装 A 装置时,酒精灯应在固定试管之_______(填“前”或“后”)放置,该装置一般用于____固体(填“药品名称”)制氧气时使用,试管口的棉花团作用是___。写出用一种白色固体制取氧气的化学方程式____。如果用大理石和浓盐酸制取CO2,常混有HCl气体,为了得到一瓶纯净干燥的二氧化碳,连接装置的顺序____,其中除去HCl气体时发生的反应的化学方程式为_____。对于制取CO2后剩下的溶液甲同学进行探究,取少量的溶液滴加无色酚酞试液,溶液无色,甲同学猜想剩余溶液一定是氯化钙溶液。(氯化钙溶液显中性)大家一致认为甲同学实验不能证明他的猜想,理由是___。如果要证明甲的猜想是正确的,可以选择____(填字母)来代替酚酞试液。
A 石蕊试液 B 氢氧化钠溶液 C 稀硫酸
18.某化学兴趣小组同学进行如下实验探究。实验室常用的制取气体的装置如图:
仪器a的名称_____。实验室制二氧化碳的反应方程式为_____,该反应属于_____(填写基本反应类型)实验室用过氧化氢溶液和二氧化锰粉末混合制取氧气,选用的装置组合可以是_____,装置B中注射器的作用是_____。若用G装置收集氧气,写出验满的方法_____,用制得的氧气做铁丝燃烧实验时没看见火星四射,原因可能是_____。某同学用一定浓度盐酸与石灰石在一个密闭性良好的装置里反应,将生成的气体通入澄清石灰水中,始终未见浑浊,造成此现象的可能原因:_____。
四、计算题(本题包括1个小题,共12分)
19.(6分)现有碳酸钠和氯化钠的固体混合物12.6g,其中含氧元素4.8g,将该混合物加入到一定质量的稀盐酸中,恰好完全反应,得到137g氯化钠溶液。计算:原固体混合物中碳酸钠的质量分数(结果保留至0.1%)______;所用稀盐酸中溶质的质量分数(结果保留至0.1%)______。
参考答案
一、选择题(本题包括12个小题,每小题3分,共36分.每小题只有一个选项符合题意)
1、B
【解析】
A、木炭燃烧过程中有新物质二氧化碳等生成,属于化学变化,不符合题意;
B、裁切玻璃过程中只是形状发生改变,没有新物质生成,属于物理变化,符合题意;
C、铁钉生锈过程中有新物质铁锈生成,属于化学变化,不符合题意;
D、醋除水垢过程中有新物质生成,属于化学变化,不符合题意。故选B。
化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别:是否有新物质生成。
2、A
【解析】
A、一氧化碳具有还原性,在加热的条件下,一氧化碳还原氧化铜生成铜,黑色粉末逐渐变为红色,故A正确;
B、电解水一段时间后,正负极产生气体的体积比约为1:2,质量比为8:1,故B错误;
C、打开盛有浓盐酸的瓶盖,在瓶口出现大量白雾,而不是白烟,故C错误;
D、二氧化碳能与水化合生成了碳酸,碳酸使紫色石蕊变红,二氧化碳不能使干燥的紫色石蕊纸花变红,故D错误。
故选:A。
3、D
【解析】
A、打开盛浓盐酸试剂瓶的瓶塞,瓶口上方出现白雾,而不是白烟,烟是固体小颗粒,雾是小液滴,错误;B、生成铜和二氧化碳是实验结论不是现象,错误;C、铁丝在空气中不燃烧,错误;D、蒸馏水是软水,向蒸馏水中加入适量肥皂水搅拌,产生大量泡沫,正确。故选D。
4、A
【解析】
碳酸钠溶液中含有钠离子和碳酸根离子。
A、五种四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确。
B、Cu2+、OH-两种离子能结合成氢氧化铜沉淀,不能大量共存,故选项错误。
C、Zn2+、CO32-两种离子能结合成碳酸锌沉淀,不能大量共存,故选项错误。
D、Ba2+、H+与CO32-离子,分别能结合成碳酸钡沉淀、二氧化碳和水,不能大量共存,故选项错误。
故选:A。
判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水。
5、D
【解析】
A、赤铜矿中含有铜元素和氧元素两种元素;
B、辉铜矿中含有铜元素和硫元素两种元素;
C、斑铜矿中含有铜、铁、硫三种元素;
D、孔雀石中含有铜、氢、碳、氧四种元素;
故选:D。
6、B
【解析】
试题分析:影响化学反应速率的因素有浓度、温度、压强、催化剂以及固体表面积、溶剂等因素,A.面团发酵时放在温热处,温度升高,物质反应的速率加快,选项错误;B.氮气化学性质不活泼,在食品密封包装时充入氮气,可以延缓食品的发生缓慢氧化的速率,选项正确;C.煤燃烧时向煤炉中鼓入空气,增大了反应物的接触面积,加快反应的速率,选项错误;D.用食醋除水垢时使用浓度高的食醋,物质间的接触面积增大,加快反应的速率,选项错误.
考点:影响化学反应速率的因素探究;常见气体的用途;醋酸的性质及醋酸的含量测定;完全燃烧与不完全燃烧
7、B
【解析】A、根据元素周期表中的一格可知,中间的汉字表示元素名称,甲元素的名称是溴,带“氵”字旁,属于非金属元素,错误;B、甲是溴(Br),溴的原子最外层电子数为7,在化学反应中易得到1个电子形成稳定结构,通常显-1价,乙元素是钠元素,原子最外层电子数为1,在化学反应中易失去1个电子形成稳定结构,通常显+1价,甲、乙两种元素形成化合物的化学式是NaBr,正确;C、根据元素周期表中的一格可知,乙的原子序数为11,根据原子序数=质子数,乙原子的核内质子数为11,不是中子数为11,错误;D、根据原子结构示意图可知,甲原子核外共有4个电子层,错误。故选B。
8、B
【解析】
A、t1℃时,a、c的溶解度相等,所以质量的a、c饱和溶液中,所含水的质量相等,此选项正确;
B、t1℃时a、b、c饱和溶液升温至t2℃,a、b的溶解度增大,变为饱和溶液,溶液的溶质质量分数不变,c溶解度减小,溶质质量分数变小,所得溶液的溶质质量分数大小关系是b>a>c,此选项错误;
C、a的溶解度受温度影响较大,对于溶解度受温度影响较大的物质,采用降温结晶法使溶质从溶液中结晶析出,此选项正确;
D、熟石灰的溶解度随温度的升高而减少,c物质可能是熟石灰,此选项正确。
故选B。
在溶解度曲线上,溶剂的质量都是100g,所以分析溶质的质量分数时,只需要比较溶质的多少即可,溶解度变大时,溶质不变,溶解度减小时,溶质质量等于减小后的溶解度。
9、D
【解析】
A、品红的溶解是因为品红的分子在不断地运动,品红分子运动扩散到水中形成的,选项正确;
B、篮球充气是因为气体分子间有间隙,分子间的间隔变小被压缩到篮球中,选项正确;
C、酒精挥发是因为酒精分子在不断的运动,酒精分子不断扩散到空气中,选项正确;
D、柳絮是宏观物质,不是分子、原子等,所以不能用分子的观点解释柳絮飞扬现象,选项错误,故选D。
10、A
【解析】如果把甲和乙分别放入稀硫酸中,甲溶解并产生氢气,乙不反应,说明甲的活动性在氢之前,乙的活动性在氢之后,如果把乙和丙分别放入硝酸银溶液中,过一会儿,在乙的表面有银析出,而丙没有变化,说明乙的活动性比银强,丙的活动性比银弱,所以甲、乙、丙的金属活动性由强到弱的顺序是甲>乙>丙。故选A。
点睛:根据金属活动性顺序,金属与氧气,酸和盐溶液的反应可以判断金属的活动性。
11、D
【解析】
反应后质量增加的属于生成物,反应后质量减少的属于反应物,反应后质量不变可能属于催化剂。
【详解】
由表中数据分析可知,在反应前后,甲的质量减少了10g﹣3.2g=6.8g,是反应物,参加反应的甲的质量为6.8g;同理可以确定丙是生成物,生成的丙的质量为8g﹣4.8g=3.2g;丁是生成物,生成的丁的质量为6.4g﹣2.8g=3.6g;根据质量守恒定律,乙的质量不变,可能作该反应的催化剂,也可能没有参加反应,待测的数值为0.3g。A、根据以上分析可知待测值为0.3,错误;B、根据以上分析可知该反应的反应物为甲,生成物是丙和丁,此反应可表示为:甲→丙+丁,错误;C、根据以上分析可知反应中甲和丁变化的质量比为6.8g:3.4g=2:1,错误;D、该反应的反应物为甲,生成物是丙和丁,属于分解反应,甲是分解反应的反应物,一定是化合物,正确。故选D。
解题的关键是分析表中数据(反应后质量增加的属于生成物、质量减少的属于反应物),灵活运用质量守恒定律。
12、D
【解析】
A、取用密度较大的块状药品或金属颗粒放入玻璃容器时,应先把容器横放,把药品或金属颗粒放在容器口以后,再把容器慢慢竖立起来,使药品或金属颗粒缓缓的滑到容器底部,以免打破容器;故A错误;
B、取用液体药品时应注意:①瓶塞倒放,②标签对准手心,③瓶口紧挨试管口,④倒完液体后立即盖紧瓶塞,并把试剂瓶放回原处;故B错误;
C、给试管里的液体加热时,要用酒精灯的外焰加热,为防止试管内的液体沸腾溅出伤人,试管里的液体不应超过试管容积的1/3;故C错误;
D、在容器口塞橡皮塞,应把橡皮塞慢慢转动塞进容器口,切不可把容器放在桌子上再使劲塞进塞子,以免压破容器;故D正确;
故选D。
二、填空题(本题包括4个小题,每小题7分,共28分)
13、熔点低 3 Ga2O3
【解析】
(1)镓是一种奇妙的金属,放在手心马上熔化,说明金属镓的熔点低;
(2)在原子中,质子数=核外电子数,所以2+8+18+x=31,x=3,
(3)镓原子的最外层有3个电子,在化学反应中易失去3个电子而显+3价,氧元素化合价为-2价,镓的氧化物的化学式为:Ga2O3。
答案:
(1)熔点低;
(2)3;
(3)Ga2O3。
14、(1)乙 饱和 1.1% 有固体析出 (2)②
【解析】
试题分析:(1)根据物质A、B溶解的情况, A物质有固体剩余,结合甲、乙两物质在t2℃时的溶解度,甲>乙,故A试管中放的物质是乙,由于甲的溶解度刚好是30g,故将30g甲物质在t2℃时分别放入100g水中,充分溶解,得到的溶液是饱和溶液,此时溶液中溶质质量分数=30g/130g×100%=1.1%,由于甲的溶解度随温度的升高而增大,故若将温度降至t1℃时,试管 B中的现象是:有固体析出
(2)根据溶解度曲线,可知乙的溶解度也是随温度的升高而增大,故在t2℃时,若要让试管A中的固体全部溶解,可向烧杯的水中加入氢氧化钠,因为它溶于水放热,使温度升高,故选②
考点:溶解度曲线的意义,饱和溶液和不饱和溶液的转化
15、不断搅拌,撤酒精灯 取下10克砝码,加5克砝码。如果仍然是左高右低,取下5克砝码,拨动游码至天平平衡;如果左低右高,拨动游码至天平平衡。 使测定结果偏低
【解析】
(1)要用玻璃棒搅拌,目的是防止局部温度过高,造成液体飞溅;待蒸发皿中出现较多固体时,停止加热,利用余热蒸干,而不是水份全蒸干后再加热片刻,
(2)取下10克砝码,加5克砝码。如果仍然是左高右低,取下5克砝码,拨动游码至天平平衡;如果左低右高,拨动游码至天平平衡。
(3)使测定结果偏低,因为氯化钠有部分没有被称量到。
16、SO2+2NaOH=Na2SO3+H2O 原子 Na+、SO32-
【解析】
(1)二氧化硫与氢氧化钠反应生成亚硫酸钠和水,故填写:SO2+2NaOH=Na2SO3+H2O;
(2)根据质量守恒定律的微观实质:化学反应前后,原子种类、原子数目和原子质量不变可知,反应前后不变的微粒是原子,故填写:原子;
(3)由图可知, 是生成物中的一种微粒,该反应生成亚硫酸钠和水,水为难电离物,因此,图中用微粒表示的生成物是亚硫酸钠,由于,●在反应前后数目、形状没变,所以,●表示Na+,那么表示 SO32-,故填写:Na+、SO32-。
三、实验题(本题包括2个小题,每小题7分,共14分)
17、锥形瓶 BE -1 前 高锰酸钾 防止高锰酸钾颗粒堵塞导气管 B→G→F→C NaHCO3+HCl =NaCl + H2O +CO2↑ 如果溶液中盐酸过量,滴加酚酞试液也是无色的 A
【解析】
(1)仪器①是锥形瓶。
(2) 实验室用高锰酸钾、氯酸钾制取氧气都需要加热,用过氧化氢溶液制取氧气不需加热,故从节能环保方面考虑,实验室制取较纯净的O2,应选择过氧化氢溶液(加入二氧化锰作催化剂),固液常温反应制取气体,选择的发生装置是B,排水法收集的氧气较纯,可选择发生装置E,发生反应的化学方程式为:2H2O22H2O + O2↑,反应物中氧元素的化合价为-1。
(3) 组装 A 装置时,酒精灯应在固定试管之前放置,根据酒精灯的高度,可调整试管的高度,该装置的试管口放了一团棉花,一般用于高锰酸钾固体制氧气时使用,试管口的棉花团的作用是防止高锰酸钾颗粒堵塞导气管。高锰酸钾是紫色固体,氯酸钾是白色固体,故用白色固体制取氧气的化学方程式为:
(4) CO2中混有的HCl气体可用饱和碳酸氢钠溶液除去,浓硫酸具有吸水性,可干燥二氧化碳气体,最后除去水蒸气。故除去CO2中混有的HCl气体和水蒸气,连接装置的顺序为:B→G→F→C,其中除去HCl气体时发生的反应的化学方程式为:NaHCO3+HCl=NaCl+H2O + CO2↑。
(5)酚酞试液遇中性和酸性溶液均不变色,对于制取CO2后剩下的溶液甲同学进行探究,取少量的溶液滴加无色酚酞试液,溶液无色,甲同学猜想剩余溶液一定是氯化钙溶液。(氯化钙溶液显中性)大家一致认为甲同学实验不能证明他的猜想,理由是如果溶液中盐酸过量,滴加酚酞试液也是无色的。紫色石蕊遇酸性溶液变红,所以如果要证明甲的猜想是正确的,可以选择石蕊试液来代替酚酞试液,故选A。
根据反应物的状态及反应条件选择发生装置,用排水法收集的气体较纯净。气体中含有多种气体杂质,其中一种是水蒸气,一般是最后除去水蒸气。
18、长颈漏斗 复分解反应 BD或BE 可以控制反应的速率 将带火星的木条放在c管端口处,观察木条是否复燃 铁丝表面的铁锈未除去或氧气不纯 盐酸的浓度过大
【解析】
(1)仪器a是长颈漏斗;故填:长颈漏斗;
(2)实验室中制取二氧化碳的反应原理是碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,该反应属于复分解反应;故填:;复分解反应;
(3)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应固液常温型,其中二氧化锰是一种粉末,所以选择B来制取,氧气密度比空气大,不易溶于水,所以选用的装置组合可以是BD或BE,装置B中注射器的作用是可以控制反应的速率;故填:BD或BE;可以控制反应的速率;
(4)氧气的密度比空气大,用装置G来收集氧气时,氧气从长管进入,验满时将带火星的木条放在短管端口处,观察木条是否复燃即可,用制得的氧气做铁丝燃烧实验时没看见火星四射,原因可能是:铁丝表面的铁锈未除去或氧气不纯;故填:将带火星的木条放在c管端口处,观察木条是否复燃;铁丝表面的铁锈未除去或氧气不纯;
(5)实验室要制取CO2,取一定浓度盐酸与石灰石在一个密闭性良好的装置里反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能是因为盐酸的浓度过大,故填:盐酸的浓度过大。
四、计算题(本题包括1个小题,共12分)
19、84.1% 5.7%
【解析】
(l)原固体混合物中碳酸钠的质量分数4.8g÷=10.6g;混合物中碳酸钠的质量分数为10.6g÷12.6g×100%≈84.1%;
(2)设盐酸中溶质的质量为x,生成二氧化碳质量为y
所用稀盐酸中溶质的质量分数7.3g÷(137g+4.4g-12.6g)×100%≈5.7%
物质
甲
乙
丙
丁
反应前质量/g
10
0.3
4.8
2.8
反应后质量/g
3.2
待测
8
6.4
相关试卷
这是一份2026年黄冈市中考二模化学试题(含答案解析),共12页。试卷主要包含了答题时请按要求用笔等内容,欢迎下载使用。
这是一份黄冈市2026年中考五模化学试题(含答案解析),共12页。试卷主要包含了有关溶液说法错误的是,下列实验操作正确的是,下列水果中酸度最强的是等内容,欢迎下载使用。
这是一份2026年黄冈市中考化学全真模拟试卷(含答案解析),共13页。试卷主要包含了答题时请按要求用笔,下列实验操作正确的是,下列化学方程式书写正确的是等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)





