



所属成套资源:2026届高考化学二轮复习专题练习
第21练 化学反应原理综合(A)(含答案)2026届高考化学二轮复习专题练习
展开 这是一份第21练 化学反应原理综合(A)(含答案)2026届高考化学二轮复习专题练习,文件包含专题五第21练化学反应原理综合Adocx、第21练化学反应原理综合A学生版docx等2份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。
(1)已知氨气的部分反应及信息如下:
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ΔH=-265 kJ·ml-1;
NH3(g)===NH3(l) ΔH=-23 kJ·ml-1;
NH3(l)的密度为0.68 kg·L-1。
1 L NH3(l)完全燃烧生成N2(g)和H2O(g),可以产生的热量是 。
(2)一种合成气(含体积分数为54%的H2、35%的CO、7%的CO2和4%的N2)可通过如图1所示转化制取合成氨气的原料。
①若转化Ⅰ中CO、CO2完全反应,得到的Fe3O4和CaCO3的物质的量之比为 。
②实际进行转化(Ⅰ)反应时,合成气中需添加一定量的水蒸气。添加水蒸气的目的是 。
③其他条件一定,将添加了水蒸气的合成气通过装有Fe2O3和CaO的反应管,测得出口处CO的体积分数与反应温度的关系如图2所示。
ⅰ.400~550 ℃,温度越高,出口处CO体积分数越低的原因是 。
ⅱ.高于550 ℃,出口处CO体积分数随温度升高而增大的原因是 。
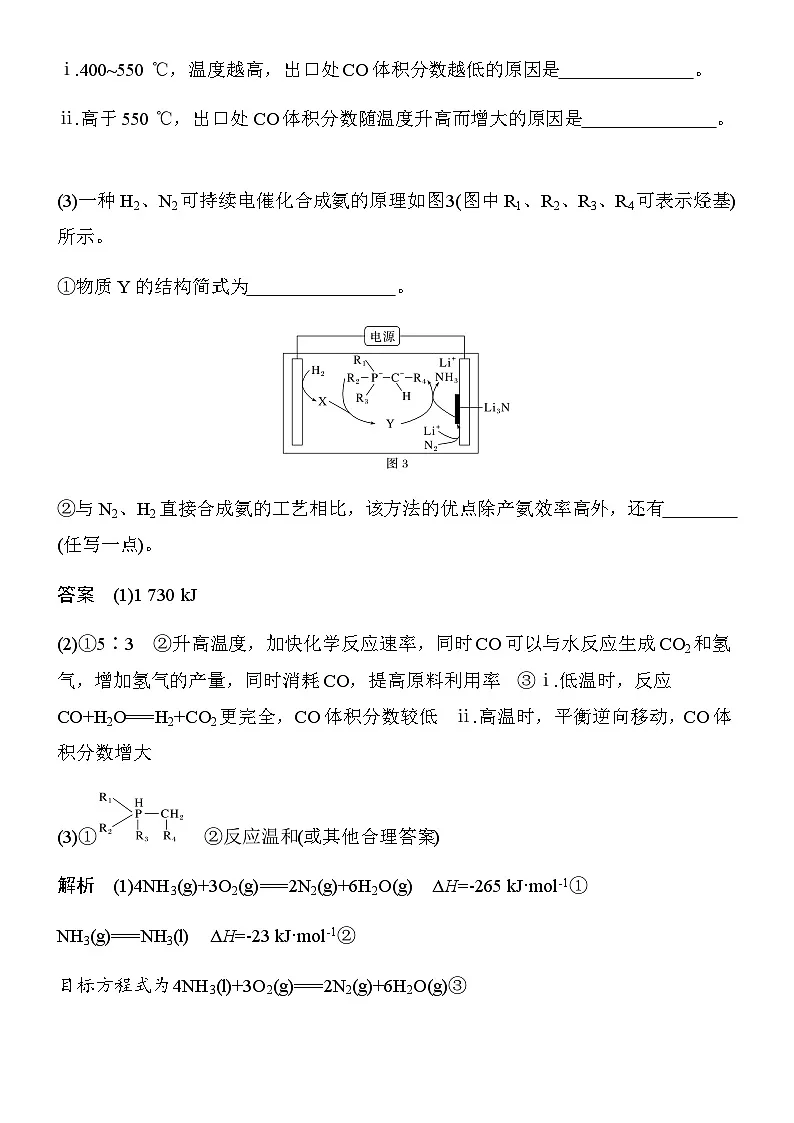
(3)一种H2、N2可持续电催化合成氨的原理如图3(图中R1、R2、R3、R4可表示烃基)所示。
①物质Y的结构简式为 。
②与N2、H2直接合成氨的工艺相比,该方法的优点除产氨效率高外,还有 (任写一点)。
答案 (1)1 730 kJ
(2)①5∶3 ②升高温度,加快化学反应速率,同时CO可以与水反应生成CO2和氢气,增加氢气的产量,同时消耗CO,提高原料利用率 ③ⅰ.低温时,反应CO+H2O===H2+CO2更完全,CO体积分数较低 ⅱ.高温时,平衡逆向移动,CO体积分数增大
(3)① ②反应温和(或其他合理答案)
解析 (1)4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ΔH=-265 kJ·ml-1①
NH3(g)===NH3(l) ΔH=-23 kJ·ml-1②
目标方程式为4NH3(l)+3O2(g)===2N2(g)+6H2O(g)③
则③=①-4×②,ΔH=(-265 kJ·ml-1)-4×(-23 kJ·ml-1)=-173 kJ·ml-1,液氨的物质的量n=0.68×1 000×117 ml=40 ml,当液氨为40 ml时,放出的热量为404×173 kJ=1 730 kJ。
(2)①同温同压下,气体的物质的量之比等于体积之比,设混合气体物质的量为1 ml,则根据CO+3Fe2O3===2Fe3O4+CO2,n(Fe3O4)=2n(CO)=2×35%×1 ml=0.7 ml,生成的二氧化碳的物质的量n(CO2)=n(CO)=0.35 ml,体系中二氧化碳一部分是原来有的0.07 ml,一部分是CO反应生成的0.35 ml,则n总(CO2)=(0.35+0.07) ml=0.42 ml,根据化学方程式:CO2+CaO===CaCO3可知,n(CaCO3)=n总(CO2)=0.42 ml,得到的Fe3O4和CaCO3的物质的量之比为0.7∶0.42=5∶3。
(3)H2-2e-===2H+,产生氢离子带正电,与带负电的离子结合,所以产物Y为,电解过程反应温和,不需要高温高压,从而降低了能耗和设备要求。
2.(15分)(2025·南京中华中学二模)氢能是一种极具发展潜力的绿色能源,制氢方法是当前研究的热点,制氢方法很多,如甲烷与水蒸气重整制氢、硼氢化钠(NaBH4)水解制氢等。
(1)甲烷水蒸气重整制氢,其涉及如下两步反应:
Ⅰ.CH4(g)+H2O(g)CO(g)+3H2(g) ΔH1=206 kJ·ml-1
Ⅱ.CO(g)+H2O(g)CO2(g)+H2(g) ΔH2=-41 kJ·ml-1
①实验发现,其他条件不变,向体系中加入CaO可明显提高平衡体系中H2的含量。分析投入CaO时,H2含量增大的原因是 。
②CH4(g)+2H2O(g)CO2(g)+4H2(g),该反应需在高温下才能自发进行,其理由是 。
(2)NaBH4水解制氢:常温下,NaBH4自水解过程缓慢,需加入催化剂提高其产氢速率。NaBH4在某催化剂表面制氢的微观过程如图1所示。已知:浓度较大时,NaB(OH)4易以NaBO2形式结晶析出。
①其他条件不变时,以D2O代替H2O催化释氢,所得气体的分子式为 ,其中过程b步用化学方程式表示为 。
②在催化剂的作用下,NaBH4与水反应,释氢体积及温度随反应时间的变化如图2所示。0~20 min内,温度随时间快速升高的原因是 。
(3)NaBH4转化为NaBO2后,电解NaBO2溶液又可制取NaBH4,实现物质的循环利用,电解装置如图3所示。
①阴极上的电极反应式是 。
②两电极区间使用阳离子交换膜,不能用阴离子交换膜的原因是 。
答案 (1)①CaO为碱性氧化物,能吸收酸性氧化物CO2,导致CO2浓度减小,促使反应Ⅱ平衡正向移动,导致CO浓度减小,引起反应Ⅰ平衡也正向移动,从而提高平衡体系中H2的含量 ②ΔH=206 kJ·ml-1-41 kJ·ml-1=165 kJ·ml-1,该反应的ΔS>0,根据ΔG=ΔH-TΔS
相关试卷
这是一份第21练 化学反应原理综合(A)(含答案)2026届高考化学二轮复习专题练习,文件包含专题五第21练化学反应原理综合Adocx、第21练化学反应原理综合A学生版docx等2份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。
这是一份第22练 化学反应原理综合(B)(含答案)2026届高考化学二轮复习专题练习,文件包含专题五第22练化学反应原理综合Bdocx、第22练化学反应原理综合B学生版docx等2份试卷配套教学资源,其中试卷共14页, 欢迎下载使用。
这是一份【原创】2022届高考二轮专题精选练习题 化学(十六) 化学反应原理综合,文件包含原创2022届高三二轮专题卷化学十六化学反应原理综合学生版docx、原创2022届高三二轮专题卷化学十六化学反应原理综合教师版docx等2份试卷配套教学资源,其中试卷共76页, 欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




