

湖南省衡阳市衡阳县第四中学2025~2026学年高二上册期末模拟综合测评卷化学(A卷)(含答案)
展开 这是一份湖南省衡阳市衡阳县第四中学2025~2026学年高二上册期末模拟综合测评卷化学(A卷)(含答案),共20页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
分值:100 分 时间:75 分钟
一、选择题:本题共 14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是 符合题目要求的。
1.下列装置或过程能实现化学能转化为电能的是( )
2.合理使用燃料可减少污染,符合“绿色化学”理念。下列说法正确的是( )
A.“可燃冰”是将水变为油的新型燃料
B.通入过量的空气使燃料充分燃烧,以达到充分利用热能的目的
C.燃料的化学能可以在不同的条件下转化为热能、电能被人类利用
D.S的标准燃烧热为,S的标准燃烧热的热化学方程式:
3.中华文明璀璨夺目,人们很早就在生产、生活中掌握了能量的相互转化,下列说法中错误的是( )
A.宋代词人辛弃疾的《青玉案·元夕》中有对“打铁花”描述的诗句:“东风夜放花千树,更吹落,星如雨。”这个过程涉及化学能转化成光能与热能
B.《本草纲目》中有记载:“阳燧,火镜也。以铜铸成,其面凹,摩热向日,以艾承之,则得火。”这个过程涉及化学能转化成热能
C.《易经》中记载:“泽中有火”“上火下泽”,这个过程涉及化学能转化成热能
D.南宋《大冶赋》中详细记载了以炭与铜矿石为原料的火法炼铜技术,这个过程涉及热能转化为化学能
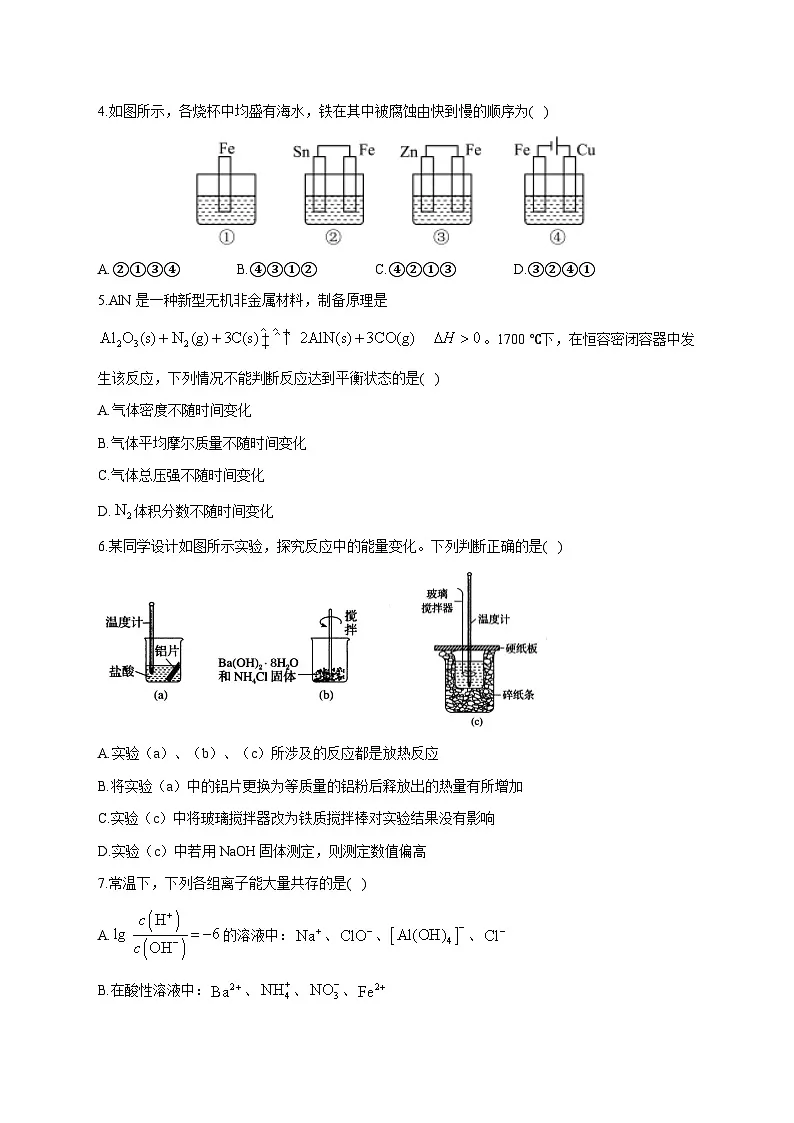
4.如图所示,各烧杯中均盛有海水,铁在其中被腐蚀由快到慢的顺序为( )
A.②①③④B.④③①②C.④②①③D.③②④①
5.AlN是一种新型无机非金属材料,制备原理是。1700 ℃下,在恒容密闭容器中发生该反应,下列情况不能判断反应达到平衡状态的是( )
A.气体密度不随时间变化
B.气体平均摩尔质量不随时间变化
C.气体总压强不随时间变化
D.体积分数不随时间变化
6.某同学设计如图所示实验,探究反应中的能量变化。下列判断正确的是( )
A.实验(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将玻璃搅拌器改为铁质搅拌棒对实验结果没有影响
D.实验(c)中若用NaOH固体测定,则测定数值偏高
7.常温下,下列各组离子能大量共存的是( )
A.的溶液中:、、、
B.在酸性溶液中:、、、
C.1 的溶液中:、、、
D.由水电离出的的溶液中:、、、
8.甲醛()氧化历程如图所示(各物质均为气态,部分物种未标出)。下列叙述错误的是( )
A.总反应中有5个基元反应
B.过渡态TS2的能垒最大
C.加入催化剂主要作用是降低TS3能垒
D.总反应的
9.汽车尾气中NO产生的反应为。一定条件下,等物质的量和在恒容密闭容器中反应,曲线a表示在温度T下随时间(t)的变化,曲线b表示改变某一条件时随时间(t)的变化。下列叙述不正确的是( )
A.温度T下、0~40 s内
B.M点小于N点
C.曲线b对应改变的条件可能是充入氧气
D.若曲线b对应改变的条件是升高温度,则
10.下列对应的实验操作、现象和结论,不正确的是( )
11.下列溶液中离子浓度关系正确的是( )
A.0.1 氨水和0.1 溶液相比,前者大于后者
B.pH=9的溶液中:
C.溶液中
D.0.2 溶液和0.1 盐酸等体积混合,在混合溶液中:
12.如图装置中,b为标准氢电极,可发生还原反应()或氧化反应(),a、c分别为、AgI/Ag电极。实验发现:1与2相连a电极质量减小,2与3相连c电极质量增大。下列说法正确的是( )
A.1与2相连,盐桥①中阳离子向b电极移动
B.2与3相连,电池反应为
C.1与3相连,a电极减小的质量等于c电极增大的质量
D.1与2、2与3相连,两个原电池装置中,电势较低的一极均为b电极
13.常温下.用0.1000 的溶液分别滴定20.00 mL浓度均为0.1000 的溶液和HCN溶液.所得滴定曲线如图:
下列说法错误的是( )
A.常温下.的电离平衡常数
B.含有等物质的量的HCN和NaCN的混合溶液中:
C.②对应溶液中存在:
D.将④和⑤对应溶液混合,混合后的溶液中存在:
14.常温下,向含(醋酸钠)、、的混合液中滴加溶液,混合液中与pX[、、]的关系如图所示。已知:相同条件下的溶解度大于的溶解度。下列说法错误的是( )
A.代表和的关系
B.向M点所示的混合溶液中加入固体增大
C.常温下,饱和溶液中
D.当同时生成和时,溶液中
二、非选择题:本大题共 4小题,共 58分
15.(12分)电解原理在工业生产中应用广泛,利用电解池可以生产化工品和处理环境污染物等。
(1)“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速率缓慢的问题,科技工作者设计耦合高效制的方法,装置如图甲所示。
部分反应机理为。
①阳极的电极反应式为_________。
②相同电量下,理论上的产量是传统电解水的_________倍。
(2)研究的综合利用、实现资源化是能源领域的重要发展方向。生物电催化技术运用微生物电解池实现了,甲烷化,其工作原理如图乙所示。
①微生物电解池实现甲烷化的阴极的电极反应式为_________。
②如果处理有机物产生标准状况下112 的,则理论上导线中通过的电子的物质的量为_________。
16.(14分)金属腐蚀是一个普遍存在的现象,其遍及国民经济和国防建设各个领域,危害十分严重,据估算,全世界每年因金属腐蚀造成的直接经济损失约占国民生产总值的2%~4%,这一数字甚至超过了水灾、火灾、风暴和地震等自然灾害的损失总和。金属的腐蚀与防护的研究对于减少经济损失、保障安全具有重要意义。回答下列问题:
(1)2024年5月8日,我国第三艘航空母舰福建舰顺利完成首次海试。舰体表面需要采取有效的防锈措施,下列防锈措施中可形成表面钝化膜的是________(填序号)。
①喷涂油漆②表面渗镀
③阳极氧化④发蓝处理
(2)2024年6月10日,我国自主设计建造的浮式生产储御油装置“海葵一号”在珠江口盆地的流花油田安家落户,其钢铁外壳镶嵌了锌块,以利用电化学原理延缓外壳的腐蚀。下列有关说法正确的是________(填序号)。
①钢铁外壳镶嵌的锌块可以用铜块替代②该法为外加电流法
③锌发生反应:④钢铁外壳为正极
(3)破损的镀锌铁皮在氨水中发生电化学腐蚀,生成和,随着腐蚀的进行,溶液的pH会________(填“变小”“不变”或“变大”),铁电极的电极反应式为________________________。
(4)钼酸钠和苯并三氮唑(BTA)的混合液常作为碳钢的缓蚀剂。常温下,碳钢在不同浓度的硫酸和缓蚀剂介质中的腐蚀速率[单位:]数据如图所示。
①要使碳钢的缓蚀效果最优,钼酸钠和BTA的浓度比应为________。
②硫酸中碳钢的最高腐蚀速率和缓蚀剂中碳钢的最低腐蚀速率之比为________。
17.(16分)常用作食品加工中的食品添加剂,用于焙烤食品;在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)可用作净水剂,其原理是________________________(用离子方程式说明)。
(2)相同条件下,溶液中的________(填“等于”“大于”或“小于”)溶液中的。
(3)几种浓度均为的电解质溶液的pH随温度变化的曲线如图甲所示。
①其中符合溶液的pH随温度变化的曲线是________(填序号),导致溶液的pH随温度变化的原因是________。
②25 ℃时,溶液中________(列计算式,不必化简)。
(4)室温时,向溶液中滴加溶液,溶液pH与加入NaOH溶液体积的关系曲线如图乙所示。
①试分析图中a、b、c、d四个点中,水的电离程度最大的是________点。
②在b点,溶液中各离子浓度由大到小的排列顺序是________________。
③由b点到c点发生反应的离子方程式为________________________,
18.(16分)新能源是未来能源发展的方向,积极发展氢能是实现碳达峰、碳中和的重要举措。回答下列问题:
(1)近年来催化重整制氢是氢能源获取的重要途径,主要反应如下:
反应Ⅰ:
反应Ⅱ:
①反应Ⅰ能自发进行的条件是_________(填标号)。
A.高温B.低温C.任意温度D.无法判断
②工业生产时,通过提高水碳比来促进反应Ⅱ的进行,这样做的好处是__________________。
③下列操作中,有利于提高催化重整速率的是_________(填标号)。
A.及时分离出
B.增加催化剂的表面积
C.恒容时按原水碳比通入热的原料气
D.恒压时通入稀释气体
(2)反应Ⅱ也可在Pd膜反应器中进行,其工作原理如图1所示。
一定温度和压强下,等物质的量的CO和通入无Pd膜反应器,仅从a口出,CO的平衡转化率为75%;若换成Pd膜反应器,CO的平衡转化率为90%,则该温度下反应Ⅱ的平衡常数。K=_________,相同时间内出口a和出口b中的质量比为_________。
(3)硼氢化钠()是一种高效储氢材料,25 ℃时在掺杂了的纳米合金催化剂表面活性位点水解制氢的机理如图2。
①写出与水反应生成和的离子方程式_________。
②已知25 ℃时和在水中的溶解度分别为28 g和55 g,其他条件相同,测得平均每克催化剂使用量下,质量分数对制速率的影响如图3所示,制的最佳质量分数为10%,试分析浓度过低或过高反应速率变慢的原因_________。
答案及解析
1.答案:B
解析:风力发电把风能转化为电能;水果电池属于原电池,把化学能转化为电能;燃料燃烧把化学能转化为热能、光能等;手机充电把电能转化为化学能。故选B。
2.答案:C
解析:“可燃冰”外观像冰,其化学组成是,油是含碳化物形成的混合物,根据元素守恒知,水不能变为油,A错误;助燃,通入足量的空气能使燃料充分燃烧,但通入过量的空气会带走热量,不利于热量的充分利用,B错误;S不能一步转化为,标准燃烧热是101 kPa时,1 ml可燃物完全燃烧生成指定产物[]时的反应热,D错误。
3.答案:B
解析:A项,“打铁花”过程中铁与氧气反应,该反应放热,化学能转化成光能和热能,正确;B项,题述过程涉及太阳能转化成热能,错误;C项,题述过程是甲烷的燃烧过程,涉及化学能转化成热能,正确;D项,炭还原氧化铜生成铜为吸热反应,涉及热能转化为化学能,正确。
4.答案:A
解析:根据题图知,①中金属铁发生吸氧腐蚀;②③是原电池,②中金属铁作负极,③中金属铁作正极;④是电解池,金属铁作阴极,被保护;金属腐蚀的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>应用原电池原理保护的腐蚀>应用电解原理保护的腐蚀,所以腐蚀速率由快到慢的顺序是②①③④。故选A。
5.答案:B
解析:气体的体积为定值,气体的总质量为变量,反应过程中密度为变量,当气体密度不变时说明反应达到平衡状态,A不符合题意;和CO的相对分子质量都是28,所以混合气体相对分子质量为定值,气体平均摩尔质量不变不能作为判断该反应是否达到平衡的标志,B符合题意;该反应为气体物质的量增大的反应,气体总压强不断增大,气体总压强不变时说明反应达到平衡状态,C不符合题意;随反应进行,氮气体积分数减小,氮气体积分数不变时说明反应达到平衡状态,D不符合题意。
6.答案:D
解析:A.金属与酸的反应为放热反应,氢氧化钡晶体与氯化铵固体的反应为吸热反应,中和反应为放热反应,A错误;B.等质量的铝片和铝粉与盐酸反应放出的热量相同,只是放热速率加快,B错误;C.铁的导热性良好,换用铁质搅拌棒后会有热量损失,导致测定的数值偏低,C错误;D.氢氧化钠固体溶于水时放热,会使测定的数值偏高,D正确。
7.答案:A
解析:,,说明溶液pH=10,碱性环境下各离子间不反应,可大量共存,A正确;酸性溶液中具有强氧化性,可与具有还原性的发生氧化还原反应,不能大量共存,B错误;与发生络合反应,不能大量共存,C错误;水电离出的,说明水的电离受到抑制,溶液可能呈强酸性也可能呈强碱性,不能在强碱性环境下大量存在,不能在强酸性环境下大量存在,D错误。
8.答案:C
解析:在反应历程中,有5个过程生成了新的粒子,总反应中有5个基元反应,A正确;过渡态与活化能关系如下:
所以反应历程中,最大能垒为255 ,即过渡态TS2的能垒最大,B正确;活化能越大,反应速率越慢,慢反应决定总反应速率,加入催化剂降低TS2的能垒,提高总反应速率,C错误;从总反应历程看,反应物总能量高于生成物总能量,所以总反应放热,,D正确。
9.答案:B
解析:温度T下、0~40 s内氮气的浓度从减少到,故,A正确;N点时反应仍在正向进行,故N点时,而M点>N点的,则M点大于N点,B错误;充入氧气,反应速率加快,更快达到平衡,且平衡时氮气的浓度比曲线a中浓度小,C正确;若曲线b改变的条件为升温,平衡时浓度较曲线a减小,说明升温平衡正向移动,则正反应吸热,D正确。
10.答案:C
解析:与水解都生成HCl,室温下,、分别暴露在潮湿的空气中,只有明显冒白雾,说明水解能力:,A正确;滴有酚酞的溶液显红色,说明水解使溶液显碱性,加入少量固体,溶液红色变浅并有白色沉淀生成,说明与反应生成沉淀,浓度减小,使水解平衡逆向移动,浓度减小,碱性减弱,溶液红色变浅,B正确;室温下,用pH计分别测定0.1 溶液、溶液的pH,溶液的pH大,说明水解程度:,则酸性:,C错误;室温下,向两份0.1 草酸溶液中分别滴加0.1 溶液或溶液,只有产生沉淀,说明:,D正确。
11.答案:C
解析:是弱碱,电离程度很小,溶液中浓度很小,是强电解质,在水溶液中完全电离,电离出的有很少一部分发生水解,所以0.1 氨水和0.1 溶液相比,前者小于后者,A错误;pH=9的溶液中,根据元素守恒,,B错误;根据质子守恒,溶液中,C正确;0.2 溶液和0.1 盐酸等体积混合,得到等浓度的、和混合溶液,溶液显碱性,溶液中碳酸根离子水解程度大于碳酸氢根离子电离程度,溶液中,D错误。
12.答案:B
解析:1与2相连,a电极为正极,b电极为负极,盐桥①中阳离子向a电极移动,A错误;2与3相连,c电极质量增大,则Ag转化为AgI,b电极上生成氢气,电池反应为,B正确;1与3相连,a电极为正极,转化为Ag,c电极为负极,Ag转化为AgI,故a电极减小的质量小于c电极增大的质量,C错误;1与2相连,b电极为负极,b电极的电势较低,2与3相连,c电极为负极,c电极的电势较低,D错误。
13.答案:D
解析:未加溶液时,0.1000 醋酸溶液的pH约为3,,电离程度较小.则的电离平衡常数,A正确;含有等物质的量的HCN和NaCN的混合溶液.即为①对应的溶液.此时溶液呈碱性.说明水解程度大于HCN电离程度.则.溶液以这两种离子为主.故,B正确;②对应的溶液溶质为等物质的量的和,根据电荷守恒得.根据元素守恒得.联立两式可得.C正确;将④和⑤对应溶液混合.根据元素守恒得.则,D错误。
14.答案:D
解析:由审题指导可知,A正确;M点为和的交点,此时和相等,向M点所示的混合溶液中加入固体,增大,所以增大,B正确;饱和浴液甲仔在几次浴胖平衡, ,C正确;当同时生成和时,溶液中,即,D错误。
15.答案:(1)①(3分)
②2(3分)
(2)①(3分)
②(3分)
解析:(1)①据图甲可知,b电极上转化为,为氧化反应,所以b电极为阳极,a电极为阴极,为阳极反应物,由反应机理可知,和反应生成,生成的转化为,由原子守恒和电荷守恒可知,在生成的同时还生成了,生成的再与氢氧化钾进行酸碱中和,故阳极反应涉及两步:ⅰ.,ⅱ.,由(ⅰ+ⅱ)×2得阳极反应式为。
②根据①中阳极反应式,再结合阴极反应式:可知,转移2 ml电子时,阴、阳两极各生成1 ml ,共2 ml ,而传统电解水:,转移2 ml电子,只有阴极生成1 ml ,所以相同电量下,理论上的产量是传统电解水的2倍。
(2)①由题图乙可知,阴极上发生还原反应转化为甲烷,电极反应式为。
②标准状况下,112 的甲烷的物质的量为,由电极反应式:可知,转移的电子的物质的量为:。
16.答案:(1)②③④(2分)
(2)③④(2分)
(3)变大(2分);(2分)
(4)①2:1(3分);②75:1(3分)
解析:(1)喷涂油漆是将油漆涂在待保护的金属表面,并没有在表面形成钝化膜,①不符合题意;表面渗镀是在高温下将气态、固态或熔化状态的欲渗镀的物质(金属或非金属元素)通过扩散作用从被渗镀的金属的表面渗入内部以形成表层合金镀层的一种表面处理的方法,②符合题意;阳极氧化是将待保护的金属与电源正极连接,在金属表面形成一层氧化膜的过程,③符合题意;发蓝处理技术通常用于钢铁等黑色金属,通过在空气中加热或直接浸泡于浓氧化性溶液中来实现,可在金属表面形成一层极薄的氧化膜,这层氧化膜能有效防锈,④符合题意。
(2)钢铁外壳镶嵌了锌块,由于金属活动性:Zn>Fe,即锌块为负极,钢铁为正极,形成原电池,Zn失去电子,发生氧化反应,电极反应式为,从而保护钢铁,延缓其腐蚀。镶嵌的锌块如用铜块替代,即钢铁为负极,铜块为正极,形成原电池,钢铁外壳腐蚀会加快,因此钢铁外壳镶嵌的锌块不可以用铜块替代,①错误、③④正确;该方法为牺牲阳极法,②错误。
(3)腐蚀的总反应为,有生成,溶液的pH变大,该电化学腐蚀中Zn作负极,Fe作正极,正极上水得电子生成氢气,铁电极的电极反应式为。
(4)①要考虑碳钢在不同浓度的硫酸和缓蚀剂介质中的腐蚀速率,由题图可知,要使碳钢的缓蚀效果最优,钼酸钠和BTA的浓度比应为;②硫酸中碳钢的最高腐蚀速率为,缓蚀剂中碳钢的最低腐蚀速率为,二者之比为75:1。
17.答案:(1)(2分)
(2)小于(2分)
(3)①Ⅰ(2分);水解使溶液呈酸性,升高温度使其水解程度增大,pH减小;(2分)②(2分)
(4)①a(2分);②(2分);③(2分)
解析:(1)硫酸铝铵是强酸弱碱盐,在溶液中电离出的铝离子发生水解反应生成氢氧化铝胶体,表面积很大的氢氧化铝胶体能吸附水中悬浮颗粒,从而达到净化水的目的,水解的离子方程式为。
(2)硫酸铝铵和硫酸氢铵中的铵根离子在溶液中均发生水解反应,硫酸铝铵溶液中铝离子水解生成的氢离子会抑制铵根离子水解,硫酸氢铵在溶液中电离出的氢离子也会抑制铵根离子的水解,等浓度的硫酸氢铵在溶液中电离出的氢离子浓度大于硫酸铝铵中铝离子在溶液中水解生成的氢离子浓度,则硫酸氢铵对铵根离子水解的抑制程度大于硫酸铝铵,所以硫酸氢铵溶液中的铵根离子浓度大于硫酸铝铵溶液中的铵根离子浓度。
(3)①硫酸铝铵在溶液中电离出的铵根离子和铝离子水解使溶液显酸性,水解反应是吸热反应,升高温度,水解平衡向正反应方向移动,溶液中氢离子浓度增大,pH减小,则符合条件的曲线是Ⅰ。②由图甲可知,25 ℃时,硫酸铝铵溶液的pH为3,溶液中存在电荷守恒:,整理可得。
(4)由图乙可知,a点加入NaOH溶液体积为100 mL,根据反应的量化关系知,a点硫酸氢铵溶液恰好与氢氧化钠溶液反应得到硫酸钠和硫酸铵的混合溶液,溶液中的铵根离子水解促进水的电离;a点到d点发生的反应为和反应生成,b点溶液是硫酸钠、硫酸铵和一水合氨的混合溶液,溶液呈中性,水的电离既不被促进也不被抑制。①硫酸铵是强酸弱碱盐,在溶液中水解促进水的电离,一水合氨是弱碱,在溶液中电离出的氢氧根离子抑制水的电离,由分析可知,由a点到d点的过程中,铵根离子的浓度逐渐减小,一水合氨的浓度逐渐增大,由促进水的电离逐渐变成抑制水的电离,所以a点水的电离程度最大。②由分析可知,b点溶液为硫酸铵、硫酸钠和一水合氨的混合溶液,溶液呈中性,由元素守恒和电荷守恒可知,溶液中离子的浓度大小顺序为。③由分析可知,由b点到c点过程中,溶液中铵根离子与氢氧根离子反应生成一水合氨,离子方程式为。
18.答案:(1)①A(2分)
②消耗CO并放出热量,从而促进反应Ⅰ平衡正向移动,提高的转化率,同时生成了更多的(3分)
③BC(2分)
(2)9(2分);1:8(2分)
(3)①(2分)
②浓度较低时,催化剂表面活性位点未被充分利用,催化剂性能未充分发挥;浓度较高时,产物易吸附在催化剂表面,从而阻碍与催化剂活性位点的接触(3分)
解析:(1)①反应Ⅰ的、,根据时反应自发进行,则反应Ⅰ在高温条件下可自发进行。
②根据反应Ⅱ的热效应和相关物质的量两个角度思考提高水碳比的好处。反应Ⅱ的正反应放热,提高水碳比促进反应Ⅱ的正向进行,可放出更多的热量,从而促进反应Ⅰ的正向进行,提高了的转化率,同时生成了更多的。
③题目的要求是提高反应速率,应区别条件的改变对反应速率和化学平衡的影响。及时分离出,可促使平衡正向移动,但不能提高反应速率,A错误;增大催化剂的表面积,其活性位点更多,可提高反应速率,B正确;恒容且水碳比不变,但温度升高,可提高反应速率,C正确;恒压时通入,原料气被稀释,反应速率降低,D错误。
(2)第一步,根据无Pd膜反应器时的数据列“三段式”计算反应的平衡常数。设通入的CO和均为1 ml,无Pd膜反应器情况下一氧化碳的平衡转化率为75%,可列“三段式”如下:,因为反应前后气体分子数不变,用物质的量代替物质的量浓度计算K,则。第二步,计算有Pd膜反应器时出口a中的物质的量。有Pd膜反应器情况下,部分被选择性分离出去,一氧化碳的平衡转化率为90%,设达到平衡时出口a中的物质的量为n ml,列“三段式”如下:,温度不变,则K不变,故,解得n=0.1.第三步,计算相同时间内出口a和出口b中的质量比。出口a中的物质的量为0.1 ml,则出口b中的物质的量为0.9 ml-0.1 ml=0.8 ml,则相同时间内出口a和出口b中的质量比为1:8。
(3)①根据信息,和发生归中反应生成,离子方程式为。
②浓度较低时,催化剂表面活性位点未被充分利用,催化剂性能未充分发挥,反应速率较慢;浓度较高时,产物易吸附在催化剂表面,从而阻碍与催化剂活性位点的接触。
A
B
C
D
风力发电
水果电池
燃料燃烧
手机充电
选项
实验操作与现象
结论
A
室温下,、分别暴露在潮湿的空气中,只有明显冒白雾
水解能力:
B
向滴有酚酞的溶液中加入少量固体,溶液红色变浅并有白色沉淀生成
溶液中,存在水解平衡
C
室温下,用pH计分别测定0.1 溶液、溶液的pH,溶液的pH大
酸性:
D
室温下,向两份0.1 草酸溶液中分别滴加0.1 溶液或溶液,只有产生沉淀
:
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
B
A
B
D
A
C
B
C
题号
11
12
13
14
答案
C
B
D
D
过渡态
TS1
TS2
TS3
TS4
能垒/()
153.37
255
112.98
129.99
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





