
高考化学一轮复习-物质的量、气体摩尔体积(复习讲义)(全国通用)(原卷版)
展开 这是一份高考化学一轮复习-物质的量、气体摩尔体积(复习讲义)(全国通用)(原卷版),共13页。
02 \l "_Tc28904" 体系构建·思维可视 PAGEREF _Tc28904 \h 3
03 \l "_Tc21962" 核心突破·靶向攻坚 PAGEREF _Tc21962 \h 4
\l "_Tc23251" 考点一 物质的量 PAGEREF _Tc23251 \h 4
\l "_Tc33" 知识点1 物质的量、阿伏加德罗常数 PAGEREF _Tc33 \h 4
\l "_Tc17580" 知识点2 摩尔质量 PAGEREF _Tc17580 \h 4
\l "_Tc9369" 考向1 考查物质的量概念的理解 PAGEREF _Tc9369 \h 5
\l "_Tc23384" 考向2 考查物质的量、质量、微粒数之间的关系 PAGEREF _Tc23384 \h 5
\l "_Tc22008" 考点二 气体摩尔体 PAGEREF _Tc22008 \h 6
\l "_Tc25133" 知识点1 影响物质体积的因素 PAGEREF _Tc25133 \h 7
\l "_Tc32577" 知识点2 气体摩尔体积 PAGEREF _Tc32577 \h 7
\l "_Tc285" 知识点3 阿伏加德罗定律及其推论 PAGEREF _Tc285 \h 7
\l "_Tc22867" 考向1 考查气体摩尔体积与阿伏加德罗常数的正误判断 PAGEREF _Tc22867 \h 8
思维建模 抓“两看”,突破气体与状况陷阱
\l "_Tc23385" 考向2 考查阿伏加德罗定律及应用 PAGEREF _Tc23385 \h 10
思维建模 应用阿伏加德罗定律及其推论要注意两个问题
\l "_Tc15220" 考向3 考查气体摩尔质量计算的常用方法 PAGEREF _Tc15220 \h 11
思维建模 求气体摩尔质量M及相对分子质量的常用方法
04 \l "_Tc273" 真题溯源·考向感知 PAGEREF _Tc273 \h 12
考点一 物质的量
\l "_Tc25045" 知识点1 物质的量、阿伏加德罗常数
\l "_Tc25045" 知识点1 物质的量、阿伏加德罗常数
(1)物质的量(n):表示含有 的物理量,单位为 ,该物理量描述
的对象是微观粒子,如分子、原子、 、中子、质子、 等。
(2)物质的量的规范表示方法:
(3)阿伏加德罗常数(NA): 任何粒子的粒子数,符号是 ,单位为 。国际上规定,1ml 粒子集合体所含的粒子数,约为 。精确数值为 中所含的碳原子数为阿伏加德罗常数。
(4)公式: 。
得分速记
①物质的量只能衡量微观粒子(如分子、原子、离子、中子、质子、电子等),必须指明具体粒子的种类或化学式,故摩尔后面应为确切的微粒名称;如1 ml氢(不确切)和1 ml大米(宏观物质)皆为错误说法。
②物质的量是物理量,摩尔是物质的量的单位,不是物理量。
③6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(NA)是指1 ml任何微粒所含的粒子数,它与0.012 kg12C所含的碳原子数相同,数值约为6.02×1023。
\l "_Tc16775" 知识点2 摩尔质量
1.概念: 的物质所具有的质量,符号是 ,常用单位是 。
2.公式: 。
3.数值:以 为单位时,任何粒子的摩尔质量在数值上都等于该粒子的 。
得分速记
(1)物质的量是计量微观粒子“集体”的物理量,只适用于微观粒子(即分子、原子、离子、质子、中子、电子等),不适用于宏观物质。
(2)摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,摩尔质量的单位是g·ml-1或kg·ml-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·ml-1为单位时,二者在数值上相等。
(3)对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变化。
\l "_Tc17630" 考向1 考查物质的量概念的理解
例1 (24-25高三上·甘肃金昌·期中)下列有关物质的量和阿伏加德罗常数的说法正确的是
A.物质的量的单位是
B.物质的量可以表示微粒的数量
C.阿伏加德罗常数的单位是ml
D.阿伏加德罗常数的值约为6.02
【变式训练1·变载体】(24-25高三上·河南平顶山·质量检测)关于1.5mlH2O2,下列说法正确的是
A.摩尔质量是34gB.含有3mlH
C.含氧原子数目约为个D.含有15ml电子
【变式训练2·变考法】(2025高三下·浙江杭州·学业考试)摩尔质量的单位是
A.ml·L-1B.gC.g·ml-1D.ml·g-1
【变式训练3·】【科学研究与学科知识结合】2018年11月在法国凡尔赛召开的国际计量大会( CGPM)第26次会议将阿伏加德罗常数的定义修改为“1摩尔包含6.02214076×1023个基本单元,这常数被称为阿伏加德罗常数,单位为ml-1”。基于这一新定义,阿伏加德罗常数的不确定度被消除了。新定义将于2019年5月20日正式生效。NA为阿伏加德罗常数的值。下列说法错误的是
A.新定义中阿伏加德罗常数的不确定度被消除
B.0.4 ml NH3与0.6mlO2在催化剂的作用下充分反应,得到NO的分子数为0.4NA
C.2.7g铝中加入足量1ml·L-1的NaOH溶液,转移的电子数为0.3NA
D.常温常压下,水蒸气通过Na2O2使其增重2g时,反应中转移的电子数为NA
\l "_Tc16322" 考向2 考查物质的量、质量、微粒数之间的关系
例2 下列对摩尔(ml)的有关说法中错误的是
A.摩尔是一个单位而非物理量
B.摩尔既能用来计量纯净物,又能用来计量混合物
C.1ml任何气体所含气体的分子数目都相等
D.0.5ml氦约含有1.204×1024个电子
思维建模 考查物质中含有的各种粒子或微观结构的问题,一般来说先计算物质基本微粒中含有多少个需要计算的粒子或微观结构,再乘以该物质的物质的量,就可以计算出相应结果,稀有气体分子都是单原子分子。以物质的量为中心计算的思维模型:
【变式训练1·变载体】下列有关叙述正确的是()
A.1 ml任何物质都含有6.02×1023个分子
B.硫酸的摩尔质量为98 g
C.2 ml H2O是1 ml H2O摩尔质量的2倍
D.摩尔是物质的量的单位
【变式训练2·变考法】(24-25高三上·四川·联考)设为阿伏加德罗常数的值,部分含氮的物质有如图转化关系。下列叙述正确的是
A.常温常压下,含原子数为
B.固体含离子总数为
C.反应①中,生成还原产物,则需要分子数为
D.中含极性键总数为
【变式训练3·】【科学研究与学科知识结合】2015年10月,屠呦呦因发现青蒿素治疟疾的新疗法而获得诺贝尔生理学或医学奖,青蒿素的分子式为C15H22O5,其摩尔质量用M表示。下面关于青蒿素的说法正确的是
A.C15H22O5的摩尔质量为282g
B.1个C15H22O5分子的质量约为g
C.1mlC15H22O5完全燃烧生成22mlH2O
D.含有6.02×1023个碳原子的C15H22O5的物质的量为1ml
考点二 气体摩尔体积
知识点1 影响物质体积的因素
1.影响物质体积大小的因素
①粒子的 (物质的本性);②粒子 的大小(由温度与压强共同决定);③粒子的 (物质的量的大小)。
2.固体、液体的体积由①粒子的 和③粒子的 的多少决定,忽略②粒子 不计。
3.气体的体积由②粒子 和③粒子的 的大小决定,忽略①粒子的 不计。
知识点2 气体摩尔体积
(1)含义: 的气体所占的体积,符号为 ,标准状况下,Vm约为 。
(2)常用单位: 。
(3)数值:在标准状况下(指温度为 ,压强为 )约为 。
(4)基本关系式:
(5)影响因素:气体摩尔体积的数值不是固定不变的,它决定于气体所处的 和 。
得分速记 气体摩尔体积(22.4 L·ml-1)应用规范
(1)使用气体摩尔体积四注意
(2)用“22.4 L·ml-1”要“二看”
一看——物质状态,必有是气体,如标准状况下水、酒精、四氯化碳等为非气体物质;标准状况下不是气体而又常在题中出现的物质有:水、苯、SO3、HF、CCl4、己烷、CS2、CHCl3、Br2、乙醇等。
二看——外界条件,必须为标准状况,标准状况是0 ℃、1.01×105 Pa,不是常温、常压。非标准状况下,气体摩尔体积一般不是22.4 L·ml-1,但也可能是22.4 L·ml-1。
(3)气体摩尔体积的适用范围:气体摩尔体积的适用范围是气体,可以是单一气体,也可以是混合气体。需要注意的是混合气体中气体之间不能发生化学反应。
(4)物质的质量、物质的量一定时,所含微粒数与物质处于何种条件无关。如常温常压下32 g O2所含的原子数目是2NA。注意不要形成定势思维,看到“常温常压”就排除选项。
知识点3 阿伏加德罗定律及其推论
1.阿伏加德罗定律:在相同的温度和压强下, 的任何气体,含有 (或气体的物质的
量相同)。
得分速记 “三同”定“一同”,即同温、同压下,同体积的任何气体具有相同的分子数。
2.阿伏加德罗定律表达式: ,其中p代表压强,V代表体积,n代表物质的量,R是气体常数,T代表开尔文温度,为273+t。
3.阿伏加德罗定律的推论(以下用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质量,V为体积,T为热力学温度)
得分速记
1、记忆方法:三正比、二反比、一连比。
2、应用阿伏加德罗定律推论时可通过pV=nRT及n=eq \f(m,M)、ρ=eq \f(m,V)导出。
3、阿伏加德罗定律既适用于单一气体,也适用于混合气体,但对于固体和液体则不适用。
4、同温、同压、同体积和同分子数,共同存在,相互制约,只要“三同”成立,“第四同”必定成立。
5、对于同一种气体,当压强相同时,密度与温度成反比例关系。
考向1 考查气体摩尔体积与阿伏加德罗常数的正误判断
例1 下列说法正确的是
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 ml H2所占体积为11.2 L
③标准状况下,1 ml H2O的体积为22.4 L
④常温常压下,28 g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4 L·ml−1
⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤B.④⑥C.③④⑥D.①④⑥
思维建模 抓“两看”,突破气体与状况陷阱
一看“气体”是否处在“标准状况”。
二看“标准状况”下,物质是否为“气体”[如CCl4、CHCl3、CH2Cl2(注:CH3Cl为气体)、H2O、溴、SO3、己烷、苯、HF等在标准状况下均不为气体]。
【变式训练1·变载体】(2025·广东湛江·二模)“稀土之父”徐光宪先生缔造了稀土的“中国传奇”。稀土材料被广泛应用于汽车尾气的净化:,下列有关说法正确的是
A.含中子的数目为
B.常温常压下,和混合气体中含氧原子的数目为
C.含共价键的数目为
D.标准状况下含电子的数目为
【变式训练2·变考法】(2025·黑龙江·一模)催化氧化法将工业副产物HCl制成,实现了氯资源的再利用,下图为该法的一种催化机理。设为阿伏加德罗常数的值。下列说法正确的是
A.18g 中含有的质子数为10
B.过程Ⅴ,氧化1ml CuCl需氧气分子数为0.25
C.标准状况下,11.2L 溶于足量水中,转移电子数为0.5
D.标准状况下,等物质的量的与HCl所占的体积均为22.4L
【变式训练3·】【工业生产与学科知识结合】(2025·山西·二模)羟胺()作为一种有机合成的还原剂,传统工业合成途径为:
已知,25℃时,,,设表示阿伏加德罗常,数的值,下列说法错误的是
A.标准状况下,所含分子数为
B.若生成1 ml NO,则反应I中转移的电子数为
C.25℃时,同浓度水溶液的pH:
D.标准状况下,中硫原子上的孤电子对数为
考向2 考查阿伏加德罗定律及应用
例2(23-24高三上·重庆渝北·质量监测)下列说法正确的是
A.同温同压下的两种气体,只要所含微粒数目相等,则所占体积一定相等
B.质量相等,密度不相等的N2和C2H4分子数目一定相等
C.标准状况下11.2L甲烷和氨气混合物中氢原子数目为2NA
D.两个体积相同的容器,若气体物质的量相等,则两容器的压强一定相等
【变式训练1·变载体】(24-25高三上·河北石家庄·月考)已知标准状况下:①6.72 L NH3;②1.204×1023个H2S分子;③5.6 gCH4;④0.5mlHCl。下列关系正确的是
A.体积大小:④>③>①>②B.原子数目③>①>②>④
C.密度大小:④>②>③>①D.质量大小:④>③>②>①
【变式训练2·变考法】同温同压下,x g的甲气体与y g的乙气体占有相同的体积,则的值可以表示
A.甲与乙的相对分子质量之比
B.等质量的甲和乙的分子个数之比
C.同温同压下甲与乙的物质的量之比
D.同温同压下,等质量的甲与乙的压强之比
【工农业生产与学科知识结合】【变式训练3】(2024·海南·一模)是一种用途广泛的优良供氧剂,可用于鱼类养殖、农作物栽培、污水处理等多方面。某恒容密闭容器中发生反应:。下列说法正确的是
A.反应结束恢复到初始温度,气体压强一定变为原来的一半
B.常温常压下,和的摩尔体积相等
C.既是氧化产物,也是还原产物
D.转移1ml电子时,生成11.2L氧气
思维建模 应用阿伏加德罗定律及其推论要注意两个问题:
1.比例关系
同温同压:体积比=物质的量比(V1/V2=n1/n2)
同温同体积:压强比=物质的量比(p1/p2=n1/n2)
同温同压同质量:体积与摩尔质量成反比(V1/V2=M2/M1)
2.密度与摩尔质量
同温同压下,气体密度比等于摩尔质量比(ρ1/ρ2=M1/M2)
考向3 考查气体摩尔质量计算的常用方法
例3按要求解答问题:
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为_______,可能是_______气体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_______。
(3)CO和CO2的混合气体18 g,完全燃烧后测得CO2体积为11.2 L(标准状况),则
①混合气体在标准状况下的密度是_______g·L-1。
②混合气体的平均摩尔质量是_______ g·ml-1。
【变式训练1·变载体】某密闭容器中间有一可自由滑动的导热性隔板(厚度不计),当左侧充入,右侧充入一定量的时,隔板处于如图位置,下列说法正确的是
A.抽出隔板后混合气体平均摩尔质量为
B.若右侧再充入,隔板可以处于容器正中间
C.左侧与右侧的气体摩尔体积比为4:1
D.若左侧再充入,可以使得两侧气体密度相等
【变式训练2·变考法】组成的混合气体,其密度是相同条件下的密度的
A.0.913倍B.1.852倍C.0.873倍D.1.631倍
【变式训练3·】【生活与学科知识结合】打火机里装有液态的丙烷和丁烷。下列说法错误的是
A.打开打火机开关,分子间距变大
B.摩擦打火石,达到气体着火点
C.丙烷完全燃烧需要空气约为
D.若n(丙烷):n(丁烷),该混合物的摩尔质量为
思维建模 求气体摩尔质量M及相对分子质量的常用方法
(1)根据物质的质量(m)和物质的量(n):M=m/n。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(NA):M=NA·m/N。
(3)根据标准状况下气体的密度ρ:M=ρ×22.4 L·ml-1。
(4)根据气体的相对密度(D=ρ1/ρ2):M1/M2=D。
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:M=M1×a%+M2×b%+M3×c%……,a%、b%、c%……指混合物中各成分的物质的量分数(或体积分数)。
1.(2024·广东卷)设为阿伏加德罗常数的值。下列说法正确的是
A.中含有键的数目为
B.溶液中含的数目为
C.和的混合气体含有的分子数目为
D.与反应生成,转移电子数目为
2.(2024·浙江卷)利用可将废水中的转化为对环境无害的物质后排放。反应原理为:(未配平)。下列说法正确的是
A.X表示
B.可用替换
C.氧化剂与还原剂物质的量之比为
D.若生成标准状况下的气体,则反应转移的电子数为(表示阿伏加德罗常数的值)
3.(2023·重庆卷)已知反应:,为阿伏加德罗常数的值,若消耗(标准状况),下列叙述错误的是
A.转移的电子数为B.生成的质量为
C.生成的氧化产物分子数为D.生成的含有孤电子对数为
4.(2023·广东卷)设为阿伏加德罗常数的值。侯氏制碱法涉及和等物质。下列叙述正确的是
A.含有的共价键数目为
B.完全分解,得到的分子数目为
C.体积为的溶液中,数目为
D.和的混合物中含,则混合物中质子数为
5.(2023·浙江卷)NA为阿伏加德罗常数的值,下列说法正确的是
A.4.4gC2H4O中含有σ键数目最多为0.7NA
B.1.7gH2O2中含有氧原子数为0.2NA
C.向1L0.1ml/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA
6.(2023·全国甲卷卷)为阿伏加德罗常数的值。下列叙述正确的是
A.异丁烷分子中共价键的数目为
B.标准状况下,中电子的数目为
C.的溶液中的数目为
D.的溶液中的数目为
7.(2022·浙江卷)为阿伏加德罗常数的值,下列说法正确的是
A.中含有个阳离子
B.乙烷和丙烯的混合气体中所含碳氢键数为
C.含有中子数为
D.和于密闭容器中充分反应后,分子总数为
8.(2022·全国甲卷卷)为阿伏加德罗常数的值,下列说法正确的是
A.25℃,下,氢气中质子的数目为
B.溶液中,的数目为
C.苯甲酸完全燃烧,生成的数目为
D.电解熔融,阴极增重,外电路中通过电子的数目为
9.(2021·山东卷)X、Y均为短周期金属元素,同温同压下,0.1mlX的单质与足量稀盐酸反应,生成H2体积为V1L;0.1mlY的单质与足量稀硫酸反应,生成H2体积为V2L。下列说法错误的是
A.X、Y生成H2的物质的量之比一定为
B.X、Y消耗酸的物质的量之比一定为
C.产物中X、Y化合价之比一定为
D.由一定能确定产物中X、Y的化合价
10.(2020·北京卷)下列说法正确的是
A.同温同压下,O2和CO2的密度相同
B.质量相同的H2O和D2O(重水)所含的原子数相同
C.物质的量相同的CH3CH2OH和CH3OCH3所含共价键数相同
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同
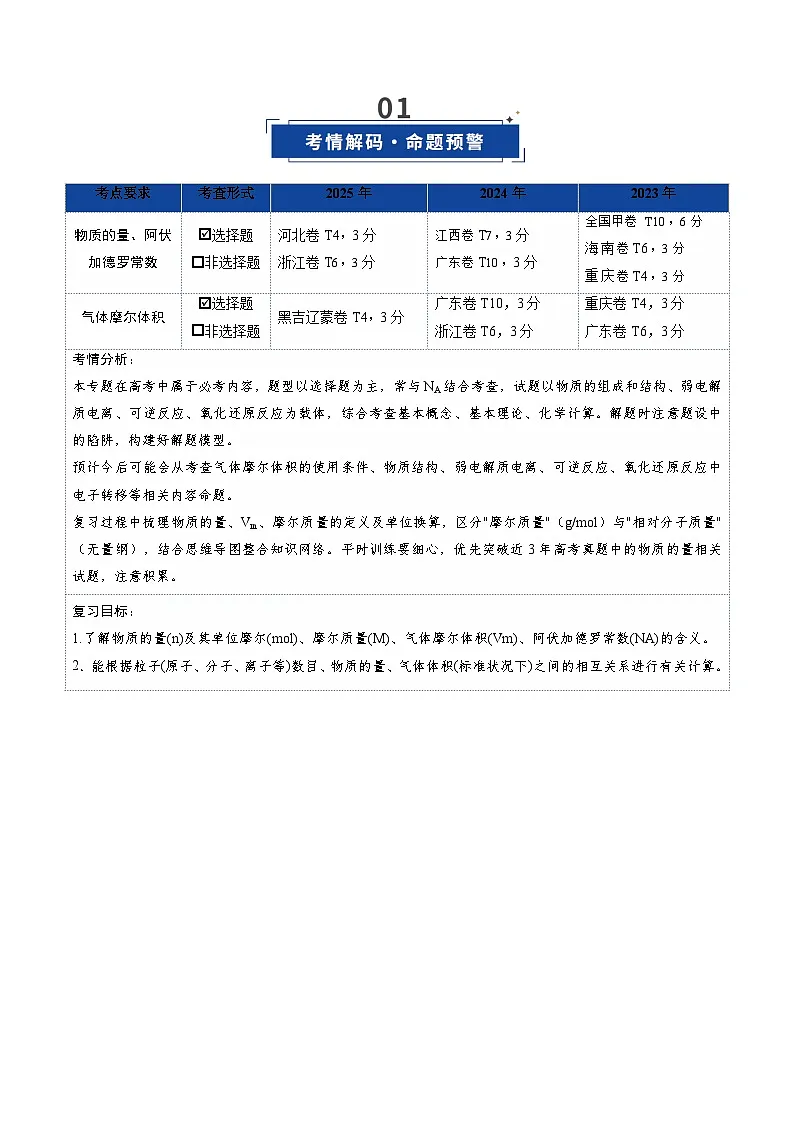
考点要求
考查形式
2025年
2024年
2023年
物质的量、阿伏加德罗常数
选择题
非选择题
河北卷T4,3分
浙江卷T6,3分
江西卷T7,3分
广东卷T10,3分
全国甲卷 T10,6分
海南卷T6,3分
重庆卷T4,3分
气体摩尔体积
选择题
非选择题
黑吉辽蒙卷T4,3分
广东卷T10,3分
浙江卷T6,3分
重庆卷T4,3分
广东卷T6,3分
考情分析:
本专题在高考中属于必考内容,题型以选择题为主,常与NA结合考查,试题以物质的组成和结构、弱电解质电离、可逆反应、氧化还原反应为载体,综合考查基本概念、基本理论、化学计算。解题时注意题设中的陷阱,构建好解题模型。
预计今后可能会从考查气体摩尔体积的使用条件、物质结构、弱电解质电离、可逆反应、氧化还原反应中电子转移等相关内容命题。
复习过程中梳理物质的量、Vm、摩尔质量的定义及单位换算,区分"摩尔质量"(g/ml)与"相对分子质量"(无量纲),结合思维导图整合知识网络。平时训练要细心,优先突破近3年高考真题中的物质的量相关试题,注意积累。
复习目标:
1.了解物质的量(n)及其单位摩尔(ml)、摩尔质量(M)、气体摩尔体积(Vm)、阿伏加德罗常数(NA)的含义。
2.能根据粒子(原子、分子、离子等)数目、物质的量、气体体积(标准状况下)之间的相互关系进行有关计算。
相同条件
结论
公式
语言叙述
T、p相同
同温、同压下,气体的体积与其 成正比
T、V相同
温度、体积相同的气体,其压强与其 成正比
T、p相同
同温、同压下,气体的密度与其 成正比
T、p、m相同
同温同压下,相同质量的任何气体的体积与它们的 成反比
T、V、m相同
同温同体积时,相同质量的任何气体的压强与它们的 成反比
T、p、V相同
同温同压下,同体积的任何气体的质量比等于它们的 之比,也等于它们的 之比
相关试卷
这是一份高考化学一轮复习-物质的量、气体摩尔体积(复习讲义)(全国通用)(原卷版),共13页。
这是一份高考化学一轮复习-物质的量、气体摩尔体积(专项训练)(全国通用)(原卷版),共9页。试卷主要包含了02) ×10-23 g,6 L,我国宇航员已经在太空泡茶了,下列说法正确的是等内容,欢迎下载使用。
这是一份物质的量、气体摩尔体积(讲义+练习、原卷版)-备战2026年高考化学一轮精讲精练复习讲义,共15页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




