

辽宁省葫芦岛市2025届高三下学期第一次模拟考试(一模)化学试卷(含答案解析)
展开 这是一份辽宁省葫芦岛市2025届高三下学期第一次模拟考试(一模)化学试卷(含答案解析),共20页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
一、单选题
1. 我国提出在2060年前完成“碳中和”的目标,下列有关低碳生活的说法不正确的是
2. 电石可通过如下反应制得:、。下列说法正确的是
3. 化学与生活经验密不可分。下列对生活经验的化学原理解释错误的是
4. 硒()在医药、催化、材料等领域有广泛应用,乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下图所示。关于硒及其化合物,下列说法不正确的是
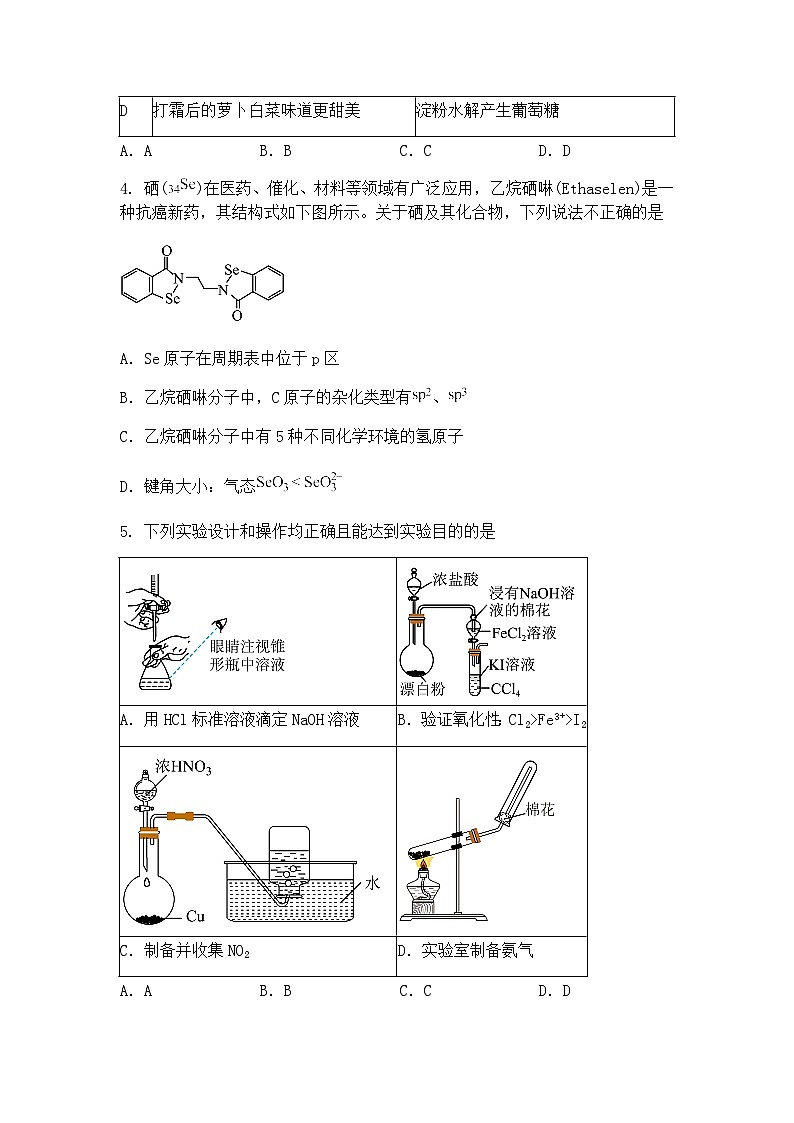
5. 下列实验设计和操作均正确且能达到实验目的的是
6. 可采用Deacn催化氧化法将工业副产物HCl制成,实现氯资源的再利用。反应的热化学方程式:。下图所示为该法的一种催化机理,下列说法不正确的是
7. 设NA为阿伏加德罗常数的值。下列说法正确的是
8. 由实验操作和现象得出的结论正确的是
9. 短周期主族元素M、N、X、Y、Z的原子序数依次增大,其中M的原子半径最小,基态N原子的s能级电子数是p能级电子数的两倍,X和Y位于同一主族,由上述五种元素形成的化合物可作离子导体,其结构如图所示。下列说法正确的是
10. 液氨的沸点-33.5℃,锂能与液氨反应,反应方程式为Li+nNH3=[e(NH3)n]¯+Li+,[e(NH3)n]¯是一种强还原剂,反应装置如图所示(夹持装置略)。下列说法不正确的是
11. 下列关于物质的结构或性质的描述解释都正确的是
12. 一种兼具合成功能的新型锂电池工作原理如图。电解质为含Li有机溶液。放电过程中产生(CF3SO2)2NLi,充电过程中电解LiCl产生Cl2下列说法正确的是
13. 利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略):
下列说法正确的是
14. Li、Fe、Se可形成一种新型超导材料,其晶胞结构如图所示。A点分数坐标为(1,1,1),下列叙述不正确的是
15. 常温下,Na2A溶液中H2A、HA-、A2-的物质的量分数与pH的关系如下图。
已知:A2-的物质的量分数 =
下列表述不正确的是
二、解答题
16. 硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为MnS及少量FeS)为原料制备硫酸锰的工艺流程如下:
①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②酸浸时,浸出液的pH与锰的浸出率关系如下图1所示。
③金属离子在水溶液中的平衡浓度与pH的关系如下图2所示(25℃),此实验条件下Mn2+开始沉淀的pH为7.54。
(1)Mn2+的价电子排布式为___________。
(2)传统工艺处理高硫锰矿时,若不经“混合焙烧”,而是直接用H2SO4浸出,其缺点为___________。
(3)实际生产中,酸浸时控制硫酸的量不宜过多,使pH在2左右。请结合图1和制备硫酸锰的流程,说明硫酸的量不宜过多的原因:___________。
(4)“中和除杂”时,应调节pH的范围为___________,其中除去Fe3+的离子方程式为___________。
(5)“氟化除杂”时,溶液中的Mg2+和Ca2+都沉淀完全时,则F-的最低浓度为___________[已知:Ksp(MgF2)=6.4×10-10;Ksp(CaF2)=3.6×10-12]。
(6)碳化结晶的离子方程式为___________。
17. 甲醇是主要的有机原料,常利用等进行制备。回答下列问题:
I.甲烷选择性氧化制备甲醇是一种原子利用率高的方法。
(1)反应①:;
反应②:。
已知键能数据为:,则键能为___________。
(2)已知大多数气体分子在催化剂表面的吸附过程是放热的。从反应速率的角度分析,通入后将体系温度维持的原因是___________(不考虑催化剂活性变化)。
Ⅱ.利用合成气制备甲醇。涉及的反应如下:
反应③:
反应④:
(3)在不同压强下、按照进行投料,在容器中发生上述2个反应,平衡时,和在含碳产物(即和)中物质的量分数及的转化率随温度的变化如下图,判断图中压强由大到小为___________。
(4)压强不变时,分析升温过程中转化率变化的原因___________。
(5)某恒温恒容体系,按进行实验,平衡时的物质的量分数为点M,此时转化率为,则该条件下反应④逆反应的平衡常数___________。
Ⅲ.科学家设计如图(串联光电催化反应池)减少排放并获取制备甲醇的。
(6)光催化电池中的半导体是在晶体硅中掺杂B原子和P原子实现的。p型半导体也称为空穴型半导体,n型半导体也称为电子型半导体。
据此,推测n型半导体掺杂的是___________(填元素符号)。
(7)产生的电极反应式为:___________。
18. CuCl在工业生产中有着重要应用。利用如图装置制备CuCl并测定产品纯度。
已知:ⅰ.CuCl是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
ⅱ.浓的溶液为无色,加水稀释即析出CuCl白色固体。
回答下列问题:
(1)①图中制取的反应中,氧化剂和还原剂的物质的量之比为___________。
②装置B中发生反应的仪器名称为___________。
③C中可选用试剂___________(填标号)。
A.溶液 B.饱和食盐水 C.浓 D.溶液
(2)制备CuCl:打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:①;②___________;③;观察到___________时停止反应。将B中溶液倾入盛有蒸馏水的烧杯中,立即得到白色CuCl沉淀,抽滤得CuCl粗品。
(3)洗涤CuCl:洗涤时最好用的乙醇洗涤滤饼,其目的是___________。
(4)CuCl纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用的溶液滴定至终点,再重复滴定2次,三次平均消耗溶液25.00mL(滴定过程中不反应)。
①产品中CuCl的质量分数为___________。
②下列操作会引起CuCl纯度测定值偏大的是___________。
A.锥形瓶水洗后误用稀硫酸润洗2-3次 B.配制标准溶液时仰视定容
C.盛装标准溶液的滴定管水洗后没有润洗
19. 有机物具有抗微生物、抗氧化等作用,其合成路线如下。
其中流程中为三苯基膦,为烃基。回答下列问题:
(1)中含氧官能团的名称为_______。
(2)的反应类型为_______,从整个流程看,设计的目的是_______。
(3)反应的化学方程式为_______。
(4)的结构简式为_______。
(5)分子中苯环上有3个取代基,且其中两个为的的同分异构体有_______种(不含立体异构),其中核磁共振氢谱有5组峰,且峰面积之比为的结构简式为_______。
(6)以、CH3CHO、为原料,制备的合成路线为,其中、的结构简式分别为_______、_______。
辽宁省葫芦岛市2025届高三下学期第一次模拟考试(一模)化学试卷
整体难度:适中
考试范围:化学与STSE、物质结构与性质、认识化学科学、化学反应原理、有机化学基础、常见无机物及其应用、化学实验基础
试卷题型
试卷难度
细目表分析
知识点分析
试题答案解析
第1题:
第2题:
第3题:
第4题:
第5题:
第6题:
第7题:
第8题:
第9题:
第10题:
第11题:
第12题:
第13题:
第14题:
第15题:
第16题:
第17题:
第18题:
第19题:
A.使用氢气等清洁能源代替传统能源有利于“碳中和”
B.推广使用煤液化技术,可减少二氧化碳的排放
C.低碳生活不意味着禁止使用所有燃料
D.在一定条件下将CO2还原为甲酸
A.基态的电子排布式:
B.的空间构型为四面体形
C.的电子式为
D.二氧化碳晶体属于共价晶体
选项
生活经验
化学原理
A
明矾水去除青铜器上的铜锈
盐类水解产生的酸与碱式盐反应
B
锡纸装食盐水让银饰由黑弈回银色
Sn未经过外电路直接把电子转移给Ag+
C
节日燃放的烟花在夜空下呈现多种色彩
原子核外电子跃迁会释放能量
D
打霜后的萝卜白菜味道更甜美
淀粉水解产生葡萄糖
A.A
B.B
C.C
D.D
A.Se原子在周期表中位于p区
B.乙烷硒啉分子中,C原子的杂化类型有、
C.乙烷硒啉分子中有5种不同化学环境的氢原子
D.键角大小:气态
A.用HCl标准溶液滴定NaOH溶液
B.验证氧化性:Cl2>Fe3+>I2
C.制备并收集NO2
D.实验室制备氨气
A.A
B.B
C.C
D.D
A.X为生成物,W为生成物
B.反应制得,放出热量57.2kJ
C.升高温度,HCl被氧化制的反应逆向移动
D.图中转化涉及的反应中有三个属于氧化还原反应
A.1ml[Cu(OH)4]2-中所含σ键数目为4NA
B.6gSiO2晶体中所含硅氧键数目为0.4NA
C.标准状况下,4.48L氯仿中所含氯原子数目为0.6NA
D.室温下,pH=13的KOH溶液中所含OH·数目为0.1NA
选项
实验操作和现象
结论
A
向0.1mL/LNaHSO3溶液中加入石蕊试液,变红色
Ka2(H2SO3)>Kh2()
B
向溶液中加入稀盐酸,产生使澄清石灰水变浑浊的气体
该溶液中含有或
C
将溴乙烷与NaOH的乙醇溶液加热产生的气体通入酸性KMnO4溶液,溶液褪色
溴乙烷与NaOH的乙醇溶液发生了消去反应
D
室温下,用pH试纸分别测定浓度为0.1ml/L的HClO溶液和0.1ml/L的HF溶液的pH,前者的pH大于后者
HClO的酸性小于HF
A.A
B.B
C.C
D.D
A.原子半径:Z>Y>X
B.简单氢化物的沸点:X>Z>N
C.未成对电子数:N>X>Z
D.该化合物中只有阳离子含有配位键
A.图中“试剂A”“试剂B”均可以为碱石灰
B.实验过程中可以通过调节分液漏斗的活塞,控制产生氨气的速率
C.图中“冷却溶剂”可以是冰水混合物
D.反应前锂片需打磨除去表面的氧化膜
A.H-O-H键角:H3O+邻羟基苯甲醛,是由于对羟基苯甲醛存在分子间氢键
C.电离能:P的第一电离能>S的第一电离能,是由于原子半径P>S
D.酸性:CH2ClCOOH>CH3COOH,是由于CH2ClCOOH的羧基中羟基极性更小
A.交换膜为阴离于交换膜
B.电解质溶液可替换为LiCl水溶液
C.理论上每生成1mlCl2,需消耗2mlLi
D.关闭S1、打开S2时总反应: 6Li+N2+4CF3SO2Cl=2(CF3SO2)2NLi+4LiCl
A.“氧化”时,发生的化学方程式:4Ag+4NaClO+2H2O=4AgCl↓+4NaOH+O2↑
B.氨水的作用是调节溶液的pH
C.若“还原”工序利用原电池来实现,则N2是正极产物
D.“还原”时,每生成1mlAg,理论上消耗0.5mlN2H4·H2O
A.该超导材料的化学式为LiFe2Se2
B.距离Se原子最近的Fe原子的个数为4
C.晶胞晶体密度为g/cm3
D.B点分数坐标为(,,)
A.0.1 ml·L-1 H2A溶液中,c(H2A) + c(HA-) + c(A2-) = 0.1 ml·L-1
B.在 0.1 ml·L-1 NaHA溶液中, c(HA-) > c(A2-) > c(H2A)
C.将等物质的量的NaHA、Na2A溶于水中,所得溶液的pH为4.2
D.M点对应的pH为2.7
题型
数量
单选题
15
解答题
4
难度
题数
容易
1
较易
1
适中
15
较难
1
困难
1
题号
难度系数
详细知识点
一、单选题
1
0.94
大气污染的治理原理及方法
2
0.85
电子排布式;价层电子对互斥理论的应用;常见分子晶体的结构;电子式
3
0.65
盐类水解在生活、生产中的应用;淀粉、纤维素的水解;焰色试验
4
0.65
杂化轨道理论;利用杂化轨道理论判断分子的空间构型;利用杂化轨道理论判断化学键杂化类型
5
0.65
氧化性、还原性强弱的比较;氨气的实验室制法;化学实验方案的设计与评价;酸碱中和滴定原理的应用
6
0.65
氧化还原反应定义、本质及特征;热化学方程式书写及正误判断;影响化学平衡的因素;温度对化学平衡移动的影响
7
0.65
22.4L/ml适用条件;根据n=m/M的相关计算;物质的量浓度的基础计算;阿伏加德罗常数的应用
8
0.65
盐类水解规律理解及应用;卤代烃的消去反应;化学实验方案的设计与评价
9
0.65
微粒半径大小的比较方法;根据原子结构进行元素种类推断;简单配合物的成键;氢键对物质性质的影响
10
0.4
氨气;氨气的实验室制法;常用仪器及使用方法;实验方案评价
11
0.65
电离能的概念及变化规律;元素性质与电负性的关系;利用杂化轨道理论判断化学键杂化类型;氢键对物质性质的影响
12
0.65
原电池、电解池综合考查;电解池电极反应式及化学方程式的书写;电解池有关计算
13
0.65
氧化还原反应方程式的书写与配平;原电池原理理解;物质分离、提纯综合应用
14
0.65
根据晶胞结构确定晶体化学式;晶胞的有关计算
15
0.65
弱电解质在水溶液中的电离平衡;盐类水解规律理解及应用
二、解答题
16
0.65
离子方程式的书写;溶度积常数相关计算;物质分离、提纯综合应用;常见无机物的制备
17
0.15
根据△H=反应物的键能之和-生成物的键能之和计算;化学平衡常数的计算;原电池电极反应式书写
18
0.65
离子方程式的书写;物质分离、提纯综合应用;实验方案评价;酸碱中和滴定原理的应用
19
0.65
同分异构体的数目的确定;合成路线的设计与优化;根据要求书写同分异构体
序号
知识点
对应题号
1
化学与STSE
1
2
物质结构与性质
2,4,9,11,14
3
认识化学科学
2,5,6,7,13,16,18
4
化学反应原理
3,5,6,8,12,13,15,16,17,18
5
有机化学基础
3,8,19
6
常见无机物及其应用
3,5,10
7
化学实验基础
5,8,10,13,16,18
相关试卷
这是一份辽宁省葫芦岛市2025届高三下学期第一次模拟考试(一模)化学试卷(含答案解析),共20页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
这是一份辽宁省葫芦岛市2025届高三下学期第一次模拟考试(一模)化学试卷,共8页。
这是一份2024届辽宁省葫芦岛市高三下学期一模化学试题(含解析),共24页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




