






2026年高考化学总复习备课课件 第4讲 新型化学电源
展开 这是一份2026年高考化学总复习备课课件 第4讲 新型化学电源,共60页。PPT课件主要包含了课时要求,CONTENTS,体验真题感悟高考,分层训练提升等级,类型四浓差电池,知识梳理,知能通关,锂电池,锂离子二次电池,离子交换膜等内容,欢迎下载使用。
1.知道常考新型化学电源的类型及考查方式;2.会分析常考新型化学电源的工作原理,能正确书写新型化学电源的电极反应式。
类型一 锂电池与锂离子电池
类型二 微生物燃料电池
类型三 物质转化循环型电池
锂电池是一类由金属锂或锂合金为负极材料、使用非水电解质溶液的电池。工作时金属锂失去电子被氧化为Li+,负极反应均为Li-e-===Li+,负极生成的Li+经过电解质定向移动到正极。
(1)锂离子电池基于电化学“嵌入/脱嵌”反应原理,替代了传统的“氧化—还原”原理;在两极形成的电势差的驱动下,Li+可以从电极材料提供的“空间”中“嵌入”或“脱嵌”。(2)锂离子电池充电时阴极反应式一般为C6+xLi++xe-===LixC6;放电时负极反应是充电时阴极反应的逆过程:LixC6-xe-===C6+xLi+。(3)锂离子电池的正极材料一般为含Li+的化合物,目前已商业化的正极材料有LiFePO4、LiCO2、LiMn2O4等。
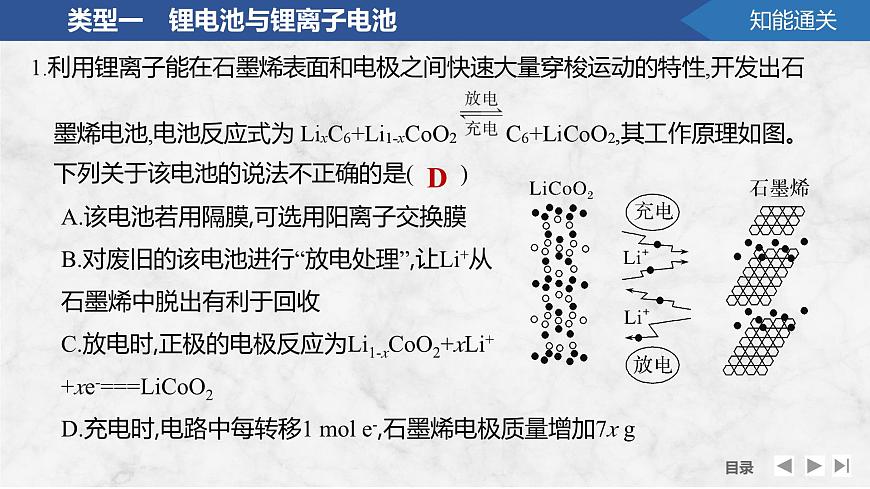
A.该电池若用隔膜,可选用阳离子交换膜B.对废旧的该电池进行“放电处理”,让Li+从石墨烯中脱出有利于回收C.放电时,正极的电极反应为Li1-xCO2+xLi++xe-===LiCO2D.充电时,电路中每转移1 ml e-,石墨烯电极质量增加7x g
解析 A.该电池通过锂离子定向移动导电,该电池若用隔膜,可选用阳离子交换膜,故A正确;B.石墨烯是负极,放电时,阳离子向正极移动,Li+从石墨烯中脱出有利于回收,故B正确;C.放电时,正极得电子发生还原反应,电极反应为Li1-xCO2+xLi+ +xe-===LiCO2,故C正确;D.充电时,电路中每转移1 ml e-,有1 ml Li+进入负极,石墨烯电极质量增加7 g,故D错误。
2.新型锂-空气电池具有巨大的应用前景。该电池放电时的工作原理如图所示,其中固体电解质只允许Li+通过。下列说法正确的是( )
A.有机电解液可以用水性电解液代替B.金属锂为负极,发生还原反应C.当外电路转移1 ml电子,理论上石墨烯电极消耗标准状况下11.2 L的O2D.放电时电池的总反应为4Li+O2+2H2O===4LiOH
解析 A.锂可以与水反应,故有机电解液不可以用水性电解液代替,A项错误;B.金属锂为负极,发生失电子的氧化反应,B项错误;C.当外电路转移1 ml 电子时,消耗0.25 ml的氧气,即理论上石墨烯电极消耗标准状况下5.6 L的O2,C项错误;D.该电池的负极反应为4Li-4e-===4Li+,正极反应为O2+4e-+2H2O===4OH-,将电极反应相加可得总反应的化学方程式4Li+O2+2H2O===4LiOH,D项正确。
微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置。其基本工作原理是在负极室厌氧环境下,有机物在微生物作用下分解并释放出电子和质子,电子依靠合适的电子传递介体在生物组分和负极之间进行有效传递,并通过外电路传递到正极形成电流,而质子通过质子交换膜传递到正极,氧化剂(如氧气)在正极得到电子被还原。
1.(2024·辽宁六校协作体开学考试)我国科学家设计的“海泥电池”既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理,其中微生物代谢产物显酸性,电池工作原理如图所示。下列说法错误的是( )
A.A电极为正极B.H+从海底沉积层通过交接面向海水层移动C.负极的电极反应式为CH2O-4e-+H2O===CO2+4H+D.高温下微生物蛋白质变性失活,故升温不一定能提高电池的效率
解析 由图可知,A极物质由氧气转化为水,化合价降低,所以A极是正极,B极是负极,据此解答。A.由分析可知,A极是正极,B极是负极,故A正确;B.质子带正电荷,放电时向正极移动,所以质子从海底沉积层通过交接面向海水层移动,故B正确; C.CH2O在微生物作用下与硫酸根离子反应生成CO2和HS-,并不是在负极的电极反应,负极上HS-失去电子发生氧化反应生成硫单质,电极反应式为HS--2e-=== S↓+H+,故C错误;D.微生物蛋白质高温条件下会失活,故升温不一定能提高电池的效率,故D正确。
1.题型背景循环电池是电化学储能领域的一个研究热点,它通过电池内部物质的循环使用来增加储能容量,增长使用寿命。2.题型分析根据物质转化,注意电极反应与电极区反应,元素化合价的变化或离子的移动(阳离子移向正极区域,阴离子移向负极区域)判断电池的正、负极,是分析该电池的关键。
1.(2025·临沂模拟)锌溴液流电池用溴化锌溶液作电解质溶液,并在电池间不断循环。下列有关说法不正确的是( )
A.充电时n接电源的负极,Zn2+通过阳离子交换膜由左侧流向右侧B.放电时每转移1 ml电子,负极区溶液质量不变C.充电时阴极的电极反应式为Zn2++2e-===ZnD.若将阳离子交换膜换成阴离子交换膜,放电时正、负极也随之改变
解析 充电时n接电源的负极,作电解池的阴极,Zn2+通过阳离子交换膜向阴极定向迁移,故由左侧流向右侧,A正确;放电时,负极Zn溶解生成Zn2+,Zn2+通过阳离子交换膜向正极定向迁移,故负极区溶液质量不变,B正确;若将阳离子交换膜换成阴离子交换膜,放电时正、负极不会改变,D错误。
2.(2025·八省联考四川卷)我国科学家发明了一种高储能、循环性能优良的水性电池,其工作示意图如下。
1.浓差电池的分析方法
在浓差电池中,为了限定某些离子的移动,常涉及离子交换膜。(1)离子交换膜的分类①阳离子交换膜,简称阳膜,只允许阳离子通过,不允许阴离子通过。②阴离子交换膜,简称阴膜,只允许阴离子通过,不允许阳离子通过。③质子交换膜,只允许H+通过,不允许其他阳离子和阴离子通过。④双极膜,又称双极性膜,是特种离子交换膜,它是由一张阳膜和一张阴膜复合制成的阴、阳复合膜。该膜的特点是在直流电场的作用下,阴、阳膜复合层间的H2O解离成OH-和H+分别通过阴、阳膜,作为H+和OH-的离子源。
(2)离子交换膜的作用①能将两极区隔离,阻止两极区产生的物质接触,防止发生化学反应。②能选择性地通过离子,起到平衡电荷、形成闭合回路的作用。(3)离子通过离子交换膜的定量关系①通过隔膜的离子带的电荷数等于电路中的电子转移数。②离子迁移:依据电荷守恒,通过隔膜的离子数不一定相等。
1.浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。下列有关该电池的说法错误的是( )
A.电池工作时,Li+通过离子导体移向X极区B.电流由Y极通过外电路流向X极C.正极发生的反应为2H++2e-===H2↑D.Y极每生成1 ml Cl2,X极区得到2 ml LiCl
解析 加入稀盐酸,X极上生成氢气,H+发生还原反应:2H++2e-===H2↑,X极为正极,Y极上Cl-发生氧化反应:2Cl--2e-===Cl2↑,Y极是负极,电池工作时,Li+向X极区移动,A、C正确;外电路中电流由正极X流向负极Y,B错误;Y极每生成1 ml Cl2,转移2 ml电子,有2 ml Li+向正极移动,则X极区得到2 ml LiCl,D正确。
2.构成原电池的条件有很多,当电解质中某离子的浓度越大时其氧化性或还原性越强。某化学实验小组用如图所示的装置实验,发现电流表指针发生偏转。
(1)电极A作 极,电极反应式为 。 (2)电极B作 极,电极反应式为 。 (3)硝酸根离子移向 (填“A”或“B”)极。 (4)由此得出的结论是,原电池反应发生的条件不仅与电极材料和电解质的性质有关,还与电解质的 有关。
Ag-e-===Ag+
Ag++e-===Ag
体验真题 感悟高考
1.(2024·江西卷)我国学者发明了一种新型多功能甲醛-硝酸盐电池,可同时处理废水中的甲醛和硝酸根离子(如图)。下列说法正确的是( )
2.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以Zn-TCPP(局部结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO4和KI混合液为电解质溶液。下列说法错误的是( )
4.(2023·全国新课标卷)一种以V2O5和Zn为电极、Zn(CF3SO3)2水溶液为电解质的电池,其示意图如下所示。放电时,Zn2+可插入V2O5层间形成ZnxV2O5·nH2O。下列说法错误的是( )
A.放电时V2O5为正极B.放电时Zn2+由负极向正极迁移C.充电总反应:xZn+V2O5+nH2O===ZnxV2O5·nH2OD.充电阳极反应:ZnxV2O5·nH2O-2xe-===xZn2++V2O5+nH2O
解析 由题中信息可知,该电池中Zn为负极、V2O5为正极,电池的总反应为xZn+V2O5+nH2O===ZnxV2O5·nH2O。A.由题信息可知,放电时,Zn2+可插入V2O5层间形成ZnxV2O5·nH2O,V2O5发生了还原反应,则放电时V2O5为正极,A说法正确; B.Zn为负极,放电时Zn失去电子变为Zn2+,阳离子向正极迁移,则放电时Zn2+由负极向正极迁移,B说法正确;C.电池在放电时的总反应为xZn+V2O5+nH2O=== ZnxV2O5·nH2O,则其在充电时的总反应为ZnxV2O5·nH2O===xZn+V2O5+nH2O,C说法不正确;D.充电阳极上ZnxV2O5·nH2O被氧化为V2O5,则阳极的电极反应为ZnxV2O5·nH2O-2xe-===xZn2++V2O5+nH2O,D说法正确。
5.(2022·全国乙卷)Li-O2电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来,科学家研究了一种光照充电Li-O2电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动阴极反应(Li++e-===Li)和阳极反应(Li2O2+2h+ ===2Li++O2)对电池进行充电。下列叙述错误的是( )
A.充电时,电池的总反应为Li2O2===2Li+O2B.充电效率与光照产生的电子和空穴量有关C.放电时,Li+从正极穿过离子交换膜向负极迁移D.放电时,正极发生反应:O2+2Li++2e-===Li2O2
解析 充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-===Li)和阳极反应(Li2O2+2h+===2Li++O2),则充电时总反应为Li2O2===2Li+O2,A正确;充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;放电时总反应为2Li+O2===Li2O2,则正极反应为O2+2Li++2e-===Li2O2,D正确。
分层训练 提升等级
基础落实选择题只有1个选项符合题意1.“自煮火锅”发热包的成分为碳酸钠、硅藻土、铁粉、铝粉、活性炭、焦炭粉、NaCl、生石灰,向发热包中加入冷水,可用来蒸煮食物。下列说法错误的是( )
A.活性炭作正极,正极上发生还原反应B.负极反应为Al-3e-+4OH-===[Al(OH)4]-C.Na+由活性炭区向铝粉表面区迁移D.硅藻土结构疏松,使各物质分散并混合均匀,充分接触
解析 发热包发热过程中有微小原电池形成,如铝粉和活性炭,在水溶液中活性炭作正极,O2得到电子发生还原反应,电极反应式为O2+2H2O+4e-===4OH-,A正确;铝粉作负极,失去电子发生氧化反应,电极反应式为Al-3e-+4OH-===[Al(OH)4]-,B正确;活性炭作正极,原电池中阳离子向正极移动,即Na+向活性炭区迁移,C错误;硅藻土结构疏松,可以使各物质分散并混合均匀,充分接触,D正确。
2.某锂离子电池的工作原理如图所示(a极材料为金属锂和石墨的复合材料),其电池总反应为Li+FePO4===LiFePO4。下列关于该电池的说法正确的是( )
A.a极为正极B.b极发生氧化反应C.Li+从a极室向b极室移动D.可以用稀硫酸作电解质溶液解析 a极上发生反应:Li-e-===Li+,a极为负极,A项错误;b极为正极,得电子,发生还原反应,B项错误;Li+透过隔膜从a极室进入b极室,C项正确;Li是活泼金属,能与稀硫酸反应,故不能用稀硫酸作电解质溶液,D项错误。
3.通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是( )
A.a为电池的正极,发生还原反应B.b极的电极反应为HCHO+H2O-4e-===CO2+4H+C.当电路中转移0.2 ml电子时,传感器内参加反应的HCHO为3.0 gD.传感器工作过程中,电解质溶液中硫酸的浓度减小
解析 氧气得电子,a为正极,发生还原反应,A正确;b极是负极,电极反应式为HCHO+H2O-4e-===CO2+4H+,B正确;负极电极反应式为HCHO+H2O-4e-=== CO2+4H+,当电路中转移0.2 ml电子时,反应的甲醛的物质的量为0.05 ml,质量0.05 ml×30 g·ml-1=1.5 g,C错误;传感器工作过程中,氧化还原反应生成水,电解质溶液中硫酸的浓度变小,D正确。
4.流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4=== CuSO4+PbSO4+2H2O。下列说法不正确的是( )
A.a为负极,b为正极B.该电池工作时PbO2电极附近溶液的pH增大C.a极的电极反应为Cu-2e-===Cu2+D.调节电解质溶液的方法是补充CuSO4溶液
A.放电时,电池的正极反应式为Li1-xMnO4+xLi++xe-===LiMnO4B.放电过程中,内电路电流方向是从负极到正极C.该电池也能在KOH溶液的环境中正常工作D.放电时Li+向电池正极方向定向迁移
解析 根据总反应式可知Li失去电子,电池负极反应式为Li-e-===Li+,由总反应式减去负极反应式可得放电时的正极反应式为Li1-xMnO4+xLi++xe-===LiMnO4,A正确;放电过程中,外电路电流方向是从正极到负极,内电路电流方向是从负极到正极,B正确;Li能与KOH溶液中的H2O反应,导致电池无法正常工作,C错误;Li+为阳离子,放电时Li+向电池正极方向定向迁移,D正确。
6.如图是常温钠离子全固态浓差电池工作示意图。正极材料为层状含钠过渡金属氧化物,负极为钠锡合金(Na15Sn4)。下列说法合理的是( )
A.该电池工作时不发生氧化还原反应B.放电时,负极的反应为Na15Sn4-15e-===15Na++4SnC.充电时,Na+会被吸附进入过渡金属氧化层D.充电时,b极接电源的正极,a极接电源的负极
解析 该电池放电时,是原电池工作原理,充电时,是电解池工作原理,无论是放电还是充电均发生了氧化还原反应,A错误;放电时,负极上钠锡合金(Na15Sn4)失电子发生氧化反应生成钠离子和锡,B正确;充电时,是电解池工作原理,Na+会向阴极移动,会脱离过渡金属氧化层,C错误;充电时,b极接电源的负极,a极接电源的正极,D错误。
7.为保护环境,降低城市水体污染,科学家利用城市废水中的尿素,设计尿素[CO(NH2)2]燃料电池,电池结构如图所示。下列说法不正确的是( )
A.电流从电极b通过外电路流向电极aB.电池工作时,正极区pH减小C.理论上每除去1 ml CO(NH2)2,电路中通过6 ml电子D.利用此法,也可除去废水中的甲醇等有机物
解析 电极b上氧气得电子生成水,为燃料电池的正极,电极a为负极,尿素失电子产生二氧化碳和氮气,电流从正极电极b流向负极电极a,A正确;正极发生反应O2+4e-+4H+===2H2O,故正极区溶液pH增大,B不正确;尿素失电子产生二氧化碳和氮气,N元素由-3价升高为0价,理论上每除去1 ml CO(NH2)2,电路中通过6 ml电子,C正确;利用此法,通过形成燃料电池的原理,也可除去废水中的甲醇等有机物,转化为二氧化碳和水,D正确。
8.中国科学院长春应用化学研究所模拟实验研究了低合金钢在海水中的局部腐蚀,研究发现缺氧的阳极区腐蚀速率比富氧介质(流动或充气)中钢的腐蚀速率大,验证了宏观氧浓差电池的存在。模拟氧浓差电池的简易装置如图,下列叙述错误的是( )
A.电子从M电极经导线流向N电极B.N电极的电极反应式为Fe-2e-===Fe2+C.正极区附近溶液的pH增大D.电路中转移0.01 ml电子时,有0.08 g O2在正极放电
9.(1)二氧化硫-空气质子交换膜燃料电池可以利用大气中所含SO2快速启动,其装置示意图如图:
(2)NH3-O2燃料电池的结构如图所示:①a极为电池的 (填“正”或“负”)极。 ②当生成1 ml N2时,电路中流过电子的物质的量为 。 解析 (2)①a极通入氨,是负极,b极通入氧气,是正极。②N的化合价由-3变成0,当生成1 ml N2时,转移6 ml电子。
A.充电时,化学能转变为电能B.放电时,K+向负极区迁移C.放电时,负极的电极反应为Al-3e-===Al3+D.充电时,阳极的电极反应为K0.5MnO2-xe-===K0.5-xMnO2+xK+
解析 充电时,应是电能转化为化学能,A项错误;由已知得,放电时,负极失去电子,故负极的电极反应为xKC8-xe-===8xC+xK+,C项错误。
11.一种双室微生物燃料电池污水净化系统原理如图所示,图中酸性污水中含有的有机化合物用C6H12O6表示。下列有关该电池的说法不正确的是( )
A.正极的电极反应式为[Fe(CN)6]3-+e-===[Fe(CN)6]4-B.电池的总反应为C6H12O6+24[Fe(CN)6]3-+6H2O===6CO2↑+24[Fe(CN)6]4-+24H+C.该“交换膜”可选用“质子交换膜”D.若将“K3[Fe(CN)6]溶液”改为“O2”,当有22.4 L O2参与反应时,理论上转移4 ml电子
解析 根据元素化合价的变化可知,[Fe(CN)6]3-生成[Fe(CN)6]4-的过程铁元素被还原,电极甲应为原电池的正极,所以正极的电极反应式为[Fe(CN)6]3-+e-===[Fe(CN)6]4-,A正确;C6H12O6被氧化生成H+和二氧化碳,[Fe(CN)6]3-被还原生成[Fe(CN)6]4-,则总反应为C6H12O6+24[Fe(CN)6]3-+6H2O===6CO2↑+24[Fe(CN)6]4-+24H+,B正确;原电池中阴离子有向负极移动的趋势,为防止[Fe(CN)6]3-移向负极,同时可以使负极产生的氢离子迁移到正极,可选用质子交换膜,C正确;氧气所处的压强和温度未知,无法计算氧气的物质的量,D错误。
12.(2024·云南玉溪模拟)如图是一种浓差电池,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性透过Cl-和Na+,在两电极板形成电势差,进而在外部产生电流。下列关于该电池的说法正确的是( )
A.a电极为电池的正极,电极反应式为2H2O+2e-===H2↑+2OH-B.C为阴离子交换膜,A为阳离子交换膜C.负极隔室的电中性溶液通过阳极表面的还原作用维持D.该电池的缺点是离子交换膜价格昂贵,电极产物也没有经济价值
解析 依据电子的移动方向判断b电极为负极,a电极为正极,氢离子得到电子在正极放电,电极反应式:2H2O+2e-===H2↑+2OH-,A正确;阳离子移向正极,Na+移向a电极,C为阳离子交换膜,Cl-移向b电极,A为阴离子交换膜,B错误;负极隔室中Cl-失去电子生成氯气,Na+通过C膜移入河水,维持负极隔室溶液的电中性,C错误;离子交换膜价格昂贵,但两极产物氢气、氯气是工业制盐酸等的原料,D错误。
13.(1)据文献报道,科学家利用氮化镓材料与铜组成如图所示的人工光合系统装置,成功地以CO2和H2O为原料合成了CH4。
①写出铜电极表面的电极反应式: 。 ②为提高该人工光合系统的工作效率,可向装置中加入少量 (填“盐酸”或“硫酸”)。
CO2+8e-+8H+===CH4+2H2O
解析 (1)原电池中电子从负极流向正极,根据图像中电子流向可知,铜电极为正极,正极上二氧化碳得电子生成甲烷,则铜电极表面的电极反应式为CO2+8e-+8H+===CH4+2H2O;负极水失电子产生氧气,电极反应式为4H2O-8e-===2O2+8H+。②电池中有质子交换膜,说明电解质溶液显酸性,必须加入酸,在光的作用下,盐酸中的Cl-易失电子产生Cl2,且盐酸易挥发,故应选硫酸。
(2)某负载二次镍氢电池放电时的工作原理如图所示,其中隔膜为 (填“阴”或“阳”)离子交换膜,负极的电极反应式为 。
LaNi5H6+6OH--6e-===LaNi5+6H2O
解析 (2)由图像可知,NiO(OH)为电池的正极,电极反应为NiO(OH)+e-===NiO+OH-, LaNi5H6为电池的负极,电极反应为LaNi5H6 +6OH--6e-===LaNi5+6H2O。根据上述分析, OH-需从正极区到负极区,因此隔膜为阴离子交换膜。
(3)利用反应NO2+NH3――→N2+H2O(未配平)消除烟气中NO2的简易装置如图所示,A、B两池溶液均为200 mL 0.01 ml·L-1 NaOH溶液,过程中溶液的体积和温度变化忽略不计。电极a的电极反应式为 。 解析 (3)根据化学方程式,NO2发生还原反应,为正极反应物,NH3发生氧化反应,为负极反应物,故电极a是负极,电极反应式为2NH3-6e-+6OH-===N2+6H2O。
2NH3-6e-+6OH-===N2+6H2O
(1)Y离子交换膜为 (填“阳”或“阴”)离子交换膜。 (2)Ⅲ室中除了O2→H2O,主要发生的反应还有 (用离子方程式表示)。(3)生成3.5 g N2,理论上需要消耗 g O2。
相关课件
这是一份2026年高考化学总复习备课课件 第4讲 新型化学电源,共60页。PPT课件主要包含了课时要求,CONTENTS,体验真题感悟高考,分层训练提升等级,类型四浓差电池,知识梳理,知能通关,锂电池,锂离子二次电池,离子交换膜等内容,欢迎下载使用。
这是一份2026届高考化学专题复习课件:新型化学电源,共41页。PPT课件主要包含了燃料电池工作原理,充电电池原理分析等内容,欢迎下载使用。
这是一份2024届高考化学一轮复习课件 第六章 化学反应与能量 热点强化练6 新型化学电源,文件包含热点强化练6新型化学电源pptx、热点强化练6新型化学电源docx等2份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




