
广东省惠州市第一中学2024-2025学年高二下学期3月月考化学试题(原卷版+解析版)
展开 这是一份广东省惠州市第一中学2024-2025学年高二下学期3月月考化学试题(原卷版+解析版),共33页。试卷主要包含了选择题,主观题等内容,欢迎下载使用。
考试时长:75分钟 满分100分
可能用到的相对原子质量:H1,C12,N14,O16,Fe56,Cu64,Zn65
一、选择题:本题共16小题,共44分。第1-10小题,每小题2分,第11-16小题,每小题4分。在每小题给出的四个选项中,只有一个选项是符合题目要求。
1. 二十大报告指出,我国在一些关键核心技术实现突破,载人航天、探月探火、深海深地探测、超级计算机、卫星导航等领域取得重大成果。下列成果中所用材料属于合金的是
A. AB. BC. CD. D
2. 下列有关化学用语说法错误的是
A. 键角:B. 基态的价电子排布式:
C. NaOH的电子式:D. 的VSEPR模型:
3. 是一种无色气体,且具有很强的稳定性,可用于灭火。下列有关说法中正确的是
A. 电负性:B. 分子是正四面体结构
C. 分子中硫原子周围无孤对电子D. 元素的第一电离能:
4. 锌电池取代目前广泛使用的蓄电池,它具有容量大、污染小的特点,其电池反应为:2Zn+O2═2ZnO,其原料为锌、空气和碱性电解质溶液,则下列叙述正确的是
A. 作原电池负极,其质量逐渐减小
B. 电路中转移电子时,理论上消耗
C. 负极的电极反应为:Zn+2OH--2e-═ZnO+H2O
D. 电池工作时溶液的pH升高
5. 下列各组粒子中所有原子都可能处于同一平面的是
A 、、B. 、、
C. 、、D. 、、
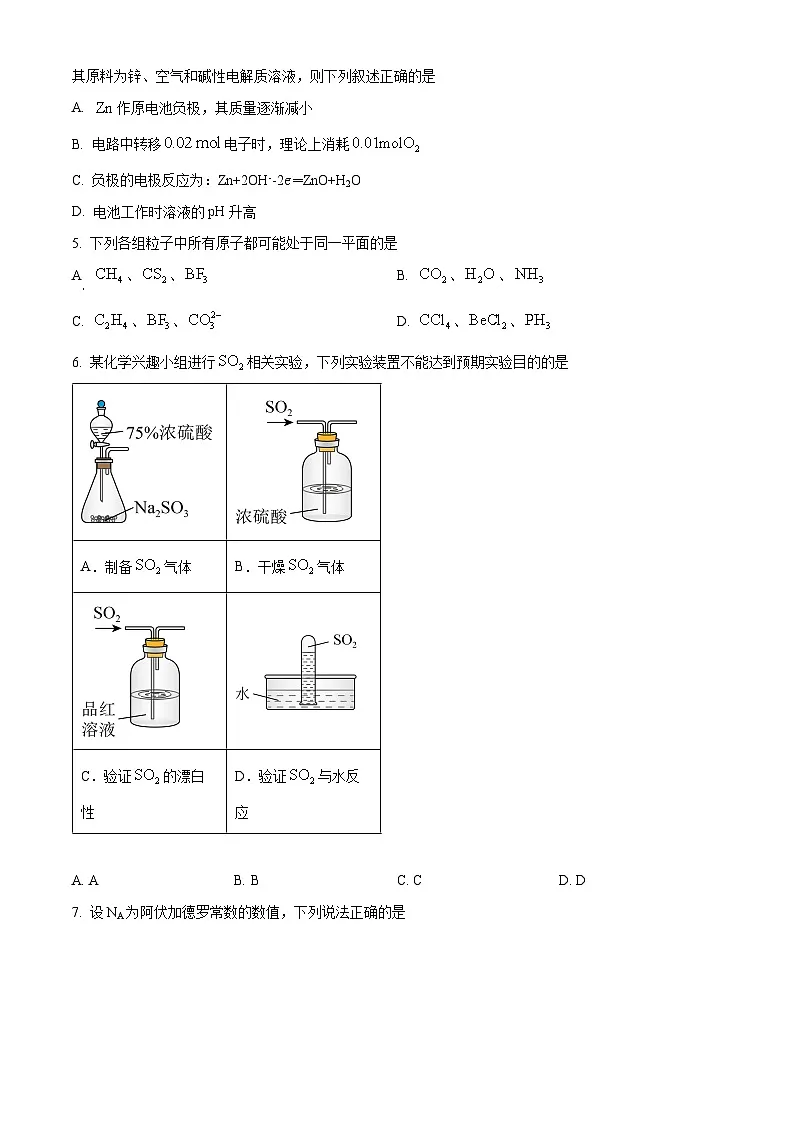
6. 某化学兴趣小组进行相关实验,下列实验装置不能达到预期实验目的的是
A. AB. BC. CD. D
7. 设NA为阿伏加德罗常数的数值,下列说法正确的是
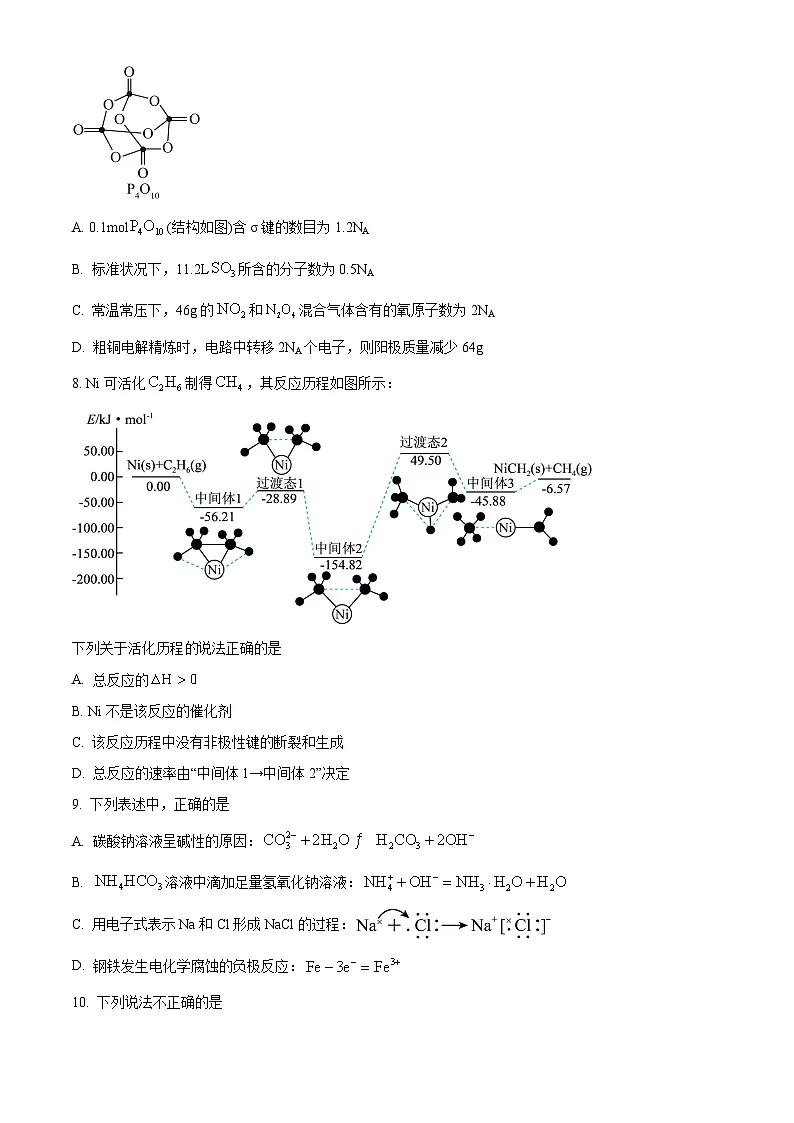
A. 0.1ml(结构如图)含σ键的数目为1.2NA
B. 标准状况下,11.2L所含的分子数为0.5NA
C. 常温常压下,46g的和混合气体含有的氧原子数为2NA
D. 粗铜电解精炼时,电路中转移2NA个电子,则阳极质量减少64g
8. Ni可活化制得,其反应历程如图所示:
下列关于活化历程说法正确的是
A. 总反应的
B. Ni不是该反应的催化剂
C. 该反应历程中没有非极性键的断裂和生成
D. 总反应的速率由“中间体1→中间体2”决定
9. 下列表述中,正确的是
A. 碳酸钠溶液呈碱性的原因:
B. 溶液中滴加足量氢氧化钠溶液:
C. 用电子式表示Na和Cl形成NaCl的过程:
D. 钢铁发生电化学腐蚀的负极反应:
10. 下列说法不正确的是
A. 用二硫化碳清洗做过硫升华实验的烧杯,其应用了“相似相溶”规律
B. 苹果酸中含有1个手性碳原子
C. HF、、均易溶于水的原因之一是与均能形成氢键
D. 以极性键结合的分子一定是极性分子
11. 某化学兴趣小组采用次氯酸钙与稀盐酸反应制取氯气,并探究了氯气的性质。实验装置如图所示,下列说法正确的是
A. g处变为橙色,h处变为黄色,说明氧化性;
B. 湿润的pH试纸先变红后褪色,说明Cl2有酸性和漂白性
C. f处变红,是因为被还原为,遇KSCN溶液变红
D. b试管中的离子方程式为:
12. 室温下,调节GaCl3溶液的pH,测定含Ga微粒的浓度分数随pH的变化情况如图所示:
已知:,下列说法错误的是
A. 的平衡常数的数量级为
B. pH=3时,
C. 向GaCl3溶液中加入NaOH溶液,会先生成沉淀,后沉淀溶解
D. 常温下,从GaCl3、FeCl3混合溶液中分离出GaCl3、FeCl3,可将溶液pH调节到10,过滤后,分别向滤液、滤渣中加入足量稀盐酸
13. 硫从远古时代就被人们知晓并使用.已知低浓度的溶液中存在X和Y两种结构.下列说法正确的是
A. X中的键角是
B. Y结构的空间构型为正四面体形
C. 基态硫原子中有16种空间运动状态的电子
D. X和Y通过氢键可形成结构
14. 常温下,用0.05NaOH溶液分别滴定10.00mL浓度均为0.10的()溶液和HCN()溶液,所得滴定曲线如图。下列说法正确的是
A. ①所标曲线为NaOH滴定HCN,两种弱酸滴定均可选用甲基橙作指示剂
B. 溶液中水的电离程度:
C. ③处溶液有
D. 点①和点②溶液混合后:
15. 短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是p能级电子数的两倍,Z和M位于同一主族,由上述五种元素形成的化合物可作离子导体,其结构如图所示。下列说法错误的是
A. 原子半径:M>Y>ZB. 简单氢化物的沸点:M>Z>Y
C. 同周期中第一电离能小于Z元素有五种D. YX4与的空间结构相同
16. 是重要的还原剂与储氢材料,在120℃下的干燥空气中相对稳定,其合成方法为:下列说法正确的是
A. 基态铝原子核外有13种不同空间运动状态的电子
B. 该反应可以在水溶液中进行
C. 与中Al原子杂化方式相同
D. 与其空间构型均为正方形
二、主观题
17. 黄铜矿(主要成分为)是生产铜、铁和硫酸的原料。回答下列问题:
(1)基态Cu原子价电子排布式为_______。
(2)从原子结构角度分析,第一电离能与的关系是:_____(填“>”““I2,但是无法说明Br2和I2的氧化性强弱关系,故A错误;
B.氯气与水反应生成HCl和次氯酸,HCl能使pH试纸变红,次氯酸有漂白性,所以后来pH试纸又褪色,但都不是氯气的性质,是氯气和水反应产物的性质,故B错误;
C.f处变红,是因为Fe2+被氯气氧化为Fe3+,Fe3+遇KSCN溶液变红,故C错误;
D.b试管中次氯酸根和氯离子在酸性条件下发生归中反应生成氯气,b中的离子方程式为:,故D正确;
故选D。
12. 室温下,调节GaCl3溶液的pH,测定含Ga微粒的浓度分数随pH的变化情况如图所示:
已知:,下列说法错误的是
A. 的平衡常数的数量级为
B. pH=3时,
C. 向GaCl3溶液中加入NaOH溶液,会先生成沉淀,后沉淀溶解
D. 常温下,从GaCl3、FeCl3混合溶液中分离出GaCl3、FeCl3,可将溶液pH调节到10,过滤后,分别向滤液、滤渣中加入足量稀盐酸
【答案】A
【解析】
【详解】A.根据题图中信息可知:时,,,室温下,则题给反应的平衡常数,数量级为,A说法错误;
B.根据题图中信息可判断,pH=3时,,B说法正确;
C.向GaCl3溶液中加入NaOH溶液,会先生成Ga(OH)3沉淀,后沉淀转化为,沉淀溶解,C说法正确;
D.根据计算,完全沉淀时(一般离子浓度小于等于,可认为沉淀完全),根据计算pH小于等于2.67,则将溶液pH调节到10,过滤后,滤渣为Fe(OH)3,GaCl3转化为进入滤液,分别向滤液、滤渣中加入稀盐酸后,Fe(OH)3、分别转化为FeCl3、GaCl3,D说法正确;
答案选A。
13. 硫从远古时代就被人们知晓并使用.已知低浓度的溶液中存在X和Y两种结构.下列说法正确的是
A. X中的键角是
B. Y结构空间构型为正四面体形
C. 基态硫原子中有16种空间运动状态的电子
D. X和Y通过氢键可形成结构
【答案】D
【解析】
【详解】A.X中,S原子有一对孤对电子,由于孤对电子对成键电子对的排斥,O−S−O的键角小于109°28′,A错误;
B.Y中S连接的4个原子不完全相同,故结构为四面体而非正四面体,B错误;
C.基态硫原子原子核外电子占据9个原子轨道,有9种空间运动状态的电子,C错误;
D.X中的H可以与Y中的O形成氢键,形成结构,D正确;
本题选D。
14. 常温下,用0.05NaOH溶液分别滴定10.00mL浓度均为0.10的()溶液和HCN()溶液,所得滴定曲线如图。下列说法正确的是
A. ①所标曲线为NaOH滴定HCN,两种弱酸滴定均可选用甲基橙作指示剂
B. 溶液中水的电离程度:
C. ③处溶液有
D. 点①和点②溶液混合后:
【答案】D
【解析】
【详解】A.两种酸浓度相同,由于HCN酸性更弱,故其pH更大,①所标曲线为NaOH滴定HCN,恰好反应生成NaCN,显碱性,由于甲基橙的变色范围是pH在3.1到4.4之间,因此滴定HCN时,不宜用甲基橙作为指示剂,A错误;
B.②处溶液,溶液呈酸性,醋酸电离为主,抑制水的电离,③处溶液,此时存在和少量的,④处为滴定终点,溶液中恰好生成,水解促进水的电离,因此溶液中水的电离程度:②ZB. 简单氢化物的沸点:M>Z>Y
C. 同周期中第一电离能小于Z的元素有五种D. YX4与的空间结构相同
【答案】B
【解析】
【分析】短周期主族元素X、Y、Z、M、N的原子序数依次增大,基态Y原子s能级电子数是p能级电子数的两倍,则Y为C元素;由阴阳离子的结构可知,X、Y、Z、M、N形成的共价键数目分别为1、4、4、6、1,Z和M位于同一主族,则阴阳离子中均存在配位键,X为H元素、Z为N元素、M为P元素、N为Cl元素。
【详解】A.原子的电子层数越多,原子的原子半径越大,同周期元素,从左到右原子半径依次减小,则原子半径的大小顺序为P>C>N,A正确;
B.M、Z、Y为磷、氮、碳元素,对应的简单氢化物为磷化氢、氨气、甲烷,氨气分子间存在氢键而沸点异常高,故简单氢化物的沸点高低为NH3>PH3>CH4,B错误;
C.同周期元素,从左到右第一电离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,元素的第一电离能大于相邻元素,则同周期中第一电离能小于氮的有锂、铍、硼、碳、氧,共5种元素,C正确;
D.YX4为CH4,为,中心原子均采用sp3杂化,无孤电子对,空间结构均为正四面体,D正确;
故选B。
16. 是重要的还原剂与储氢材料,在120℃下的干燥空气中相对稳定,其合成方法为:下列说法正确的是
A. 基态铝原子核外有13种不同空间运动状态的电子
B. 该反应可以在水溶液中进行
C. 与中Al原子杂化方式相同
D. 与其空间构型均为正方形
【答案】C
【解析】
【详解】A.基态铝原子核外电子排布式为1s22s22p63s23p1,共占据7个轨道,所以有7种不同空间运动状态的电子,A错误;
B.LiAlH4会和水反应,该反应不能在水溶液中进行,B错误;
C.与中心原子的价层电子对数均为4,Al原子杂化方式相同,均为sp3杂化,C正确;
D.与中心原子的价层电子对数均为4,不含孤电子对,空间构型均为正四面体形,D错误;
故选C。
二、主观题
17. 黄铜矿(主要成分为)是生产铜、铁和硫酸的原料。回答下列问题:
(1)基态Cu原子的价电子排布式为_______。
(2)从原子结构角度分析,第一电离能与的关系是:_____(填“>”“ (3) ①. sp2 ②. 10NA ③. ④. CH4
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




