

【2025届上海高三化学二模】2025届上海市闵行区高三化学二模试卷与答案
展开 这是一份【2025届上海高三化学二模】2025届上海市闵行区高三化学二模试卷与答案,共11页。试卷主要包含了本试卷共8页,含五个大题,25g/L,实验测得平均消耗标准溶液15等内容,欢迎下载使用。
(考试时间60分钟,满分100分)
特别提示:
1.本试卷共8页,含五个大题。答题时,考生务必按答题要求在答题纸规定位置上作答,在草稿纸、本试卷上答题一律无效。
2.选择类试题中,标注“不定项”的试题,每小题有12个正确选项,只有1个正确选项的,多选不给分,有2个正确选项的,漏选1个给一半分,错选不给分;未特别标注的试题,每小题只有1个正确选项。
本卷所用相对原子质量:H-1C-12O-16S-32Cu-64
一、含铜废料的处理和应用
电子制造,治金等行业易产生含铜废料,可将其转化为胆矾(),实现资源的回收和利用。
1.基态铜原子核外有________种能量不同的电子。
A.4B.7C.15D.29
2.根据基态原子的价电子排布,比较Cu与Fe的第二电离能:)________)。
A.>B.570°C)机制。具体反应如下:
1.铁元素位于元素周期表第________周期第________族。
2.计算的________________。
高炉气中存在反应:,勒夏特列通过研究该反应提出了化学平衡移动原理。
3.恒温恒容时,能说明上述反应达到平衡状态的是________(不定项)
A.与的物质的量之比为1:2
B.
C.和的浓度不再改变
D.混合气体的密度不再改变
4.同温度和压强下,上述反应达到平衡时和的体积分数变化如图所示。根据化学平衡移动原理,解释两种气体体积分数的变化趋势。
________________________________________
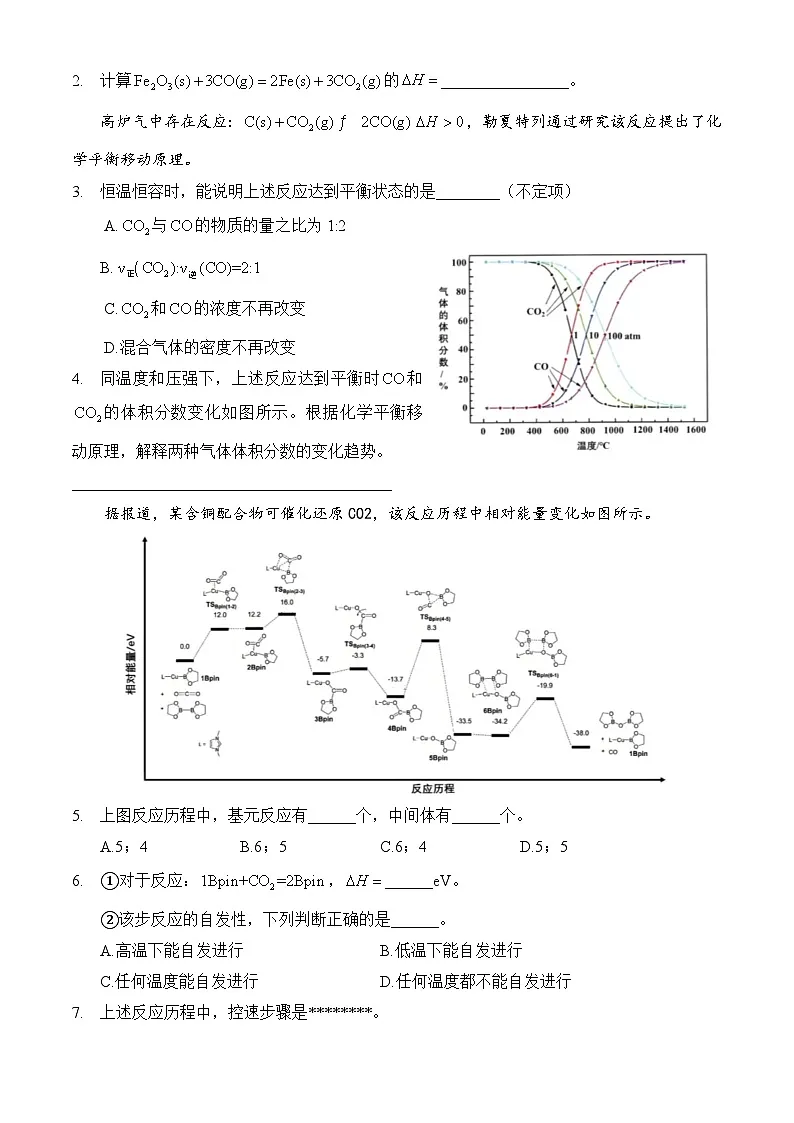
据报道,某含铜配合物可催化还原CO2,该反应历程中相对能量变化如图所示。
5.上图反应历程中,基元反应有______个,中间体有______个。
A.5;4B.6;5C.6;4D.5;5
6.①对于反应:,______eV。
②该步反应的自发性,下列判断正确的是______。
A.高温下能自发进行B.低温下能自发进行
C.任何温度能自发进行D.任何温度都不能自发进行
7.上述反应历程中,控速步骤是********。
A.1Bpin转化为2BpinB.2Bpin转化为3Bpin
C.4Bpin转化为5BpinD.6Bpin转化为最终产物
三、焦亚硫酸钠
焦亚硫酸钠()常被用作食品漂白剂、膨松剂和防腐剂等。该物质易溶于水,微溶于乙醇,其水解呈酸性,与强酸反应放出较多。
工业上可由的过饱和溶液经结晶脱水制备,原理为:
(Ⅰ)当一级反应釜中溶液pH在3~4时,停止通入,搅拌10分钟,复测pH在3~4范围内,得到的过饱和溶液。
(II)将一级反应釜降温至0℃,并搅拌1小时,析出,再经过滤、洗涤、干燥得到产品。
1.一级反应器中发生反应的化学方程式为________________________________。
2.简述二级反应器和三级反应器的作用________________________________________。
3.一级反应器析出的需要洗涤两次,选用试剂依次是①________、②________。
A.水B.无水乙醇C.饱和水溶液
4.在流程图中画出可循环利用物质的循环线。
5.长期放置的固体会部分被氧化为。检验样品是否变质的实验方法是________________________________________________________________。
6.作为食品添加剂,不得用于直接浸泡、熏蒸等非工艺必要接触。结合化学用语解释原因。
________________________________________________________________
焦亚硫酸钠作为食品添加剂,在葡萄酒中残留量一般不得超过0.25g/L(以计)。某小组检测葡萄酒样品中残留量,实验如下:取150mL葡萄酒样品,加稀硫酸酸化后加热,将产生气体通入足量双氧水中充分吸收,再除去过量的,冷却后滴加酚酞,最后用0.100ml/L标准溶液滴定上述吸收液。
已知:
7.滴定操作中用到的玻璃仪器有________。
A.玻璃棒B.滴定管C.烧杯D.容量瓶
8.下列操作会使得测定结果偏低的是________。(不定项)
A.酸化时,将稀硫酸改为稀盐酸B.加入稀硫酸后,未进行加热操作
C.当酚酞变色时,立刻停止滴定D.盛放标准溶液的滴定管未润洗
9.实验测得平均消耗标准溶液15.00mL,计算该样品中的残留量是否在安全范围内(残留量以计,写出计算过程)。
四、盐酸达泊西汀的合成
盐酸达泊西汀(G)是神经递质抑制类药物。G的一种合成路线如下图所示。
1.测定A中的官能团,最适合的仪器是________。
A.紫外可见光谱仪B.红外光谱仪
C.核磁共振氢谱仪D.原子发射光谱仪
2.B中含氧官能团的名称为________。
A.酮羰基B.羟基C.醚键D.醛基
3.反应③的反应类型为________。
A.取代反应B.加成反应C.消去反应D.还原反应
4.已知反应①的另一产物为(一元有机强酸)。
合成时,D与按物质的量之比约为1:2投料。简述的作用。
________________________________、________________________________________
5.试剂a和试剂b分别为________、________。
6.上述路线制备出的G为粗产品,进一步提纯的方法为________。
A.过滤B.重结晶C.蒸馏D.萃取分液
7.写出一种满足下列条件的1-萘酚()的同分异构体的结构简式。________
a.属于芳香族化合物,所有碳原子处于同一平面
b.常温下,与希夫试剂反应后溶液变为紫红色
c.核磁共振氢谱显示有4类化学环境不同的氢原子,且峰面积之比为3:2:2:1
8.已知:
结合上述路线中的信息,以、BrCH₂CH₂Br为原料,设计的合成路线。(其他试剂任选)
五、酒石酸
酒石酸()存在于多种植物中,常用作食品酸味剂、化工原料等。其结构简式和电离平衡常数见下表。
1.酒石酸分子含________个不对称碳原子。
A.0B.1C.2D.4
2.“三室两膜”电解法制备酒石酸(用表示)的工作原理如图所示。下列说法正确的是
A.交换膜A为负离子交换膜
B.阴极的电极反应式为
C.每生成15g,则阳极生成1.12L气体
D.电解过程不需再补充
3.酒石酸氢钾()俗称塔塔粉,常用于糕点制作、烘焙食品等。计算判断塔塔粉水溶液的酸碱性,并推测其在食品加工中的主要作用。
________________________________________________________________________
25°C时,0.100ml/L酒石酸水溶液中加入强酸或强碱调节pH时,各含碳微粒的物质的量分数(α)随pH变化如图所示。
4.当pH=6时,溶液中主要存在的含碳离子是________。
5.下列说法正确的是________。(不定项)
A.B曲线表示,溶液中始终存在:
B.曲线交点m和q对应的pH分别为2.98和4.38
C.pH从3到4时,水的电离程度先增大后减小
D.曲线A和C交点n对应的pH约为3.68
酒石酸和混合液可用于浸取废旧锂电池正极材料(Ni、C均为+3价)中的金属离子,实现回收再利用。
6.补全图中的物质,并配平下列浸取反应的化学方程式。
已知速率常数(k)与温度(T)关系为(其中E为活化能,近似为常数:)。在不同温度下测得浸取反应的速率常数,结果见下表。
7.如图所示,根据上述实验结果拟合出与的线性方程:,由此可知,浸出反应的活化能________。(保留小数点后两位)
参考答案
一、含铜废料的处理和应用(23分)
1.(2分)B
2.(2分)A
3.(2分)C
4.(2分)B
5.(3分)编号①的水分了与中心离子以配位键结合,编号②的水既有配位键又有氢键,编号③的水分子与、其他水分子均形成氢键,所以受热时胆矾脱去结晶水的温度不同。(合理即可)
6.(2分)22
7.(5分);
8.(5分)4;
二、高炉反应的研究(19分)
1.(2分)四8(或VIII)
2.(3分)-24.8
3.(2分)CD
4.(4分)当温度不变时,由于该反应是体积增大的反应,压强增大,平衡左移,所以体积分数减小,体积分数增大。
当压强不变时,由于该反应正反应吸热,温度升高,平衡右移,所以体积分数增大,体积分数减小。(合理即可)
5.(2分)B
6.(4分)①12.2②D
7.(2分)C
三、焦亚硫酸钠(22分)
1.(2分)
2.(2分)将过量的充分吸收,提高其利用率。(合理即可)
3.(2分)①C;B
4.(3分)
5.(3分)取少量样品于试管中,滴加足量稀盐酸无明显现象,再加入溶液,若产生白色沉淀,则证明有,样品被氧化,反之,则未变质。(合理即可)
6.(2分),,,在水中会生成有毒有害的。(合理即可)
7.(2分)B
8.(2分)BC
9.(4分)根据反应:
,,
可知:
,,
该葡萄酒中的含量为,
所以样品中的残留量不在安全范围内。(合理即可)
四、盐酸达泊西汀的合成(20分)
1.(2分)B
2.(2分)B
3.(2分)A
4.(2分)作反应试剂;作碱中和甲磺酸,提高E的产率。(合理即可)
5.(4分);(合理即可)
6.(2分)B
7.(2分)(合理即可)
8.(4分,合理即可)
五、酒石酸(16分)
1.(2分)C
2.(2分)B
3.(3分)由于,水解的平衡常数,说明的电离程度大于其水解程度,则塔塔粉水溶液显酸性,推测塔塔粉的主要作用是与食品中的碱性物质反应,调节酸碱度。(合理即可)
4.(2分)B
5.(2分)BD
6.(3分)
7.(2分)53.86选项
A
B
C
D
杂化轨道类型
sp2
sp2
sp3
sp3
空间结构
空间结构角形
平面三角形
正四面体形
平面四边形
结构简式
温度/°C
速率常数
40
0.0031
50
0.0055
60
0.0096
70
0.0171
80
0.0323
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)




