






2025年盐城中考化学(人教版)总复习《第二部分+专题28化学计算》课件
展开 这是一份2025年盐城中考化学(人教版)总复习《第二部分+专题28化学计算》课件,共47页。PPT课件主要包含了复习目标,知识梳理,一有关化学式的计算,书写格式,在NH4NO3中,35%,其他类型的计算,质量分数,x064g,x20t等内容,欢迎下载使用。
3.能根据化学方程式进行简单的计算,如已知反应物的质量求生成物的质量,或已知生成物的质量求反应物的质量。
1.根据化学式计算相对分子质量、各元素的质量比以及某元素的质量分数。
2.理解溶液中溶质质量分数的概念,并能进行有关计算,包括溶液的配制、稀释等问题。
4.运用质量守恒定律、元素守恒、电荷守恒等守恒思想进行计算,简化计算过程,提高解题效率。如在化学反应中,反应前后元素的种类和质量不变,利用这一原理可以解决一些复杂的混合物计算问题。
1.相对分子质量的计算
(1)、概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。(符号为Mr).
①、是化学式中各原子的相对原子质量的总和.
②、是分子的相对质量,不是实际质量.
③、它的单位也是 1.
(2)、计算物质的相对分子质量(Mr)
O2的相对分子质量= 16×2=32
(NH4)2CO3的相对分子质量
H2O的相对分子质量=1×2 + 16=18
计算: O2、H2O、(NH4)2CO3的相对分子质量
=(14+1×4)×2 + 12 + 16 ×3
计算硝酸铵中各元素的质量比
m(N) : m(H) : m( O ) = 14×2 : 1×4 : 16×3
= 28 : 4 : 48
= 7 : 1 : 12
2、计算物质组成元素的质量比
元素质量比=(相对原子质量×原子个数)之比
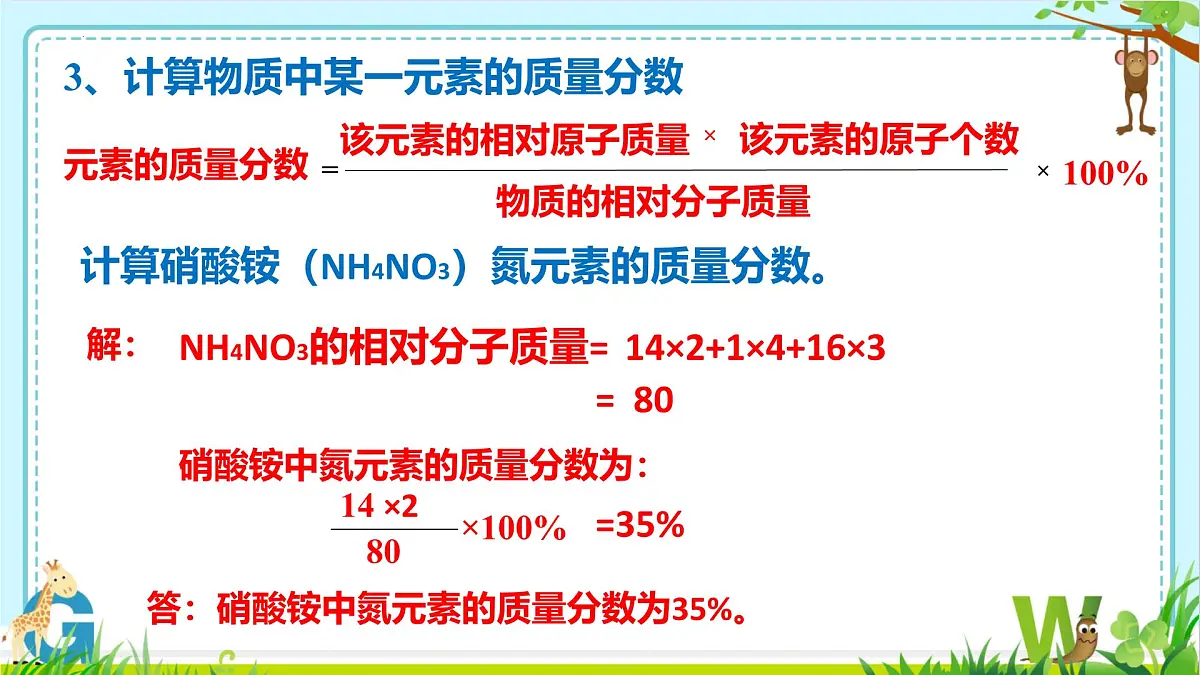
3、计算物质中某一元素的质量分数
计算硝酸铵(NH4NO3)氮元素的质量分数。
NH4NO3的相对分子质量=
14×2+1×4+16×3
硝酸铵中氮元素的质量分数为:
答:硝酸铵中氮元素的质量分数为35%。
计算依据:质量守恒定律,参加化学反应和反应生成的各物质的质量比是一个定值。
1. 利用化学方程式的简单计算的依据
(1).化学方程式中物质的实际质量之比等于相对质量之比。
(2).化学方程式中各反应物、生成物之间的质量比为定值。
(3).在化学方程式中各物质的质量比在数值上等于各物质的相对分子质量与其化学计量数的乘积之比。
二.有关化学方程式的计算
2KMnO4 K2MnO4+MnO2+O2↑
例1:加热分解6.32 g高锰酸钾,可以得到多少克氧气?
解:设加热分解6.32g高锰酸钾,可以得到氧气的质量为x。
答:加热分解6.32 g高锰酸钾可以得到0.64 g氧气。
316 32
6.32g x
2. 利用化学方程式的简单计算的基本思路
依据化学方程式进行计算的基本思路
首先,要搞清楚问题是什么,即题目中要求的未知量是么?
其次,要弄清楚化学反应的原理,写出化学方程式,并明确题目中哪些已知量是有用的。
第三,根据化学方程式中反应物与生成物间的定量关系,确定已知量与未知量之间的关系;
第四,将上述关系列成比例式求解;最后,检查计算过程和结果无误后,简明地写出答案。
例2:工业上高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳,如果要制取11.2 t氧化钙,需要碳酸钙多少吨?
解:设需要碳酸钙的质量为x。
CaCO3 CaO+CO2↑
答:需要碳酸钙20t。
3. 利用化学方程式的简单计算的步骤和书写格式
⑶标出相关物质的化学计量数与相对分子质量乘积、已知量、未知量
数据与物质的化学式要对齐,已知量要带单位进行运算
4. 利用化学方程式的简单计算的步骤和注意事项
千万别丢下我啊! 谢谢噢!
溶质质量 = 溶液质量× 溶质质量分数
(1)、定义:溶质的质量与溶液的质量之比。(通常以百分数表示)
1.溶液中溶质质量分数
(3). 注意:①溶质的质量:溶解的那部分溶质,未溶解的不计。②溶液的质量 = 溶质的质量 + 溶剂的质量。 (必须分清溶质、溶剂与溶液)。 ③计算时上下质量单位要统一。④不要忘记X100%,最后得到百分数。⑤物质的质量分数要在不超过其最大溶解量的范围时才有意义。
在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
答: 配制150kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
请问溶质的质量分数与溶解度有什么区别?
溶质的质量分数36% 是指: 100克溶液中含有36克溶质。 T℃时溶解度36克是指: 在T ℃ 时,100克水最多溶解该溶质36克。
3、溶质质量分数与溶解度的比较
某温度下的饱和溶液:质量分数=
化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的 硫酸溶液需要多少克水?
解:设稀释后溶液的质量为x
50g 98% = X 20%
需要水的质量= 245 g– 50g = 195g
稀释前溶质质量= M浓溶液×C%浓溶液
稀释后溶质质量= M稀溶液×C%稀溶液
(1)、稀释前溶质质量如何表示?
(2)、稀释后溶质质量如何表示?
M浓×C%浓= M稀×C%稀
水的质量= M稀- M浓
稀释前溶质质量= 稀释后溶质质量
= (M浓+M水) × C%稀
另解:把50g质量分数为98%的浓硫酸稀释成质量分数为20%的稀硫酸,需要加水多少克?
50g×98% =(50g + x)×20%
解:设加水的质量为x。
例4:100g 9.8%硫酸跟多少克锌反应?同时生成多少克氢气?
解:100g的9.8%硫酸中含纯硫酸的质量为:
100g×9.8%=9.8g
设参加反应的锌质量为X ,生成氢气的质量为Y
Zn + H2SO4 = ZnSO4 + H2
65 98 2
X 9.8g Y
X=6.5g Y=0.2g
溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。
4. 溶质的质量分数与化学方程式的综合计算
(1).在化学反应中没有气体或沉淀所得溶液质量“只加不减”①根据质量守恒定律:反应后溶液的质量=反应前所有溶液的质量+被溶解固体的质量 ②反应后溶液的质量=反应后溶液中溶质的质量+所有水的质量
(2).生成物中有气体或沉淀生成:所得溶液质量“有加有减”①根据质量守恒定律 反应后溶液的质量=反应前所有溶液的质量+被溶解固体的质量—气体或沉淀的质量②反应后溶液的质量=反应后溶液中溶质的质量+所有水的质量(不减气体或沉淀)
例1.(2024江苏无锡)维生素C(C6H8O2)中碳、氢、氧元素的质量比为( )A. 3:4:1 B. 9:1:4 C. 9:2:4 D. 6:8:2
【解析】维生素C中碳、氢、氧元素的质量比为(12×6):(1×8):(16×2)=72:8:32 = 9:1:4,故答案选B。
例2.(2024临沂)“临沂炒鸡”是临沂一张靓丽的美食名片,其特色是麻辣鲜香。在炒鸡过程中,鸡肉中的部分脂肪会转化为脂肪酸和甘油等。已知甘油的化学式为C3H8O3,则关于甘油的说法正确的是( )A. 甘油是由碳、氢、氧三种原子构成的B. 甘油中碳、氢、氧元素的质量比为3:8:3C. 甘油的相对分子质量为92gD. 甘油中氢元素的质量分数最小
【解析】甘油是由甘油分子构成的,A错误;甘油中碳、氢、氧元素的质量比为(12×3):(1×8):(16×3)=9:2:12,B错误;相对分子质量的单位是“1”,不是“g”,C错误;由B选项可知氢元素质量分数最小,D正确。
例3.(2024广西)已知1g氮元素大致相当于6.25g蛋白质。若某奶粉中蛋白质的含量为20%,则100g该奶粉中氮元素的质量约为( )A. 1.6g B. 3.2g C. 4.8g D. 6.4g
【解析】100g该奶粉中蛋白质的质量为100g\times20\% = 20g,因为1g氮元素大致相当于6.25g蛋白质,所以20g蛋白质中氮元素的质量为20\div6.25 = 3.2g,故答案选B。
例4.(2024黑龙江牡丹江)将6g某合金样品放入烧杯中,向其中加入100g稀盐酸恰好完全反应,烧杯中剩余物的总质量是105.8g,该合金样品可能是( )A. Cu,Zn合金 B. Fe,C合金 C. Mg,Al合金 D. Mg,Cu,Al合金
【解析】根据质量守恒定律,生成氢气的质量为6g + 100g - 105.8g = 0.2g。铜与稀盐酸不反应,锌、铁、镁、铝与稀盐酸反应的化学方程式分别为Zn + 2HCl = ZnCl2+H2↑、Fe + 2HCl = FeCl2+H2↑、Mg + 2HCl = MgCl2+H2↑、2Al + 6HCl = 2AlCl3+3H2↑。生成0.2g氢气分别需要锌6.5g、铁5.6g、镁2.4g、铝1.8g。6g合金样品与稀盐酸反应生成0.2g氢气,说明合金中一定含有不与稀盐酸反应的铜或碳,且含有能与稀盐酸反应产生氢气的金属,故答案选D。
例5.苹果酸(C4H6O5)是一种白色晶体,有较强的吸湿性,易溶于水、乙醇,有特殊愉快的酸味,主要用于食品和医药行业。下列关于苹果酸的说法中正确的是( )A.苹果酸中有 4 个碳原子、6 个氢原子、5 个氧原子B.苹果酸中氧元素的质量分数最大C.苹果酸中 C、H、O 三种元素质量比为:4∶6∶5D.苹果酸的相对分子质量为 134g
【解析】A、苹果酸是由分子构成的,每个苹果酸分子中含有4个碳原子、6个氢原子、5个氧原子,选项说法错误;B、根据苹果酸的化学式为C4H6O5,碳、氢、氧三种元素质量比为(12×4):(1×6):(16×5)═24:3:40,可见其中氧元素的质量分数最大,选项说法正确;C、根据苹果酸的化学式为C4H6O5,碳、氢、氧三种元素质量比为(12×4):(1×6):(16×5)═24:3:40,选项说法错误;D、相对分子质量的单位不是“g”而是“1”,通常省略不写,选项说法错误。故选B。
例6.某化学反应的微观示意图如图所示。下列判断不正确的是( )A. 该反应中元素的化合价均发生了改变 B. 生成物乙是单质C. 该化学反应中甲、丙、乙的分子个数比为2∶1∶3 D. 根据质量守恒定律可推知,1个乙分子中含有6个A原子
【解析】单质中元素的化合价为零,化合物中元素的化合价代数和为零;由图可知,反应前AB为化合物,反应后AB以单质存在,该反应中元素的化合价均发生了改变;所以据质量守恒定律可知,化学反应前后原子的种类、个数不变。所以生成物乙的一个分子由两个A原子构成,所以乙为同种元素组成的单质。该化学反应中甲、丙、乙的分子个数比为2∶1∶3;故答案为:D。
例7.黑火药是中国四大发明之一,其主要反应为2KNO3+3C+SK₂S+X↑+3CO₂↑,下列说法正确的是( )A.X的化学式为2N B.该反应属于分解反应C.该反应前后各元素的化合价均未改变 D.参加反应的碳、硫质量比为9:8
【解析】A、由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前钾、氮、氧、碳、硫原子个数分别为2、2、6、3、1,反应后的生成物中钾、氮、氧、碳、硫原子个数分别为2、0、6、3、1,根据反应前后原子种类、数目不变,则每个X分子由2个氮原子构成,则物质X的化学式为N2,故选项说法错误。B、该反应的反应物是三种,不符合“一变多”的形式,不属于分解反应,故选项说法错误。C、反应物和生成物是均含有单质,一定有元素的化合价发生改变,故选项说法错误。 D、参加反应的碳、硫质量比为(12x3): 32=9:8,故选项说法正确。故选:D
例8.在化学反应 A+B2═2C 中,已知 20g A 和足量 B2 充分反应后,生成 30g C.已知 B 的相对原子质量为 16,则 C 的相对原子质量是( )A.20 B.32 C.48 D.96
【解析】根据质量守恒定律可知 20gA 和 B2 充分反应生成 30gC 时参加反应的 B2 质量应为 30g﹣20g=10g;设 C 的相对分子质量是 x,则A+B2=2C 32 2x 10g 30g x=48故选:C。
例9.将20 g H2、O2的混合气体点燃,完全反应后生成18 g水,则原混合物中H2和O2的质量比可能是( )A. 2:1 B. 1:8 C. 1:10 D. 1:4
【解析】H2与O2反应生成18 g水,则参加反应的H2、O2质量分别为2 g、16 g,原混合气体质量为20 g,剩余的2 g可能是H2或O2,则原混合物中H2和O2的质量比可能为4 g:16 g=1:4(H2过量)或2 g:18 g=1:9(氧气过量)。
【解析】设所得硫酸溶液中溶质的质量分数是x,根据溶液稀释前后,溶质的质量不变,则100g×98%=(900g+100g)×x x=9.8%. 故选A
例12.将100g 98%的浓硫酸注入900g水中,所得稀硫酸中溶质的质量分数为( )A. 9.8% B. 10.0% C. 10.9% D. 11.1%
例13. t℃时,A物质的饱和溶液中A的质量分数为15%,B物质的溶解度是25g,C物质的10g饱和溶液蒸干后可得1.5gC。若取等质量的3种物质的饱和溶液,则3种溶液中所含溶质的质量大小顺序是( )A. A>C>B B. C>A>B C. B>C=A D. A>B>C
【解析】A物质的饱和溶液中A的质量分数为15%B物质的溶解度是25g,则B物质的饱和溶液的溶质质量分数为×100%=20%C物质的饱和溶液的溶质质量分数为 ×100%=15%所以取等质量的3种物质的饱和溶液,所含溶质的质量大小顺序是B>C=A故选C。
例14.如图为甲、乙两物质的溶解度曲线,下列说法正确的是( )A. 甲、乙两物质均属于难溶物质B. 甲物质的溶解度大于乙物质的溶解度C. t1℃时,甲、乙两物质饱和溶液的溶质质量分数相等D. t2℃时,甲物质饱和溶液的溶质质量分数为50%
【解析】A、通过分析溶解度曲线可知,在10℃时,甲、乙物质的溶解度大于10g,所以甲、乙两物质均属于易溶物质,故A错误;B、在比较物质的溶解度时,需要指明温度,故B错误;C、t1℃时,甲、乙两物质的溶解度相等,所以饱和溶液的溶质质量分数相等,故C正确;D、t2℃时,甲的溶解度是50g,所以甲饱和溶液的溶质质量分数= ,故D错误。故选C
【解析】A、从溶液c 和溶液d可以看出,降低温度则溶液中会析出晶体,说明该物质的溶解度随温度的升高而增大,正确;B、溶液b中加入20g固体得到的溶液c中没有未溶解的固体,说明加入的物质全部溶解,故溶液b一定是不饱和溶液,正确;C、溶液d变成溶液e的过程中没有发生化学变化,说明溶液d中的固体除掉,可能是经过过滤除去,溶液d中溶质质量等于溶液e中的溶质质量,错误;D、若是溶液d中的固体是经过过滤除去,则溶液d和溶液e的溶质质量分数可能相同,正确。故选C。
例15.小张同学用某固体物质进行如图的实验,根据实验判断下列说法不正确的是( )A. 该固体物质的溶解度随温度的升高而增大B. 溶液b一定是不饱和溶液C. 溶液d中溶质质量一定大于溶液e中的溶质质量D. 溶液d和溶液e的溶质质量分数可能相同
例16.由于高铁列车车厢是密闭的空间,因此需要提供清洁的空气和保持车厢的卫生。高铁酸钠(Na2FeOx)是高铁上常用的一种“绿色、环保、高效”的消毒剂。(1)已知高铁酸钠的相对分子质量为166,则x的值为____________。(2)____________克的高铁酸钠中含有4.6克的钠元素。(3)C2H4和C2H6O的混合物中,碳元素的质量分数为60%,则混合物中氧元素的质量分数为____________。(保留小数点后一位)
【答案】(1)4 (2)16.6 (3)26.7%
【解析】(1)已知高铁酸钠的相对分子质量为166,则23×2+56+16x=166,解得x=4。 (2)含有4.6克的钠元素的高铁酸钠的质量为 。(3)可将C2H6O看作C2H4H2O,除去H2O,由于C2H4中碳、氢元素质量比为(12×2):4=6:1,碳元素的质量分数为60%,则氢元素的质量分数为10%,则剩余的“H2O”的质量分数为1-60%-10%=30%,则氧元素的质量分数为
例19.小慧称取20 g某氯化铜样品放入烧杯中,加入50 g水使氯化铜完全溶解,逐滴加入一定溶质质量分数的氢氧化钾溶液,反应生成沉淀的质量与所加氢氧化钾溶液质量的关系如图所示[CuCl2+2KOH===2KCl+Cu(OH)2↓,氯化铜样品中所含杂质既不溶于水,也不参与反应]。试计算:(1)生成沉淀的质量为________g。(2)当恰好完全反应时,所得溶液的溶质质量分数。
解:(2)设当恰好完全反应时,生成氯化钾的质量是x,参与反应的氯化铜质量为y。CuCl2+2KOH===2KCl+Cu(OH)2↓135 149 98 y x 9.8 g
3.根据化学方程式进行简单的计算,如已知反应物的质量求生成物的质量,或已知生成物的质量求反应物的质量。
课堂小结:我们复习了以下内容,你掌握了吗?
化学就象你头顶上的果实,只要肯稍作努力,成功的甜蜜就属于你!祝你成功!
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




