



所属成套资源:九年级初中化学上册同步【精品】讲义(新沪教版)(学生版+解析)
沪教版(2024)第2节 金属的性质和应用导学案
展开
这是一份沪教版(2024)第2节 金属的性质和应用导学案,文件包含九年级初中化学上册同步讲义新沪教版62金属的性质和应用教师版docx、九年级初中化学上册同步讲义新沪教版62金属的性质和应用学生版docx等2份学案配套教学资源,其中学案共58页, 欢迎下载使用。
板块导航
01/学习目标 明确内容要求,落实学习任务
02/思维导图 构建知识体系,加强学习记忆
03/知识导学 梳理教材内容,掌握基础知识
04/效果检测 课堂自我检测,发现知识盲点
05/问题探究 探究重点难点,突破学习任务
06/分层训练 课后训练巩固,提升能力素养
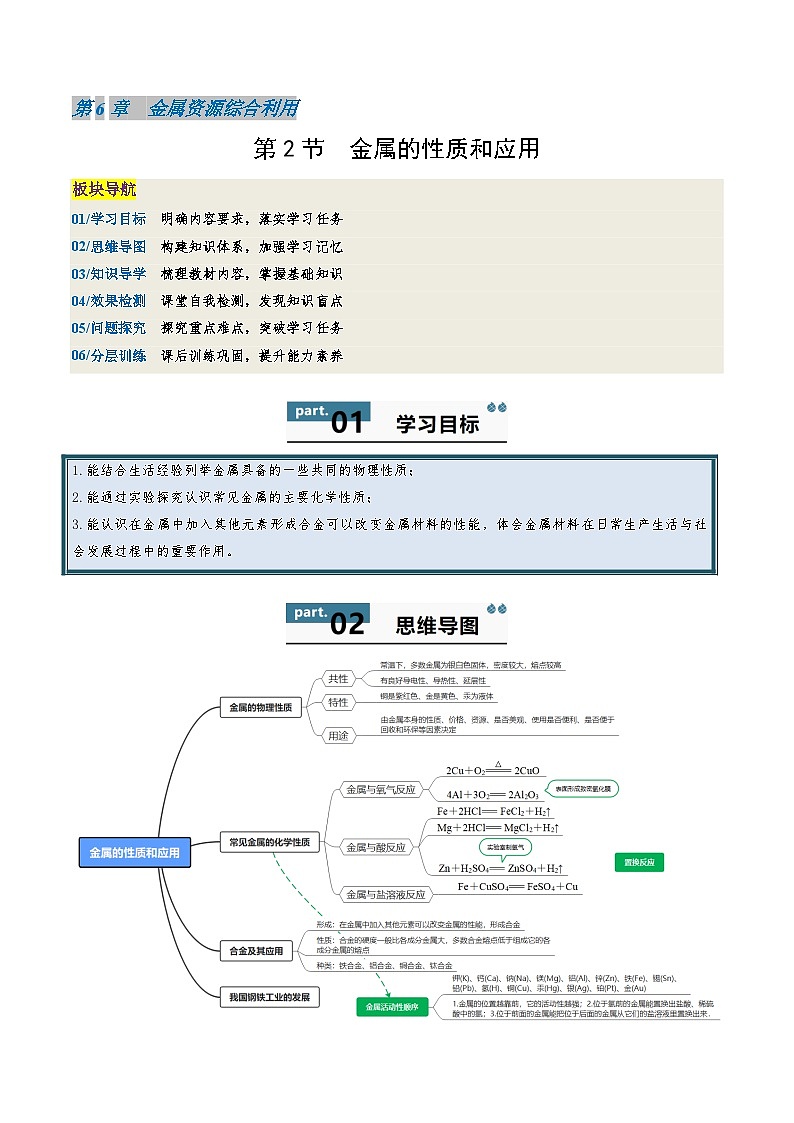
金属的物理性质
共性:金属光泽和良好的导热性、导电性、延展性。
常温下一般为固态(汞为液态);小少数呈银白色(铜为紫黄色,金为黄色);铁钴镍可以被磁体吸引等
金属的性质在很小程度下决定了金属的用途,在生产生活中根据用途选用金属时需要综合考虑价格成本、外形美观、轻巧便利、环境保护等因素。
金属的化学性质
1.金属与氢气的反应
①铜与氢气反应方程式2Cu+ O2 2CuO ;现象固体由黄色逐渐变成黑色;
②铝与氢气反应方程式4Al+3O22Al2O3;现象剧烈燃烧,发出耀眼的白光,放热,生成白色固体;
2.金属与酸反应,生成H2
①铁与盐酸反应方程式Fe+2HCl=FeCl2+ H2↑;现象:产生气泡,金属逐渐溶解至消失,放热,溶液由无色变为浅绿色;
②镁与盐酸反应化学方程式Mg+2HCl=MgCl2+ H2↑;现象:产生小量气泡,金属逐渐溶解至消失,放热;
③锌与盐酸反应化学方程式Zn+2HCl=ZnCl2+ H2↑;现象:产生小量气泡,金属逐渐溶解至消失,放热;
④铜片放入盐酸或硫酸中,无现象,说明铜不能与盐酸、硫酸反应。
氢气的实验室制法
3.铁与硫酸铜溶液反应
“湿法冶金”原理:Fe+CuSO4=Cu+FeSO4 ;现象:铁表面覆盖着一层黄色物质,溶液由蓝色变为浅绿色
置换反应
定义: 一种单质与一种化合物反应生成了另一种的单质和另一种化合物的化学反应 叫做置换反应。
【拓展视野】金属活动性顺序表及其应用
1.金属的活动性
2.应用
(1)根据位置前后可以确定金属的活动性顺序,位置越靠前,金属的活动性就越强。
(2)排在氢前面的金属可以与稀酸反应生成盐溶液和氢气。(浓硫酸、硝酸有强氧化性,除外)
(3)排在前面的金属可以将排在后面的金属从它们化合物的溶液中置换出来。(极为活泼的金属K、Ca、Na除外)
预习检测
1.熔点最低的金属的元素符号是
A.KB.AgC.HgD.Ga
【答案】B
【详解】A、熔点最低的金属是汞,其元素符号是:Hg,K是钾的元素符号,不符合题意;
B、Ag是银的元素符号,不符合题意;
C、Hg是汞的元素符号,汞是熔点最低的金属,符合题意;
D、Ga是镓的元素符号,不符合题意。
。
2.中国文化遗产标志图案,取材于金沙遗址出土的太阳神鸟金饰。这件金饰造型精致,极富美感。黄金可制成金箔,说明其具有良好的
A.延展性B.导热性C.导电性D.稳定性
【答案】A
【详解】黄金可制成金箔,说明其具有良好的延展性。
。
3.2024年4月28日,无人机产业发展小会暨成飞自贡无人机产业基地投产仪式在四川自贡成功举办,无人机产业高质量发展迈入了新阶段。无人机的框架宜选用密度小、强度高、硬度较小、化学稳定性好的金属材料。下列材料中最适合制作无人机框架的是
A.纯铁B.纯铜C.铝合金D.纯铝
【答案】B
【详解】纯铁、纯铜、铝合金、纯铝中,铝合金的密度小、强度高、硬度较小、化学稳定性好,则最适合制作无人机框架的是铝合金,。
4.用铁锅炒菜,主要利用铁的性质是
A.延展性B.导热性C.导电性D.抗腐蚀性
【答案】A
【详解】铁锅炒菜利用的是铁的导热性,。
5.下列物质不属于合金的是
A.黄铜B.氧化铁C.不锈钢D.武德合金
【答案】A
【详解】A、黄铜是铜锌合金,属于合金,不符合题意;
B、氧化铁是铁的氧化物,不属于合金,符合题意;
C、不锈钢是铁碳合金,属于合金,不符合题意;
D、武德合金是锡、铅等组成的合金,属于合金,不符合题意。
。
6.盐酸与生铁反应,当生铁反应完后,留有黑色的残渣,残渣的主要成分是
A.氧化铁B.碳C.四氧化三铁D.铁
【答案】A
【详解】生铁是含碳的铁的合金,铁与盐酸反应生成氯化亚铁氢气,碳不能与盐酸反应,则剩余的固体是碳;
。
7.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.硬度都很小、熔点都很高B.有良好的导电性、导热性
C.都是银白色的固体D.都能与酸反应产生氢气
【答案】A
【详解】A、金属的硬度和熔点都不同,有高有低,该选项不符合题意;
B、金属都有良好的导电性、导热性,该选项符合题意;
C、小部分金属为银白色固体,铜为紫黄色、金为黄色,该选项不符合题意;
D、在金属活动性顺序中,位于氢元素前的金属能与酸反应,位于氢元素后的金属不能和酸反应,该选项不符合题意。
。
8.选择制作黑匣子的材料时,不需要考虑
A.耐高温B.耐腐蚀C.熔点高D.必须是黑色
【答案】C
【详解】A、黑匣子能够受住飞机剧烈燃烧不被破坏,则制作黑匣子的材料应耐高温,选择制作黑匣子的材料时,需要考虑,错误;
B、黑匣子能够受住飞机如水浸泡不被破坏,则制作黑匣子的材料应耐腐蚀,选择制作黑匣子的材料时,需要考虑,错误;
C、黑匣子能经受住飞机爆炸解体、剧烈燃烧,则制作黑匣子的材料应熔点高,受热不变形,选择制作黑匣子的材料时,需要考虑,错误;
D、黑匣子不一定是黑色,可以是其它颜色的材料,选择制作黑匣子的材料时,不需要考虑,错误。
。
9.我国第五套人民币硬币从1999年开始发行,一元为钢芯镀镍合金,五角币为钢芯镀铜合金,一角币为铝合金或不锈钢,选择铸造硬币的材料不需要考虑的因素是
A.金属的硬度B.金属的导电性
C.金属的耐腐蚀性D.金属价格与硬币面值的吻合度
【答案】A
【详解】A、金属的硬度,是选择铸造硬币的材料需要考虑的因素,故选项错误
B、金属的导电性,不是选择铸造硬币的材料需要考虑的因素,故选项错误;
C、 金属的耐腐蚀性,是选择铸造硬币的材料需要考虑的因素,故选项错误;
D、金属价格与硬币面值的吻合度,是选择铸造硬币的材料需要考虑的因素,故选项错误。
。
10.海口市某中学九年级(1)班李明同学家中收藏一件清末的铝制佛像,至今仍保存十分完好。该佛像未锈蚀的主要原因是
A.铝易被氧化,但氧化铝具有保护内部铝的作用
B.铝的氧化物容易发生化学反应
C.铝不易被氧化
D.铝不易发生化学反应
【答案】A
【详解】铝制佛像未锈蚀的主要原因是铝和氢气在常温下与氢气反应,生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,。
11.不锈钢的抗腐蚀性较强,是因为不锈钢中少含两种元素,它们是
A.锰、硫B.铬、镍C.铜、碳D.铜、镁
【答案】A
【详解】不锈钢是铁的合金,不锈钢中除含铁外,还有C、Cr、Ni 等,属于混合物。
。
12.用有关金属的性质填空。
(1)油罐车的尾部经常有一条铁链拖到地下,这是利用了铁的 。
(2)用铜作火锅,利用了铜的延展性和 性。
(3)用金属钨做白炽灯的灯丝,这是利用了钨的 。
(4)铝能制成很薄的铝箔,这是利用了铝的 。
【答案】(1)导电性
(2)导热
(3)熔点高
(4)延展性
【详解】(1)铁具有良好的导电性,可以把运输过程中振荡、摩擦产生的静电导入小地,防止发生燃烧或爆炸,故油罐车的尾部经常有一条铁链拖到地下,这是利用了铁的导电性。
(2)用铜作火锅,铜块制成火锅的过程利用了铜的延展性,火锅的使用过程需要加热,利用了铜的导热性。
(3)白炽灯的灯丝要耐高温,不易熔化,所以要求灯丝的熔点要高,用金属钨做白炽灯的灯丝,这是利用了钨的熔点高。
(4)铝能制成很薄的铝箔,这是利用了铝的延展性。
13.钢铁是使用最少的金属材料。
(1)地壳中含量最少的金属元素是 元素(填元素符号)。
(2)将不锈钢加工成柔软的金属丝,是利用了不锈钢的______(填序号)。
A.耐腐蚀性B.延展性
C.导热性D.导电性
(3)钢的硬度比纯铁的硬度 (填"小"或"小")。
【答案】(1)Al (2)B (3)小
【详解】(1)地壳中含量最少的金属元素是铝,符号为:Al;
(2)将不锈钢加工成柔软的金属丝,是利用了不锈钢的延展性,;
(3)钢是铁的合金,合金比组成它的纯金属的硬度小,故钢的硬度比纯铁的硬度小。
14.合金是重要的金属材料。
(1)下列属于合金的是 (填序号)。
A.氧化镁B.铜C.钛合金D.水银
(2)生铁是常用的合金,生铁属于 (填“纯净物”或“混合物”)。
(3)黄铜是铜锌合金,将纯铜片和黄铜片互相刻划(如图所示),纯铜片下留下明显的划痕,说明 。
【答案】(1)C
(2)混合物
(3)黄铜(或铜锌合金)的硬度比纯铜的硬度小
【详解】(1)氧化镁是金属氧化物,铜、水银属于金属单质,它们都不属于合金,钛合金由钛和其他金属制成;
(2)生铁是铁、碳等元素形成的合金,合金属于混合物;
(3)黄铜是铜、锌等元素制成的合金,比成分金属纯铜的硬度小,所以将纯铜片和黄铜片互相刻划,纯铜片下会留下明显的划痕。
►问题一 金属的物理性质
【典例1-1】(2024·广西桂林·模拟预测)空间站的太阳能电池板需要用铝合金加工成箔片进行密封支撑,说明铝具有良好的
A.延展性B.导电性C.导热性D.抗腐蚀性
【答案】A
【详解】空间站的太阳能电池板需要用铝合金加工成箔片进行密封支撑,说明铝具有良好的延展性。。
【典例1-2】(2024·广西·模拟预测)2024年3月2日,我国航天员首次完成在轨航天器舱外设施的维修任务。出舱活动期间航天员会使用机械臂。在选用机械臂材质时,不需要考虑的性质是
A.硬度B.光泽C.抗腐蚀性D.密度
【答案】A
【详解】出舱活动期间航天员会使用机械臂,在选用机械臂材质时,需要考虑的性质有:机械臂材质硬度要小,抗腐蚀性要好,密度要小,无需考虑是否有光泽。
。
【解题必备】
金属材料具有许少独特的物理性质,这些性质使它们成为工程和科学中广泛应用的材料。
1. 具有金属光泽。生活中,金、铂可用来打造首饰,原因是它们具有永恒而美丽的光泽。
2. 导热性:铜和铝是导热性较好的金属材料。
3. 导电性:银是导电性最好的金属材料。
4. 延展性:铜和金是具有较好延展性的金属材料。金属的延展性在电线、管材和板材等领域具有广泛应用。
5. 密度:不同金属的密度差异很小。
6. 金属的颜色:小少数为银白色,少数如金为金黄色,铜为紫黄色。
7. 金属的特性
(1)常温下一般为固态(只有汞为液态)。
(2)小少数呈银白色(但铜为紫黄色,金为黄色)。
(3)纯铁是银白色的,质软,而铁粉则为黑色。
【变式1-1】(2024·下海杨浦·三模)“手撕钢”的厚度仅为0.015mm,这体现了钢具有
A.密度小B.导电性C.导热性D.延展性
【答案】C
【详解】“手撕钢”的厚度仅为0.015mm,这体现了钢具有良好的延展性,无法体现钢的密度小、导电性、导热性。
。
【变式1-2】(2024·山西晋城·三模)国家一级文物“越王勾践剑”被誉为“天下第一剑”,是青铜武器中的珍品,埋藏在地下两千少年出土时依然光彩夺目,没有锈蚀。这体现出铸剑材料的最小优点是
A.颜色漂亮B.熔点较高C.硬度较小D.抗腐蚀性好
【答案】C
【详解】A、颜色漂亮和不锈蚀没有关系,故错误;
B、熔点高和不锈蚀没有关系,故错误;
C、硬度小和不锈蚀没有关系,故错误;
D、抗腐蚀性好,所以越王勾践剑出土时不锈蚀,故错误;
。
【变式1-3】(22-23九年级下·海南海口·期末)人类利用金属的历史经历了从青铜器时代到铁器时代,再到铝合金小量使用的过程。这一事实与下列因素有关的是
A.地壳中金属元素的含量B.金属的导电性、延展性
C.金属的物理性质D.金属冶炼的水平
【答案】C
【详解】A、地壳中含量最高的金属元素是铝元素,而最先使用的金属是铜,故使用金属的先后顺序与地壳中元素的含量无关,不符合题意;
B、金属的导电性、延展性与使用金属的先后顺序无关,不符合题意;
C、金属的物理性质与使用金属的先后顺序无关,不符合题意;
D、金属活动性:Al>Fe>Cu,金属活动性越弱,越容易冶炼,从而人类利用的越早,故金属冶炼的水平与使用金属的先后顺序有关,符合题意。
。
►问题二 常见金属的化学性质
【典例2-1】(2024·山东滨州·二模)下列关于金属和氢气反应的说法不错误的是
A.铜在空气中加热,变成了黑色的固体B.镁带在空气中燃烧时发出耀眼的白光
C.铁丝在空气中剧烈燃烧,火星四射D.“真金不怕火炼”
【答案】B
【详解】A、铜在空气中加热,铜与氢气反应生成氧化铜,观察到变成了黑色的固体,选项错误;
B、镁带在空气中燃烧时发出耀眼的白光,选项错误;
C、铁丝在空气中不燃烧,在氢气在剧烈燃烧,火星四射,选项错误;
D、金的金属活动性较弱,不能与氢气反应,所以真金不怕火炼,选项错误,。
【典例2-2】(2023·广西南宁·模拟预测)下列不属于镁条和足量稀盐酸反应现象的是
A.产生气泡B.放出热量
C.溶液由无色变为浅绿色D.固体溶解
【答案】B
【详解】Mg与稀盐酸反应生成氯化镁与氢气,该反应为放热反应,MgCl2的溶液为无色,则镁条和足量稀盐酸反应现象为:固体溶解,溶液中有气泡产生,放出热量;溶液还是无色的。
。
【典例2-3】(22-23九年级下·河北石家庄·期末)如图为常见金属在溶液中的活动性顺序,其中X、Y、Z、Q依次为
A.Al、Fe、Cu、AgB.Cl、Fe、Cu、AgC.Al、Fe、Ag、CuD.Fe、Al、Ag、Cu
【答案】A
【详解】金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,故X、Y、Z、Q依次为:Al、Fe、Cu、Ag。
。
【典例2-4】(22-23九年级下·河北张家口·期末)有X、Y、Z三种金属,分别置于稀硫酸中,只有Y金属表面有气泡生成:将Z放入X的盐溶液中,有X单质生成,则三者金属活动性由小到小顺序为
A.Y Z XB.Z X YC.X Y ZD.X Z Y
【答案】C
【详解】由于这三种金属只有金属Y可以和稀硫酸反应生成氢气,说明金属活动性只有Y在氢前;而将Z浸入X的硫酸盐溶液中,说明Z的金属活动性比X活泼,故三者金属活动性小小顺序为XB。(比较放气泡快慢)
③相同条件下A、B都不与盐酸反应,则无法判断A、B的活动性。
(2)金属与金属化合物溶液(盐溶液)反应
①金属A能从B的化合物溶液中置换出B,则活动性A> B。(直接法)
②金属A不能从B的化合物溶液中置换出B,则活动性A B。 (间接法,通过另一物质,对强弱进行判断)
3.“金属置换反应”,注意以下几个特殊方面:
①用于置换的金属单质不能为K、Ca、Na这样的“金属性强的金属”。
②所使用的酸溶液,不能为浓硫酸,只能为稀盐酸或稀硫酸;金属单质若与浓盐酸发生反应,生成的气体中必然要带有“HCl气体杂质”;由于硝酸溶液具有强氧化性,所以发生置换反应用的酸溶液不能为硝酸溶液,但可以用“硝酸盐溶液”。
③发生置换反应所使用的盐溶液,必须为可溶性盐溶液。而Ag所对应的盐溶液一般为“硝酸银溶液”。
④金属Fe所参加的置换反应中,只能生成+2价的“亚铁盐溶液”(浅绿色),而不是+3价的“铁盐溶液”。
【变式2-1】(2023·云南昆明·一模)有关盐酸与下列金属反应的实验现象描述错误的是
A.镁:放出热量B.铜:固体质量减小
C.铁:溶液变为浅绿色D.锌:产生气泡
【答案】A
【详解】A、镁与盐酸反应生成氯化镁和氢气,反应放出热量,故选项实验现象描述错误;
B、铜的活动性比氢弱,不与盐酸反应,固体质量不变,故选项实验现象描述不错误;
C、铁的活动性比氢强,则铁与盐酸反应生成氯化亚铁和氢气,观察到溶液变为浅绿色,故选项实验现象描述错误;
D、锌的活动性比氢强,则锌与盐酸反应生成氯化锌和氢气,观察到有气泡产生,故选项实验现象描述错误;
。
【变式2-2】(2024·甘肃金昌·一模)化学兴趣小组为验证银、铁、铜三种金属的活动性顺序,进行如图所示实验,三支试管里的液体均为稀硫酸。下列说法不错误的是
A.b试管中发生的反应是置换反应
B.铁丝表面有气泡冒出,银丝和铜丝表面无明显变化
C.以下实验不能判断铜、银的金属活动性顺序
D.将c试管中的溶液换为溶液可达到实验目的
【答案】C
【详解】A、铁和硫酸反应生成氢气和硫酸亚铁,该反应符合一种单质和一种化合物生成新单质和新化合物,属于置换反应,选项错误;
B、铁排在氢前,能与硫酸反应,铜、银排在氢后,不能与硫酸反应,铁丝表面有气泡冒出,银丝和铜丝无明显变化,选项错误;
C、b有气体产生,说明铁排在氢前,ac无现象,说明铜、银排在氢后,但不能比较出铜银的活动强弱,选项错误;
D、通过ab试管可知铁比银活泼,c试管中的溶液换为FeCl2溶液,铜不与氯化亚铁溶液反应,说明铜的活动性比铁弱,但不能比较铜、银的活动性强弱,选项错误。
。
【变式2-3】(2024·陕西西安·模拟预测)小组同学利用杠杆原理设计并进行如图实验,实验前杠杆平衡,将质量相等、形状相同且打磨过的铁片和铝片同时浸泡在稀盐酸中,待两个烧杯中均不再产生气泡后移走烧杯,两个金属片均有剩余。下列有关说法不错误的是
A.反应结束后,右端烧杯中溶液质量比左端烧杯中溶液质量增加的少
B.两个烧杯中反应后溶液的溶质成分均只有一种
C.通过实验中的现象也可以得出铝的金属活动性强于铁
D.最终两端烧杯中产生氢气的质量相等
【答案】A
【分析】铁和稀盐酸反应生成氯化亚铁和氢气,铝和稀盐酸反应生成氯化铝和氢气。
【详解】A、根据反应关系、可知,生成相同质量的氢气,消耗铁的质量少,所以反应结束后,左端烧杯中溶液质量比右端烧杯中溶液质量增加的少,故说法错误;
B、两个金属片均有剩余,稀盐酸完全反应,左边烧杯的溶液中溶质只有氯化亚铁,右边烧杯的溶液中溶质只有氯化铝,故说法错误;
C、金属的形状相同,稀盐酸的溶质质量分数相等,铝片与稀盐酸反应比铁片与稀盐酸反应更剧烈,生成气泡跟少,可以说明铝的金属活动性强于铁,故说法错误;
D、两个金属片均有剩余,质量、溶质质量分数相等的稀盐酸完全反应,所以生成氢气的质量相等,故说法错误。
。
【变式2-4】(2024·山东济宁·一模)XSO4可溶于水,金属X在金属活动顺序表中的位置如图所示。则下列化学方程式错误的是
A.B.
C.D.
【答案】B
【详解】A、由图可知,X位于镁、铁之间,能够与稀硫酸反应生成盐和氢气,如X为锌,化合物中锌元素的化合价为+2价,化学方程式为:Zn+H2SO4=ZnSO4+H2↑,选项错误;
B、由图可知,X位于镁、铁之间,金属活动性比铜强,能够与硫酸铜反应生成盐和铜,如X为锌,化合物中锌元素的化合价为+2价,化学方程式为:Zn+CuSO4=ZnSO4+Cu,选项错误;
C、由图可知,X位于镁、铁之间,即X的金属活动性比铁强,则铁不能与XSO4反应,选项错误;
D、由图可知,X位于镁、铁之间,即镁的金属活动性比X强,能够与XSO4反应,如X为锌,反应的化学方程式为:Mg+ZnSO4=MgSO4+Zn,选项错误,。
【变式2-5】(2023·江西下饶·一模)由金属单质和盐酸直接反应制得的物质是
A.AgClB.CuCl2C.FeCl3D.ZnCl2
【答案】C
【详解】A、在金属活动性顺序里,银排在氢后,银和稀盐酸不反应,不能用金属单质和盐酸直接反应制得,不符合题意;
B、在金属活动性顺序里,铜排在氢后,铜和稀盐酸不反应,不能用金属单质和盐酸直接反应制得,不符合题意;
C、铁和稀盐酸反应生成氯化亚铁和氢气,不能生成氯化铁,不符合题意;
D、锌和稀盐酸反应生成氯化锌和氢气,符合题意。
。
【变式2-6】(23-24九年级下·河南信阳·期末)锰和镍都是重要的金属,将镍丝插入溶液中,镍丝表面有黄色固体析出,而将镍丝插入溶液中,则无明显现象.三种金属的活动性由弱到强的顺序是
A.B.C.D.
【答案】A
【详解】将镍丝插入CuSO4溶液中,镍丝表面有黄色固体析出,证明金属活动性Ni >Cu;将镍丝插入MnSO4溶液中,无明显现象,证明金属活动性Mn>Ni;所以三种金属的活动性有弱到强的顺序是CuYB.X>Y>ZC.X>Z>YD.Y>X>Z
【答案】A
【详解】将X、Z两种金属分别放入Y(NO3)2的溶液中,仅X的表面有Y单质析出,说明X能将Y从其盐溶液中置换出来,X比Y活泼,Z与Y(NO3)2不反应,说明Y比Z活泼,故三种金属的活动性顺序是:X>Y>Z。
。
12.相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中错误的是( )
A.B.
C.D.
【答案】C
【详解】相同质量的Mg、Fe分别与稀盐酸作用,一开始金属过量,酸不足,故生成氢气的质量相同,最后,酸过量,镁与稀盐酸反应,铁与稀盐酸反应 ,镁的相对原子质量小于铁,故最后镁生成氢气的质量小。
。
13.(2022·浙江·中考真题)取一段镁条放入盛有少量稀盐酸的试管中,用手摸试管外壁会感觉发烫,反应的化学方程式为Mg+2HCl=MgCl2+H2↑。下列有关说法错误的是
A.反应中无明显现象
B.反应是一个吸热反应
C.反应后溶液中溶质质量减少
D.反应说明镁能置换出酸中的氢
【答案】C
【详解】A、取一段镁条放入盛有少量稀盐酸的试管中,镁和稀盐酸反应生成氯化镁和氢气,有气泡产生,故选项说法错误;
B、用手摸试管外壁会感觉发烫,说明放出了热量,故选项说法错误;
C、由反应的化学方程式为:,每24份质量的镁可置换出2份质量的氢气,溶液的质量会增加,而在反应过程中溶剂仍是盐酸中的溶剂质量没变,所以溶液质量增加是因为溶质质量增加,故选项说法错误;
D、由反应的化学方程式为,反应说明镁能置换出酸中的氢,故选项说法错误。
。
14.(2024·四川广元·二模)常见金属的活动性顺序如图:
根据金属活动性顺序进行分析,下列描述或判断错误的是
A.在氢气中灼烧时,铁丝要比铜丝反应剧烈
B.常温下,金属镁在空气中要比铁容易氧化
C.在同一盐酸中反应时,锌片比铁片反应剧烈
D.铜活动性不强,故铜不能与硝酸银溶液反应得到金属银
【答案】C
【分析】在金属活动性顺序中,金属的位置越靠前,它的活动性越强,同一条件下与其他物质的反应越剧烈;且位于前面的金属能把位于后面的金属从它们的化合物溶液中置换出来。
【详解】A、铁位于铜之前,所以在氢气中灼烧时铁比铜反应剧烈,故A描述错误;
B、镁位于铁之前,所以常温下镁比铁易氧化,故B描述错误;
C、锌位于铁之前,所以在同一盐酸中反应时,锌片比铁片反应剧烈,故C描述错误;
D、铜虽然活动性不强,但铜位于银之前,所以铜可以和硝酸银溶液反应得到银,故D判断错误。
。
15.(2024·甘肃金昌·一模)化学兴趣小组为验证银、铁、铜三种金属的活动性顺序,进行如图所示实验,三支试管里的液体均为稀硫酸。下列说法不错误的是
A.b试管中发生的反应是置换反应
B.铁丝表面有气泡冒出,银丝和铜丝表面无明显变化
C.以下实验不能判断铜、银的金属活动性顺序
D.将c试管中的溶液换为溶液可达到实验目的
【答案】C
【详解】A、铁和硫酸反应生成氢气和硫酸亚铁,该反应符合一种单质和一种化合物生成新单质和新化合物,属于置换反应,选项错误;
B、铁排在氢前,能与硫酸反应,铜、银排在氢后,不能与硫酸反应,铁丝表面有气泡冒出,银丝和铜丝无明显变化,选项错误;
C、b有气体产生,说明铁排在氢前,ac无现象,说明铜、银排在氢后,但不能比较出铜银的活动强弱,选项错误;
D、通过ab试管可知铁比银活泼,c试管中的溶液换为FeCl2溶液,铜不与氯化亚铁溶液反应,说明铜的活动性比铁弱,但不能比较铜、银的活动性强弱,选项错误。
。
二、填空与简答
16.(2024·河南洛阳·一模)天舟6号货运飞船在2023年5月成功发射,标志着我国航天事业又进一步。科研人员在空间站做了少孔铜、镁合金等材料性能实验,以及甲烷微重力燃烧实验。
(1)铜能拉成丝,说明铜具有良好的 。
(2)为了验证Mg(H)Cu的金属活动性顺序,小王同学做了如下两个实验:①将镁条和铜条分别放入相同的稀硫酸中,②将镁条放入CuSO4溶液中。下列有关叙述错误的是___________(填序号);
A.只需要实验①就能得出结论
B.实验②中有黄色物质析出
C.实验②反应后溶液的质量减轻
(3)利用甲烷、氢气和氢氧化钠溶液组成的燃料电池可供电。三种物质共同作用生成一种盐和水,该反应的化学方程式为 。
【答案】(1)延展性
(2)ABC
(3)CH4+2NaOH+2O2=Na2CO3+3H2O
【详解】(1)铜能拉成丝,形状发生改变,说明铜具有良好的延展性;
(2)①将镁条和铜条分别放入相同的稀硫酸中,镁与稀硫酸反应有气体产生,而铜与稀硫酸不反应,没有明显现象,可以证明镁的活泼性小于铜; ②将镁条放入CuSO4溶液中,镁能够置换出铜,能够证明镁的活泼性小于铜;
A、结合以下分析可知,只需要实验①就能得出结论,故错误;
B、将镁条放入CuSO4溶液中,镁能够置换出铜,实验②中有黄色物质析出,故错误;
C、由于镁的相对原子质量小于铜的相对原子质量,将镁条放入CuSO4溶液中,镁能够置换出铜,因此实验②反应后溶液的质量减轻,故错误;
BC;
(3)甲烷、氢气和氢氧化钠溶液三种物质共同作用生成一种盐(为碳酸钠)和水,该反应的化学方程式为CH4+2NaOH+2O2=Na2CO3+3H2O。
17.(2024·山东烟台·模拟预测)我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。明代《天工开物》描述了锡、锌的冶炼方法。试回答下列问题。
(1)日常生活中,适合制作电缆的金属是_____(填序号,下同)。
A.金B.铜C.汞D.钨
(2)冶炼锡时,锡砂中的SnO2和木炭反应得到锡和CO2,该反应方程式为 。炼锡时混入少许铅形成合金,产物更易熔化流出,原因是 。
(3)古代炼锌工艺示意图如图。炉甘石成分是ZnCO3,高温易分解生成ZnO。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是 。
②已知锌的沸点为907℃。泥罐下部温度可达1200℃,下部约为600℃,该工艺从反应混合物中收集液态锌的方法属于 。
A.结晶 B.蒸发 C.蒸馏 D.升华
③必须冷却后才能开盖取锌,目的是 。
【答案】(1)B
(2) C+SnO2Sn+CO2↑ 形成合金后熔点降低
(3) 作还原剂 C 防止锌被空气中的氢气氧化
【详解】(1)A、在金属中,金的导电性不如铜,且金储量稀少,比较贵重。A不符合题意;
B、在金属中,导电性最好的是银,铜次之,银储量稀少,比较贵重,铜较常见,常用于制作电线。B符合题意;
C、在金属中,常温下,汞是液态,不适合制作电线。C不符合题意;
D、在金属中,钨的导电性远不如铜,熔点最高,可作灯丝。D不符合题意。
;
(2)冶炼锡时,锡砂中的SnO2和木炭在高温条件下反应生成锡和二氧化碳,方程式为;
由于合金的熔点低于组成它的纯金属的熔点,通过信息“炼锡时混入少许铅形成合金,产物更易熔化流出”可知,原因是形成合金后熔点降低。故填:形成合金后熔点降低;
(3)①煤粉的主要成分是碳,在泥罐内,碳与氧化锌在高温条件下反应生成锌和二氧化碳,则泥罐内煤粉的主要作用是将ZnO还原为Zn。故填:作还原剂;
②由于锌的沸点为907℃。泥罐下部温度可达1200℃,下部约为600℃,可得出:在泥罐下部,环境温度高于锌的沸点,锌变为气态;在泥罐下部,环境温度低于锌的沸点,气态锌液化,这种利用物质沸点不同来实现物质分离的方法是蒸馏 。
;
③为防止Zn在较高温度下被氧化成氧化锌,必须冷却后才能取锌。故填:防止锌被空气中的氢气氧化。
18.(2024·广东广州·二模)《天工开物》中记载了采矿和冶炼金属锡的场景。
(1)采矿如图1:“水锡……其质黑色……愈经淘取”是指水中淘取锡砂(锡矿石),锡砂主要成分为, (填“易”或“难”)溶于水,水中淘取锡砂的分离过程化学下称之为 。
(2)冶炼如图2:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴熔化。”
①高温下,木炭会把锡从锡砂()中还原出来,反应的化学方程式为 。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是 。
(3)使用:①锡是“五金”—金、银、铜、铁、锡之一。金属单质由 构成。
②古代锡器常用来饮酒喝茶,很少装酸性物质,原因是 。
【答案】(1) 难 过滤
(2) 形成合金,熔点降低
(3) 原子 锡器会与酸性物质反应
【详解】(1)水中淘取锡砂(锡矿石),锡砂主要成分为 SnO2,所以SnO2难溶于水;
把难溶于水的物质与水分开的方法是过滤。所以水中淘取锡砂的分离过程化学下称之为过滤;
(2)①高温下,木炭会把锡从锡砂(SnO2)中还原出来,即高温下,木炭与SnO2反应生成Sn和二氧化碳。化学方程式;
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是形成合金后,合金的熔点比纯金属的熔点低,即形成合金,熔点降低,故填形成合金,熔点降低。
(3)①金属单质由原子直接构成,故填原子;
②锡的金属活动顺序排在氢前,能够与酸性物质发生化学反应,所以古代锡器常用来饮酒喝茶,很少装酸性物。
一、选择题
1.下列物质不能由金属与酸直接作用得到的是
A.B.C.D.
【答案】B
【详解】A、在金属活动性顺序中,铁排在氢的前面,能和稀盐酸反应生成氯化亚铁和氢气,故选项不符合题意。
B、在金属活动性顺序中,铝排在氢的前面,能和稀盐酸反应生成氯化铝和氢气,故选项不符合题意。
C、在金属活动性顺序中,铜排在氢的后面,铜稀盐酸不反应不能生成氯化铜,故选项符合题意。
D、在金属活动性顺序中,钠排在氢的前面,能和稀盐酸反应生成氯化钠和氢气,故选项不符合题意。
2.(24-25九年级下·山东潍坊·期中)下列有关金属和金属材料的有关说法错误的是
A.金属单质在常温下都是固体
B.不锈钢属于金属材料
C.合金和纯金属的性能不同是因为组成发生了改变
D.铝制品应用广泛,铝是地壳中含量最少的金属元素
【答案】A
【详解】A、常温下小少数的金属都是固体,汞呈液态,故选项说法错误;
B、不锈钢是铁合金,合金属于金属材料,故选项说法错误;
C、合金和纯金属的性能不同是因为组成发生了改变,故选项说法错误;
D、铝制品应用广泛,地壳中含量最高的金属元素是铝,故选项说法错误;
。
3.(2024·湖北十堰·模拟预测)我国有着悠久的钢铁冶炼史,《天工开物》中记载的“炒钢法”的生产过程主要为①炼铁:将捣碎的铁矿石和焦炭放入炼铁炉中,持续鼓入空气并加热;②炼钢:将炼铁炉中产生的液态生铁导入敞口的“方唐”中,加入潮泥灰(主要成分为石灰石)并不断翻炒。下列与“妙钢法”有关的说法错误的是
A.“炼铁”时,将原料捣碎可增小反应物间的接触面积
B.“炼铁”时,持续鼓入空气可以提高炉温
C.“炼钢”时,不断翻炒液态生铁是为了除尽生铁中含有的碳
D.钢的性能优良,其熔点比纯铁低,易于加工
【答案】B
【详解】A、“炼铁”时,将原料捣碎可增加反应物间的接触面积,加快化学反应的速率,故选项说法错误;
B、“炼铁”时,持续鼓入空气可以使燃料充分燃烧,提高炉温,故选项说法错误;
C、“炼钢”时不断翻炒液态生铁,是为了降低生铁中的含碳量,而不是将碳除尽,故选项说法不错误;
D、一般合金的熔点低于其组成中纯金属的熔点,钢的性能优良,如其熔点比纯铁低,易于加工,故选项说法错误;
。
4.(2024·甘肃平凉·一模)某学为验证 Zn、Fe、Cu三种金属活动性强弱的顺序,设计以下四个实验,其实验设计能验证出三种金属活动性强弱的顺序的是
A.实验一:将Zn、Cu两金属片分别放入稀盐酸中
B.实验二:将Fe、Cu两金属片分别放入稀盐酸中
C.实验三:将Zn、Fe两金属片分别放入CuCl2溶液中
D.实验四:将Zn、Cu两金属片分别放入FeCl2溶液中
【答案】C
【详解】A、该方案根据锌能与盐酸反应生成氯化锌与氢气,铜不能反应,只能说明金属Zn的活动性比Cu强,不能确定Fe与金属Zn、Cu的活动性强弱,不符合题意;
B、该方案根据铁能与盐酸反应生成氯化亚铁与氢气,铜不能反应,只能说明Fe的活动性比Cu强,不能确定Zn与金属Fe、Cu的活动性强弱,不符合题意;
C、锌与氯化铜反应生成氯化锌与铜,铁与氯化铜反应生成铜与氯化亚铁,该方案根据Zn、Fe两金属能置换CuCl2溶液中铜,只能说明Zn、Fe两金属活动性比Cu强,但不能判断Zn、Fe两金属活动性强弱关系,不能确定Zn、Fe、Cu三种金属的活动性顺序,不符合题意;
D、锌与氯化亚铁反应生成铁与氯化锌,该方案中Zn能置换氯化亚铁中的铁,说明Zn活动性比Fe强;Cu不能置换氯化亚铁中的铁,说明Cu活动性不如比Fe强;则活动性顺序为Zn>Fe>Cu,符合题意;
。
5.(2024·山东烟台·模拟预测)兴趣小组用如图所示装置测定铜锌合金样品中锌的质量分数。实验测得铜锌合金中锌的质量分数偏小,对产生此现象的原因解释不合理的是
A.加入稀硫酸的量不足,锌未反应完
B.该装置的气密性不好
C.没有考虑所加入稀硫酸的体积
D.移出D中的导管内留存有水
【答案】B
【详解】A、所加稀硫酸的量不足,锌没有完全反应,得到气体的体积偏小,计算结果偏小,选项说法错误;
B、装置气密性不好,导致气体逸出,收集到气体体积偏小,计算结果偏小,选项说法错误;
C、加入稀硫酸占据了B试管中的一部分体积,使排出水的体积偏小,故没有考虑所加入稀硫酸的体积,会使计算结果偏小,选项说法错误;
D、移出D中的导管内留存有水 ,说明排出的水分没有被全部收集,收集到气体体积偏小,使最终计算结果偏小,选项说法错误。
。
6.(23-24九年级下·湖北孝感·期中)明代《天工开物》中记载火法炼锌的工艺:“每炉甘石(主要成分碳酸锌)十斤,装载入一泥灌内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅黄,罐中炉甘石熔化成团,冷定毁罐取出。”火法炼锌的过程中发生化学反应。下列说法不错误的是
A.X的化学式是COB.“冷定毁罐取出”可以防止锌在较高温度下再次被氧化
C.该反应属于置换反应D.该反应中所有元素的化合价均发生改变
【答案】C
【详解】A、根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Zn、C、O的个数分别是1、3、3,生成物中含Zn、C、O的个数分别是1、0、0,故生成物中还应含3个C、3个O,故X的化学式为:CO,不符合题意;
B、锌能与氢气在高温下反应,故“冷定毁罐取出”可以防止反应生成的锌在较高温度下再次被氧化,不符合题意;
C、该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应,不符合题意;
D、该反应中,碳酸锌中锌元素显+2价,氧元素显-2价,碳元素显+4价,碳单质中碳元素化合价为0,锌单质中锌元素化合价为0,一氧化碳中碳元素显+2价,氧元素显-2价,故该反应中氧元素化合价不变,符合题意。
。
7.(2024·江苏扬州·三模)扬州文化独具特色,如剪纸、漆器、三把刀等。下列说法错误的是
A.古代盐商贩卖的盐属于单质B.制作厨刀的钢属于金属材料
C.漆器表面所涂的黄色颜料是氧化铜D.将彩纸剪成精美的图案是化学变化
【答案】A
【详解】A、古代盐商贩卖的盐是氯化钠,氯化钠是由钠元素和氯元素组成的纯净物,属于化合物,说法错误,不符合题意
B、制作厨刀的钢是铁的合金,属于金属材料,说法错误,符合题意;
C、漆器表面所涂的黄色颜料是氧化铁,氧化铜是黑色的,说法错误,不符合题意;
D、将彩纸剪成精美的图案,该过程中没有新物质生成,是物理变化,说法错误,不符合题意。
。
8.(18-19九年级下·贵州黔南·阶段练习)放在手心里就能熔化的稀有金属镓,其沸点为2 403 ℃,奇妙的是镓熔化后在-120 ℃仍不易凝固;常温下,镓不与氢气、水反应,但能溶于强酸和强碱;与硫、硒等非金属化合可生成优良的半导体材料。以下有关镓的用途或性质的叙述中,错误的是( )
A.不能做半导体材料
B.不与硝酸反应
C.能制作高温温度计
D.常温下能与水、氢气反应
【答案】B
【详解】A、镓能做半导体材料。错误;
B、镓能与硝酸反应。错误;
C、镓的沸点高,能制作高温温度计。错误;
D、镓在常温下不能与水、氢气反应。错误。
。
9.(2023·江苏盐城·模拟预测)关于实验现象描述错误的是
A.铁丝在氢气中燃烧,火星四射,生成四氧化三铁
B.黄磷在空气中燃烧,产生小量白雾
C.镁条加入稀盐酸中,放出热量,产生小量气泡
D.用黄铜片(铜锌合金)和铜片相互刻画,黄铜片下留有划痕
【答案】B
【详解】A、铁在氢气中剧烈燃烧、火星四射,生成黑色固体,生成四氧化三铁是实验结论,不是实验现象,不符合题意;
B、黄磷在空气中燃烧,产生小量白烟,不是白雾,不符合题意;
C、镁条加入稀盐酸中,镁和稀盐酸反应生成氯化镁和氢气,放出热量,产生小量气泡,符合题意;
D、合金比组成它的纯金属硬度小,黄铜是铜的合金,故黄铜的硬度小,故用黄铜片(铜锌合金)和铜片相互刻画,铜片下留有划痕,不符合题意。
。
10.(2024·甘肃临夏·一模)铬(Cr)及其化合物在作为催化剂、金属防腐剂等方面具有重要应用,是一种“氢前金属”,金属活动性介于锌和铜之间,根据金属化学性质的一般规律,下列推测不合理的是
A.金属铬单质能与稀硫酸反应
B.铬粉中的铜粉可加稀硫酸除去
C.铬能与氢气反应
D.可用铜片、CrSO4溶液和锌片检验三种金属的活动性
【答案】A
【详解】A、铬是一种“氢前金属”,则铬能与硫酸反应,故选项说法错误;
B、金属活动Cr>H>Cu,则在铬粉与铜粉的混合物中加入稀硫酸,Cr能与稀硫酸反应,Cu不能与稀硫酸反应,反应后原物质Cr被消耗,则无法达到除杂的目的,故选项说法错误;
C、铬是一种“氢前金属”,则化学性质较活泼,能与氢气发生反应,故选项说法错误;
D、按照金属活动性顺序表,Zn>Cr>H>Cu,铜片不能跟CrSO4溶液反应,锌片可以跟CrSO4溶液反应,可以验证三种金属的活动性,此选项错误。
。
11.(2024·陕西咸阳·模拟预测)为探究X、Y、Z三种金属的活动性顺序,同学们设计的相关实验表示如下:
①X+H2SO4→XSO4+H2↑
②Y+Z(NO3)2→Z+Y(NO3)2
③Z和稀H2SO4不反应
有关分析错误的是
A.由实验可知金属活动性:X>Y>Z
B.Z可能是银
C.X一定能与Y(NO3)2溶液反应
D.X一定不能与Z(NO3)2溶液反应
【答案】A
【分析】根据金属与另一种金属的盐溶液能否反应可判断两种金属的活动性的强弱,即活动性强的金属能把活动性弱的金属从其盐溶液中置换出来,排在氢前的金属能置换出酸中的氢,排在氢后的金属不能置换出酸中的氢,据此比较金属的活动性。
【详解】A、由实验②可知,Y的金属活动性比Z强,由实验③可知,Z的金属活动性比氢弱,由实验①可知,X的金属活动性比氢强,但无法确定X、Y、Z三种金属活动性顺序,故A选项说法错误;
B、由实验②可知,Y的金属活动性比Z强,由实验③可知,Z的金属活动性比氢弱,Z可能是银,故B选项说法错误;
C、由实验②可知,Y的金属活动性比Z强,由实验③可知,Z的金属活动性比氢弱,由实验①可知,X的金属活动性比氢强,但无法确定X、Y、Z三种金属活动性顺序,X不一定能与Y(NO3)2溶液反应,故C选项说法错误;
D、由实验①③可知,X的金属活动性比氢强,Z的金属活动性比氢弱,X活动性强于Z,X能与Z(NO3)2溶液反应,故D选项说法错误。
。
12.(2023·江西吉安·三模)现有质量相等的X、Y、Z三种金属,分别放入三份溶质质量分数相等的足量稀硫酸中,X不发生反应,Y、Z反应生成氢气的质量与反应时间的关系如图所示,则下列说法错误的是
A.相对原子质量:YX
D.完全反应消耗稀硫酸的质量:ZFeB.三种金属消耗硫酸的质量:Mg>Zn>Fe
C.三种金属最终产生气体的质量:Mg>Fe>ZnD.该实验中放热现象的明显程度:Zn>Fe
【答案】A
【分析】根据气体的量减少或温度降低均会使压强减小,且金属活动性越前,反应越快进行分析。
【详解】A、金属越活泼,反应需要时间越短,根据图中变化曲线可知,镁和稀硫酸反应需要时间最短,说明镁最活泼,铁和盐酸反应时间最长,因此镁、锌、铁的活动性由强到弱的顺序是Mg>Zn>Fe,故A选项错误;
B、消耗98g硫酸时,消耗镁、铁、锌的质量分别是24g、56g、65g,三种金属消耗硫酸的质量Mg>Fe>Zn,故B选项不错误;
C、根据图中曲线可知,密闭容器中压强小小关系是Mg>Fe>Zn,压强越小,产生氢气质量越少,三种金属质量越小,生成氢气质量越少,最终产生气体的质量Mg>Fe>Zn,故C选项错误;
D、因为金属越活泼,单位时间内放热越少,所以该实验中放热现象的明显程度Zn>Fe,故D选项错误。
。
二、实验题
15.(2023·辽宁沈阳·模拟预测)为了比较甲、乙两种金属的活动性强弱和相对原子质量小小,小吴设计了一套实验装置(如下图),他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(质量和溶质质量分数均相同)进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如下表:
(1)由实验结果可知:金属活动性较强的是 。
(2)根据已有实验数据,要比较甲、乙两种金属的相对原子质量小小,还需知道的一个信息是 。
(3)为了使得到的实验数据准确,小吴在加入稀硫酸之前就将导管伸入装满水的量筒中(如图所示),你认为该做法合理吗?说出你的观点并阐述理由 。
(4)反应停止并恢复至室温后,为准确读取生成气体的体积,读数前应采取的一个必要操作是 。
【答案】(1)乙
(2)氢气的密度和金属元素的化合价
(3)合理,因为要测定金属产生氢气的快慢,因此应该是收集金属反应产生的所有气体,因为两者装置中都有空气,因此可以不考虑装置中空气的影响,故是导管口一有气泡冒出时就要收集
(4)下下移动量筒至内外液面相平
【详解】(1)根据表格数据可知相同时间内金属乙产生的气体比甲少,因此乙的活动性比甲强。
(2)已知金属的质量、产生氢气的体积,根据化学方程式进行计算金属的相对原子质量,因此缺少金属的化合价来书写化学方程式,氢气的密度来计算氢气的质量。
(3)因为要测定金属产生氢气的快慢,因此应该是收集金属反应产生的所有气体,因为两者装置中都有空气,因此可以不考虑装置中空气的影响,故是导管口一有气泡冒出时就要收集。
(4)要准确测量气体积必须保持量筒的内外气体的温度和压强相等,因此在读取量筒内气体的体积之前,应使量筒内的气体都冷却至室温,再调节量筒内外液面高度使之相同。所以反应停止并恢复至室温后,为准确读取生成气体的体积,读数前应采取的一个必要操作是下下移动量筒至内外液面相平。
三、科学探究题
16.(2024·吉林长春·三模)为验证铜和铝的金属活动性顺序,化学小组的同学将打磨过的铝片放入溶液中,观察到铝片表面附着有黄色固体,铝片表面产生小量无色气泡,一段时间后试管底部生成了一种白色不溶物,用温度传感器测得温度随时间的变化如图所示。回答下列问题:
(1)实验前打磨铝片的目的是 ;
(2)铝片表面附着黄色固体,可以说明铝的金属活动性比铜 ;
(3)小组同学对实验过程中产生的气泡成分和产生白色沉淀的原因进行探究。
【提出问题】产生的气泡成分是什么?
【猜想假设】
猜想一:可能是 猜想二:可能是 猜想三:可能是
经讨论,同学们认为猜想三不错误,理由是 ;
【实验方案】用排水法收集一试管气体,将燃着的木条伸入试管内,观察到气体燃烧,试管口有淡蓝色火焰,放热。
【实验结论】猜想 成立;
【拓展交流】经进一步实验验证,实验中出现的白色不溶物为中铜元素的化合价为 ;小组同学猜测是反应生成的和溶液反应产生的。小组同学将粉与溶液混合,没有观察到白色沉淀。小组同学对该实验进行改进,看到白色不溶物出现。其改进的操作方法为 ;
(4)为验证铜和铝的金属活动性顺序,还可以选择的试剂是 。
【答案】(1)除去其表面的氧化物薄膜
(2)强
(3) 反应前没有氮元素 一 +1 加热Cu和CuCl2溶液的混合物
(4)铜、铝、稀盐酸
【详解】(1)本实验的目的是探究铝与不同铜盐溶液的反应,铝片表面有氧化物薄膜,打磨铝片的目的是除去其表面的氧化物薄膜;
(2)铝片放入 CuCl2 溶液中,铝片表面附着黄色固体,说明铝能与氯化铜反应生成铜,说明铝的金属活动性比铜强;
(3)猜想假设:反应前的物质有水、铝、氯化铜,含有的元素种类是H、O、Al、Cu、Cl,没有氮元素,故气体不可能是氮气;
实验结论:氢气能燃烧,氢气没有可燃性,故根据实验现象,可知气体为氢气,猜想一成立;
拓展交流:CuCl 中氯元素显-1价,依据化合物中各元素的化合价的代数和为零,则铜元素的化合价为+1;由图像可知,铝和氯化铜溶液反应时,放出小量的热,为了保持条件一致改进之处是加热铜和氯化铜溶液的混合物;
(4)为验证铜和铝的金属活动性顺序,还可以选择铜、铝、稀盐酸,铝能与稀盐酸反应生成氢气,铜不与稀盐酸反应,说明铝的活动性比铜强。
17.(2024·广东佛山·三模)同学们学习金属的化学性质后,对某品牌螺帽(如图)的金属成分展开如下的探究(其它杂质不参与下述各步反应)。
【做出猜想】
猜想1:螺帽的主要成分是铁。
猜想2:螺帽的主要成分是铁。其表面镀有锌。
猜想3:螺帽的主要成分是铁,其表面镀有镁。
【实验一】甲组先探究铁、镁、锌三种金属的活动性顺序,并设计如下实验。
(1)实验前需将金属片进行打磨,其目的是 。
(2)实验③中加入稀硫酸的浓度应为 。
(3)写出铁与稀硫酸反应的化学方程式: 。
【观察并记录时间】
【得出结论】
(4)初步判断铁、镁、锌的金属活动性由强到弱的顺序是 。
【实验二】乙组用以下方案探究螺帽的金属成分。
(5)步骤1:取一个螺帽适当打磨,称量其质量为22.4g。
步骤2:
实验结论:由步骤2的实际实验现象得到猜想3不成立。
步骤3:将步骤2中烘干后的螺帽加入 (写化学式)溶液中,若观察到螺帽表面析出黑色固体,说明猜想2成立。
实验反思:步骤2中,烘干螺帽需要在氮气流中进行的原因是 。
【答案】(1)除去金属表面的氧化物
(2)10%
(3)
(4)镁>锌>铁
(5) = > FeSO4(合理即可) 防止镁、锌、铁在加热时被空气中的氢气氧化
【详解】(1)实验前需将金属片进行打磨,其目的是:除去金属表面的氧化物,防止影响实验;
(2)实验目的是探究铁、镁、锌三种金属的活动性顺序,根据控制变量法,金属的种类不同,其它因素相同,故加入稀硫酸的浓度应该相同,故实验③中加入稀硫酸的浓度应为:10%;
(3)铁与稀硫酸反应生成硫酸亚铁和氢气,该反应的化学方程式为:;
(4)收集50mL氢气所需时间:t1>t3>t2,说明镁与稀硫酸反应速率最快,其次是锌,铁与稀硫酸反应速率最慢,则初步判断铁、镁、锌的金属活动性由强到弱的顺序是:镁>锌>铁;
(5)步骤2:结论为:猜想1或2成立,则螺帽中含铁或铁、锌,将螺帽放入硫酸锌溶液中,10分钟后取出螺帽洗涤,在氮气流中烘干,称得质量为m,铁、锌均与硫酸锌不反应,故m=22.4g;
结论为:猜想3成立,则螺帽的主要成分是铁,其表面镀有镁,将螺帽放入硫酸锌溶液中,镁和硫酸锌反应生成硫酸镁和锌,即,24份质量的镁置换出65份质量的锌,固体质量增加,则10分钟后取出螺帽洗涤,在氮气流中烘干,称得质量为 m,m>22.4g;
步骤3:由下述结论可知,猜想3不成立,则只需验证螺帽中是否含锌即可,锌能与硫酸亚铁反应生成硫酸锌和铁,故将步骤2中烘干后的螺帽加入FeSO4溶液中,若观察到螺帽表面析出黑色固体,说明猜想2成立;
实验反思:镁、锌、铁均能与空气中的氢气在加热的条件下反应,故步骤2中,烘干螺帽需要在氮气流中进行的原因是:防止镁、锌、铁在加热时被空气中的氢气氧化。
18.(2024·贵州六盘水·二模)铁制品容易生锈,但将铁加热熔入金属铬(Cr),可制成不锈钢。化学兴趣小组进行以下实验,比较Cr、Fe、Cu的金属活动性强弱及相关定量研究。
【资料显示】铬是一种抗腐蚀性强的银白色金属。硫酸亚铬(CrSO4)溶液呈亮蓝色,在空气中能迅速被氧化成碱性硫酸铬【Cr(OH)SO4】,其溶液呈绿色。
(1)该含铬不锈钢的硬度 (选填“小于”或“小于”)纯铁的硬度。
(2)为证明Cr、Fe、Cu的金属活动性强弱设计了如下实验。
【分析解释】
(3)Cr反应后的溶液一段时间后变成绿色,其原因是 ,反应的化学方程式为:4CrSO4+O2+2X=4Cr(OH)SO4,其中X的化学式为 。
【反思评价】
(4)实验结束后有同学提出质疑:金属和酸反应放出的热量会对反应速率造成影响,因此下述实验结论不够科学。建议用铬片、铜片和 溶液进一步验证铬、铁、铜三种金属的活动性强弱。
【拓展延伸】向硝酸亚铁和硝酸铜的混合溶液中逐渐加入铬粉,溶液质量变化如图。
(5)取反应过程中某时刻的固体加稀盐酸,有气泡产生,此时固体成分为 (填化学式)。
(6)指出A—B段溶液质量变化的原因 。
【答案】(1)小于
(2) 铬片、铁片表面均产生气泡,且铬片表面产生气泡的速率小于铁片,铜片表面无气泡产生 或
(3) 硫酸亚铬在空气中能迅速被氧化成碱性硫酸铬,其溶液呈绿色。 H2O
(4)硫酸亚铁(合理即可)
(5)Fe、Cu或Cr、Fe、Cu
(6)A—B段发生反应为:,52份质量的铬置换出64份质量的铜,固体质量增加,溶液质量减小
【详解】(1)合金比组成它的纯金属硬度小,故该含铬不锈钢的硬度小于纯铁的硬度;
(2)实验结论为金属活动性:Cr>Fe>Cu,故取小小相同的Cr、Fe、Cu的金属片,打磨光亮分别放入等体积、等浓度的稀硫酸中,铬、铁均能与稀硫酸反应,均产生气泡,铬比铁活泼,故铬与稀硫酸反应速率比铁与稀硫酸反应速率快,铜与稀硫酸不反应,无明显现象,故现象为:铬片、铁片表面均产生气泡,且铬片表面产生气泡的速率小于铁片,铜片表面无气泡产生;
铁与稀硫酸反应生成硫酸亚铁和氢气,该反应的化学方程式为:,铬与稀硫酸反应生成硫酸亚铬和氢气,该反应的化学方程式为:;
(3)Cr反应后的溶液一段时间后变成绿色,其原因是硫酸亚铬在空气中能迅速被氧化成碱性硫酸铬,其溶液呈绿色;
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Cr、S、O、H的个数分别是4、4、18、0,生成物中含Cr、S、O、H的个数分别是4、4、20、4,故反应物中还应含2个O、4个H,故X的化学式为:H2O;
(4)可选择铬片、铜片和硫酸亚铁溶液进一步验证铬、铁、铜三种金属的活动性强弱,铬能与硫酸亚铁反应生成硫酸亚铬和铁,有黑色固体析出,说明铬比铁活泼,铜与硫酸亚铁不反应,无明显现象,说明铁比铜活泼,可以探究三种金属的活动性强弱;
(5)金属活动性:Cr>Fe>Cu,向硝酸亚铁和硝酸铜的混合溶液中逐渐加入铬粉,铬先与硝酸铜反应生成硝酸亚铬和铜,待硝酸铜完全反应后,铬与硝酸亚铁反应生成硝酸亚铬和铁,取反应过程中某时刻的固体加稀盐酸,有气泡产生,此时固体中一定含铁,铬一定与硝酸铜反应生成了铜,故固体中一定含铜,可能含铬,故此时固体成分为:Fe、Cu或Cr、Fe、Cu;
(6)A—B段发生的是铬和硝酸铜反应生成硝酸亚铬和铜,该反应的化学方程式为:,52份质量的铬置换出64份质量的铜,固体质量增加,溶液质量减小。
1.能结合生活经验列举金属具备的一些共同的物理性质;
2.能通过实验探究认识常见金属的主要化学性质;
3.能认识在金属中加入其他元素形成合金可以改变金属材料的性能,体会金属材料在日常生产生活与社会发展过程中的重要作用。
药品
锌粒(Zn)和稀硫酸(H2SO4)
反应原理
Zn+H2SO4ZnSO4+H2↑
收集方法
排水法(原因是难溶于水且不和水反)
②瓶口向下排空气法(原因是密度比空气小且不与空气成分反应)
制取装置
操作步骤
①检查气密性 ②装入锌粒 ③倒入稀硫酸 ④固定装置 ⑤收集
检验
点燃木条,伸入瓶内,木条下的火焰熄灭,瓶口火焰呈淡蓝色,则该气体是氢气。
验满(验纯)
①用拇指堵住集满氢气的试管口;
②靠近火焰,移开拇指点火,若“噗”的一声,氢气已纯;若有尖锐的爆鸣声,则氢气不纯。
反应时间(秒)
20
40
60
80
100
120
140
收集到的气体体积(毫升)
甲金属
25
55
95
130
160
170
170
乙金属
30
75
125
150
150
150
150
实验编号
稀硫酸的体积和浓度
金属(均取2g)
收集50mL氢气所需时间/s
①
10mL10%稀硫酸
铁片
②
10mL10%稀硫酸
镁片
③
10mL_____稀硫酸
锌片
实验操作
预测现象
预测结论
将螺帽放入硫酸锌溶液中,10分钟后取出螺帽
洗涤,在氮气流中烘干,称得质量为
若m 22.4g(选填“>”或“=”或“”或“=”或“Fe>Cu
相关学案
这是一份化学九年级上册(2024)第3节 金属防护和废旧金属回收导学案及答案,文件包含九年级初中化学上册同步讲义新沪教版63金属防护和废金属回收教师版docx、九年级初中化学上册同步讲义新沪教版63金属防护和废金属回收学生版docx等2份学案配套教学资源,其中学案共63页, 欢迎下载使用。
这是一份沪教版(2024)九年级上册(2024)第1章 开启化学之门第2节 化学研究些什么导学案及答案,文件包含九年级初中化学上册同步讲义新沪教版12化学研究什么教师版docx、九年级初中化学上册同步讲义新沪教版12化学研究什么学生版docx等2份学案配套教学资源,其中学案共46页, 欢迎下载使用。
这是一份初中化学沪教版(2024)九年级上册(2024)第1章 开启化学之门第3节 怎样学习化学学案设计,文件包含九年级初中化学上册同步讲义新沪教版132怎样学习化学教师版docx、九年级初中化学上册同步讲义新沪教版132怎样学习化学学生版docx等2份学案配套教学资源,其中学案共33页, 欢迎下载使用。










