






还剩13页未读,
继续阅读
浙教版九年级科学上册同步精品课堂 专题3:物质的分离与除杂(课件)
展开
这是一份浙教版九年级科学上册同步精品课堂 专题3:物质的分离与除杂(课件),共21页。
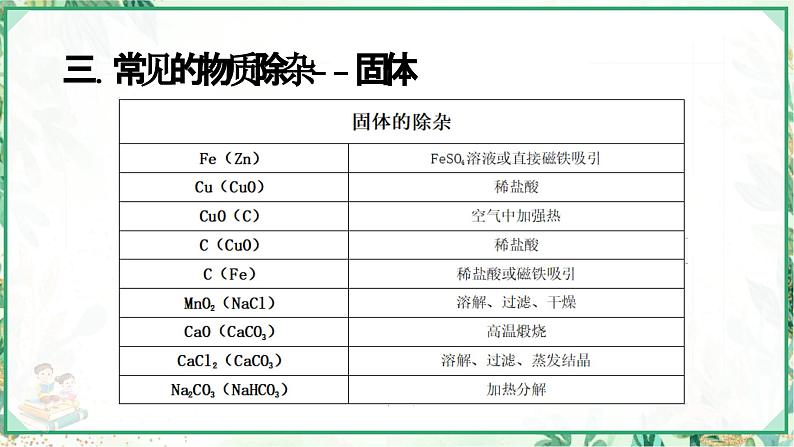
九年级科学第一章物质及其变化专题三物质的分离与除杂课堂导入 生活中我们两种物质混合在一起,我们有时候要想办法将他们分开,比如稻谷里有米糠,我们采取风车吹让他们分开,那化学物质混合后我们要怎么分开呢?01知识点分析基础知识点的罗列和例题难点易错点和知识点总结一.物质的分离与除杂1.物质的分离:通过特定的方式将不同的物质分开的过程。2.物质的除杂:利用特定的方式除去原物质中的杂质。3.除杂的原则:(1)不增:不引入新的杂质,注意适量等关键词(2)不减:不减少被除杂的物质(主要是化学方法,物理方法可能会减少)(3)简单易分离:操作尽可能简单,分离尽力简单(4)除尽:杂质需要彻底清除干净二.除杂的方法--物理方法(1)过滤:分离不溶性固体与液体的方法,如氯化钙溶液中有碳酸钙(2)冷却结晶:溶解度随温度变化比较大的,如硝酸钾中有氯化钠 蒸发结晶:溶解度随温度变化比较小的,如氯化钠中有硝酸钾(3)磁铁吸引:分离有无磁性的物体,如铜粉中有铁粉(4)挥发或汽化:加热除去溶液中的HCl,蒸干得到固体(5)蒸馏:分离沸点不同的液体,分离液态空气法制氧气(工业制氧)(6)吸附:活性炭的吸附性(7)物理吸收:浓硫酸和固体氢氧化钠或氯化钙吸水二.除杂的方法--化学方法(1)热分解法:加热分解固体 如碳酸钠中有碳酸氢钠,氧化钙里有碳酸钙(2)洗气法(最干净的除气体杂质):利用化学物质吸收,如氢氧化钠吸收二氧化硫,氯化氢,二氧化碳(3)化气法:将杂质变成气体除去,氯化钠溶液中有碳酸钠,加盐酸(4)沉淀法:将杂质变成沉淀除去,如氢氧化钠溶液中有碳酸钠,加氢氧化钙(5)溶解法:将杂质溶解,如硫酸钡中有碳酸钡,加盐酸使其溶解(6)转化法:将杂质转化为需要的物质,如氢氧化钙中有氧化钙,加水三.常见的物质除杂--气体三.常见的物质除杂--固体三.常见的物质除杂--溶液02典例精析精选近年各地中考、一模以及名校练习等好题进行分析【2020·杭州模拟】下列关于物质除杂所用的试剂和方法错误的是( ) 【答案】B【2020·嘉兴模拟】下列除去杂质的方法中,正确的是( ) 【答案】A【2021·宁波一模】下列实验方法不能达到实验目的的是( ) 【答案】A【2020·宁波一模】某CO气体中含有少量的CO2和H2O,为了得到纯净、干燥的CO,除杂装置(如图)的导管按气流方向连接顺序是( )A.a→b→c→d B.b→a→d→ C.c→d→b→a D.d→c→b→a【答案】C【2020·杭州模拟】 下列物质的鉴别、除杂(括号中为杂质)的方法中,选用试剂或方法不合理的是( )A.鉴别铝、铁、铜三种金属:加入等体积、等浓度的稀硫酸,观察现象B.鉴别硝酸铵、碳酸钙、硫酸铜:加入足量的水C.NaCl溶液(Na2SO4):加入过量的BaCl2溶液D.CO2(HCl):通入足量的硝酸银溶液【答案】C【2020·湖州二模】下列除去杂质的方法中正确的是( ) 【答案】B【2020·杭州模拟】医用氯化钙可用于补钙、抗过敏等。生产医用的二水合氯化钙(),常以工业碳酸钙(含少量杂质铝离子、铁离子)为原料,主要经过溶解、除杂、过滤、酸化、蒸发结晶等过程,其工艺流程如下图所示:(1)在溶解和酸化的操作过程中,加入的酸是___________。(2)除杂操作的方法是加入适量的氢氧化钙,然后将所得沉淀过滤,滤渣中一定有的成分是___________(填化学式)。【答案】 盐酸 Fe(OH)3、Al(OH)3【2020·宁波模拟】大理石中含少量硫化物,使制得的CO2中混有H2S气体。小科欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:查阅资料:Ⅰ.H2S能与NaOH等碱溶液或CuSO4溶液反应。Ⅱ.CO2中混有的HCl气体可用饱和NaHCO3溶液吸收。(1)图甲装置①中所盛试剂应选用_____(填字母)。A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液(2)为证明CO2和NaOH能发生反应,小科重新设计了图乙所示的方案。则图乙方案中所加的试剂X应该是_____。【答案】 D BaCl2【2022·杭州模拟】在除杂质的操作中,为了将杂质完全去除,通常需加入过量的除杂试剂。为了除去 NaCl 样品中混有的少量 Na2SO4和 MgCl2,某校化学课外活动小组设计的提纯 NaCl的流程如图所示:(1) 加入过量的氢氧化钠可除去的阳离子是_________(写离子符号)。(2) 试剂 X 的化学式为________,溶液 M 中所含有的阴离子有_________。(3) 某同学用提纯得到的 NaCl晶体配制一定溶质质量分数的氯化钠溶液, 在量取液体时仰视读数, 会导致所配制溶液的溶质质量分数偏________(填 “大”或 “小”)。【答案】 Mg2+ Na2CO3 、Cl-、OH- 小【2020·杭州二模】实验室用大理石和稀盐酸制取二氧化碳时,因大理石中含少量硫化物,使制得的CO2中混有H2S等气体。为了获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:查阅资料:I、H2S能与NaOH等碱溶液、CuSO4溶液反应。Ⅱ、CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。(1)图1中装置甲所盛试剂是___________(填字母)。A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液(2)图1装置中丙的作用是___________。(3)为证明CO2和NaOH能发生反应,小高重新设计了图2所示的方案。则图2方案中所加试剂X应该是___________。【答案】 D 除去水蒸气 氯化钡溶液【2020·金华二模】通过海水晒制可得粗盐,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质.以下是一种由粗盐制备精盐的实验方案流程图:分析该流程图,回答下列问题:(1)试剂X为________(填写化学式). (2)试剂Y为 ________.(填写化学式). (3)操作Z为 ________. (4)选择的除杂的试剂不能用KOH代替NaOH溶液,理由是________.【答案】 Na2CO3 HCl 蒸发结晶 会引进新的杂质KCl
九年级科学第一章物质及其变化专题三物质的分离与除杂课堂导入 生活中我们两种物质混合在一起,我们有时候要想办法将他们分开,比如稻谷里有米糠,我们采取风车吹让他们分开,那化学物质混合后我们要怎么分开呢?01知识点分析基础知识点的罗列和例题难点易错点和知识点总结一.物质的分离与除杂1.物质的分离:通过特定的方式将不同的物质分开的过程。2.物质的除杂:利用特定的方式除去原物质中的杂质。3.除杂的原则:(1)不增:不引入新的杂质,注意适量等关键词(2)不减:不减少被除杂的物质(主要是化学方法,物理方法可能会减少)(3)简单易分离:操作尽可能简单,分离尽力简单(4)除尽:杂质需要彻底清除干净二.除杂的方法--物理方法(1)过滤:分离不溶性固体与液体的方法,如氯化钙溶液中有碳酸钙(2)冷却结晶:溶解度随温度变化比较大的,如硝酸钾中有氯化钠 蒸发结晶:溶解度随温度变化比较小的,如氯化钠中有硝酸钾(3)磁铁吸引:分离有无磁性的物体,如铜粉中有铁粉(4)挥发或汽化:加热除去溶液中的HCl,蒸干得到固体(5)蒸馏:分离沸点不同的液体,分离液态空气法制氧气(工业制氧)(6)吸附:活性炭的吸附性(7)物理吸收:浓硫酸和固体氢氧化钠或氯化钙吸水二.除杂的方法--化学方法(1)热分解法:加热分解固体 如碳酸钠中有碳酸氢钠,氧化钙里有碳酸钙(2)洗气法(最干净的除气体杂质):利用化学物质吸收,如氢氧化钠吸收二氧化硫,氯化氢,二氧化碳(3)化气法:将杂质变成气体除去,氯化钠溶液中有碳酸钠,加盐酸(4)沉淀法:将杂质变成沉淀除去,如氢氧化钠溶液中有碳酸钠,加氢氧化钙(5)溶解法:将杂质溶解,如硫酸钡中有碳酸钡,加盐酸使其溶解(6)转化法:将杂质转化为需要的物质,如氢氧化钙中有氧化钙,加水三.常见的物质除杂--气体三.常见的物质除杂--固体三.常见的物质除杂--溶液02典例精析精选近年各地中考、一模以及名校练习等好题进行分析【2020·杭州模拟】下列关于物质除杂所用的试剂和方法错误的是( ) 【答案】B【2020·嘉兴模拟】下列除去杂质的方法中,正确的是( ) 【答案】A【2021·宁波一模】下列实验方法不能达到实验目的的是( ) 【答案】A【2020·宁波一模】某CO气体中含有少量的CO2和H2O,为了得到纯净、干燥的CO,除杂装置(如图)的导管按气流方向连接顺序是( )A.a→b→c→d B.b→a→d→ C.c→d→b→a D.d→c→b→a【答案】C【2020·杭州模拟】 下列物质的鉴别、除杂(括号中为杂质)的方法中,选用试剂或方法不合理的是( )A.鉴别铝、铁、铜三种金属:加入等体积、等浓度的稀硫酸,观察现象B.鉴别硝酸铵、碳酸钙、硫酸铜:加入足量的水C.NaCl溶液(Na2SO4):加入过量的BaCl2溶液D.CO2(HCl):通入足量的硝酸银溶液【答案】C【2020·湖州二模】下列除去杂质的方法中正确的是( ) 【答案】B【2020·杭州模拟】医用氯化钙可用于补钙、抗过敏等。生产医用的二水合氯化钙(),常以工业碳酸钙(含少量杂质铝离子、铁离子)为原料,主要经过溶解、除杂、过滤、酸化、蒸发结晶等过程,其工艺流程如下图所示:(1)在溶解和酸化的操作过程中,加入的酸是___________。(2)除杂操作的方法是加入适量的氢氧化钙,然后将所得沉淀过滤,滤渣中一定有的成分是___________(填化学式)。【答案】 盐酸 Fe(OH)3、Al(OH)3【2020·宁波模拟】大理石中含少量硫化物,使制得的CO2中混有H2S气体。小科欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:查阅资料:Ⅰ.H2S能与NaOH等碱溶液或CuSO4溶液反应。Ⅱ.CO2中混有的HCl气体可用饱和NaHCO3溶液吸收。(1)图甲装置①中所盛试剂应选用_____(填字母)。A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液(2)为证明CO2和NaOH能发生反应,小科重新设计了图乙所示的方案。则图乙方案中所加的试剂X应该是_____。【答案】 D BaCl2【2022·杭州模拟】在除杂质的操作中,为了将杂质完全去除,通常需加入过量的除杂试剂。为了除去 NaCl 样品中混有的少量 Na2SO4和 MgCl2,某校化学课外活动小组设计的提纯 NaCl的流程如图所示:(1) 加入过量的氢氧化钠可除去的阳离子是_________(写离子符号)。(2) 试剂 X 的化学式为________,溶液 M 中所含有的阴离子有_________。(3) 某同学用提纯得到的 NaCl晶体配制一定溶质质量分数的氯化钠溶液, 在量取液体时仰视读数, 会导致所配制溶液的溶质质量分数偏________(填 “大”或 “小”)。【答案】 Mg2+ Na2CO3 、Cl-、OH- 小【2020·杭州二模】实验室用大理石和稀盐酸制取二氧化碳时,因大理石中含少量硫化物,使制得的CO2中混有H2S等气体。为了获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:查阅资料:I、H2S能与NaOH等碱溶液、CuSO4溶液反应。Ⅱ、CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。(1)图1中装置甲所盛试剂是___________(填字母)。A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液(2)图1装置中丙的作用是___________。(3)为证明CO2和NaOH能发生反应,小高重新设计了图2所示的方案。则图2方案中所加试剂X应该是___________。【答案】 D 除去水蒸气 氯化钡溶液【2020·金华二模】通过海水晒制可得粗盐,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质.以下是一种由粗盐制备精盐的实验方案流程图:分析该流程图,回答下列问题:(1)试剂X为________(填写化学式). (2)试剂Y为 ________.(填写化学式). (3)操作Z为 ________. (4)选择的除杂的试剂不能用KOH代替NaOH溶液,理由是________.【答案】 Na2CO3 HCl 蒸发结晶 会引进新的杂质KCl
相关资料
更多









