






初中化学人教版(2024)九年级上册(2024)第五单元 化学反应的定量关系课题2 化学方程式教学演示ppt课件
展开复习:请写出氢气燃烧的化学方程式,并回顾 方程式所表示的意义
宏观:每4份质量的氢气与32份质量的氧气恰好 完全反应,生成36份质量的水
微观:每2个氢分子与1个氧分子恰好完全反应, 生成2个水分子。
计算:磷在空气中燃烧反应中反应物与生成物之间的质量比
4 P + 5 O2 ====== 2 P2O5
4×31 :16×10 : 31×4 + 16×10
124 : 160 : 284
若: 124克 ( )克 : ( )克
若: ( )克 : ( )克 : 142 克
利用化学方程式的简单计算
在化学反应中,反应物与生成物之间的质量比是成正比例关系。因此,利用正比例关系根据化学方程式中已知的一种反应物(或生成物)的质量,可出求生成物或反应物的量)。
计算依据:化学方程式中各物质的质量比 (即质量守恒定律)
例1 加热分解6.3g高锰酸钾,可以得到多少克氧气?
解:设可以得到氧气的质量为x
3.写出相对分子质量以及已知量、未知量
答:可以得到0.6克氧气
三个要领: ①步骤要完整; ②格式要规范; ③得数要准确。 三个关键: ①准确书写化学式; ②化学方程式要配平; ③准确计算式量并找准关系。
小结:化学方程式的计算
⑴设未知量时一定要注意质量单位,已知量和未知量单位不一致的一定要进行单位换算,单位必须一致才能计算。⑵写出方程式要注意配平,而且要注意方程式的完整,反应条件、气体和沉淀的符号要注意标明。
⑶相关物质的相对分子质量写在相应化学式的下面,一定要注意用相对分子质量乘以化学式前面的系数,已知量和未知量写在相应相对分子质量的下边。⑷计算结果的小数位保留按题中要求进行,若题中没有要求,一般保留一位小数。
③找出已知量和 未知量的关系
⑥回顾检查
化学方程式计算的四种类型
1.已知反应物的质量求生成物的质量;2.已知生成物的质量求反应物的质量;3.已知一种反应物的质量求另一种反应物的质量;4.已知一种生成物的质量求另一种生成物的质量。
例2:工业上,高温煅烧石灰石(主要成分碳酸钙)可制得生石灰(氧化钙)和二氧化碳。如果要制取10吨氧化钙,需要碳酸钙的质量是多少?
[解] 设需要碳酸钙的质量为x。
答:需要碳酸钙18t。
有关不纯反应物或生成物的计算。
1.化学反应方程式中不管是反应物还是生成物,代入的都是纯物质的质量.如果遇到不纯反应物或生成物,应将不纯物质换算成纯物质的质量.
2.不纯物质和纯物质质量间的换算.
纯物质的质量 = 不纯物质的质量 ×纯度(即:质量分数)
例题3、高温煅烧含杂质10%的石灰石(主要成分为CaCO3)100吨,可得生石灰( CaO)多少吨?
解:设可得生石灰质量为x
100t ×(1-10%)
答:可得生石灰50.4吨。
关于质量和体积间的换算
注意;涉及气体体积时,质量与体积之间的换算:质量 = 密度×体积 体积 = 质量÷密度
例题 4、足量的镁带在标准状况下与11.2升的氧气(密度为1.43g/L) 充分燃烧,可以生成多少克氧化镁?
解:设可生成氧化镁的质量为X
32 8016克 X
------ = ------
答:充分燃烧后可生成氧化镁 40 克。
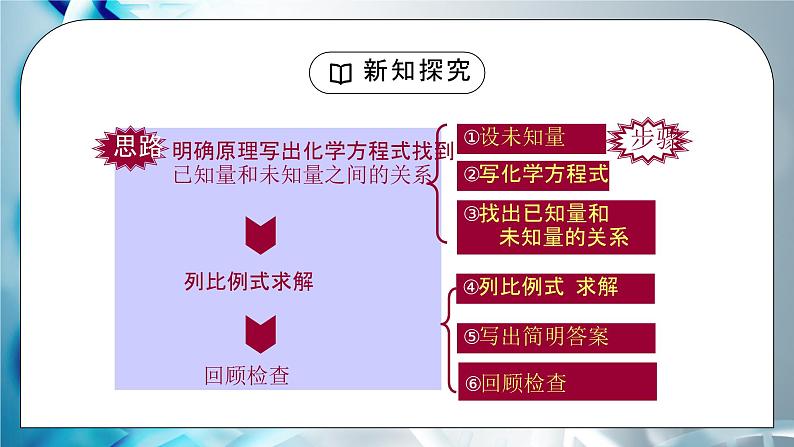
根据化学方程式进行计算的步骤(1)设未知量(2)写出反应的化学方程式(3)计算相关物质的质量比(4)标出已知量、未知量(5)列比例式(6)解比例式(7)简明地写出答语
1、实验室中用石灰石(主要成分是C aCO3)与稀盐酸制CO2,发生的反应为:CaCO3+2HCl===CaCl2+H2O+CO2↑请你计算,50 g CaCO3与足量的稀盐酸完全反应,理论上可制得CO2多少克?
解:设理论上可制得CO2的质量为x。
答:理论上可制得CO2 22g。
CaCO3+2HCl===CaCl2+H2O+CO2↑
2、根据质量守恒定律及2Mg+O2 2MgO的反应方程式,下列各组数据依次为m(Mg)、m(O2)、m(MgO)的质量,其中正确的是( )A.2g、3g、5g B.3g、2g、5g C.1g、4g、5g D.4g、1g、5g3、9g碳与16g氧气在密闭容器中点燃,充分反应,生成二氧化碳的质量是( ) A. 11g B. 22g C. 25g D. 33g
解:设制取9.6g氧气需要过氧化氢的质量为X
68 32
X 9.6g
答:制取9.6g氧气需要20.4g过氧化氢,生成水10.8g。
生成水的质量=20.4g-9.6g=10.8g
4、实验室要用9.6g氧气做实验。小红同学提议利用分解过氧化氢的方法来制取氧气。那么,至少需要准备多少过氧化氢?生成水多少?
5、工业上用磁铁矿石炼铁,其反应原理为:Fe3O4+4CO 3Fe+4CO2。用100t含四氧化三铁58%的磁铁矿石,理论上能炼出纯铁的质量是多少(要求根据化学方程式进行计算)?
解:100 t该磁铁矿石中Fe3O4的质量为:100 t×58%=58t 设理论上能炼出纯铁的质量为x
Fe3O4+4CO 3Fe+4CO2
答:理论上能炼出纯铁的质量是42t。
232 16858t x
6、氢气是理想的高能燃料,其燃烧产物对环境无污染。若充分燃烧8 g氢气,在标准状况下,最少需要氧气多少升(标准状况 下氧气的密度约为1.43 g/L)?
设需要氧气的质量为x。2H2+O2 2H2O4 328 g x4/32 =8g/XX=64 g氧气的体积为 64 g÷1.43 g/L≈44.8 L答:需要氧气的体积为44.8 L。
化学课题 3 利用化学方程式的简单计算作业课件ppt: 这是一份化学课题 3 利用化学方程式的简单计算作业课件ppt,共9页。PPT课件主要包含了写出计算过程,图K5-3-2等内容,欢迎下载使用。
初中化学人教版九年级上册课题 3 利用化学方程式的简单计算作业ppt课件: 这是一份初中化学人教版九年级上册课题 3 利用化学方程式的简单计算作业ppt课件,共7页。PPT课件主要包含了MOH,图K5-3-1等内容,欢迎下载使用。
人教版九年级上册课题 3 利用化学方程式的简单计算教学课件ppt: 这是一份人教版九年级上册课题 3 利用化学方程式的简单计算教学课件ppt,共20页。PPT课件主要包含了课程要求,课前预习,知识点精讲,课堂检测,96g,图5-3-1,课堂练习,图5-3-2,x=316g,量分数是903%等内容,欢迎下载使用。













