四川省绵竹市2024届中考第二次诊断考试化学试卷(含答案)
展开一、单选题
1.以下劳动实践活动中发生了化学变化的是( )
A.用漏勺从锅中捞取饺子B.用盐酸除去铁架台上的铁锈
C.用活性炭作简易净水器D.用氯化钠和蒸馏水配制生理盐水
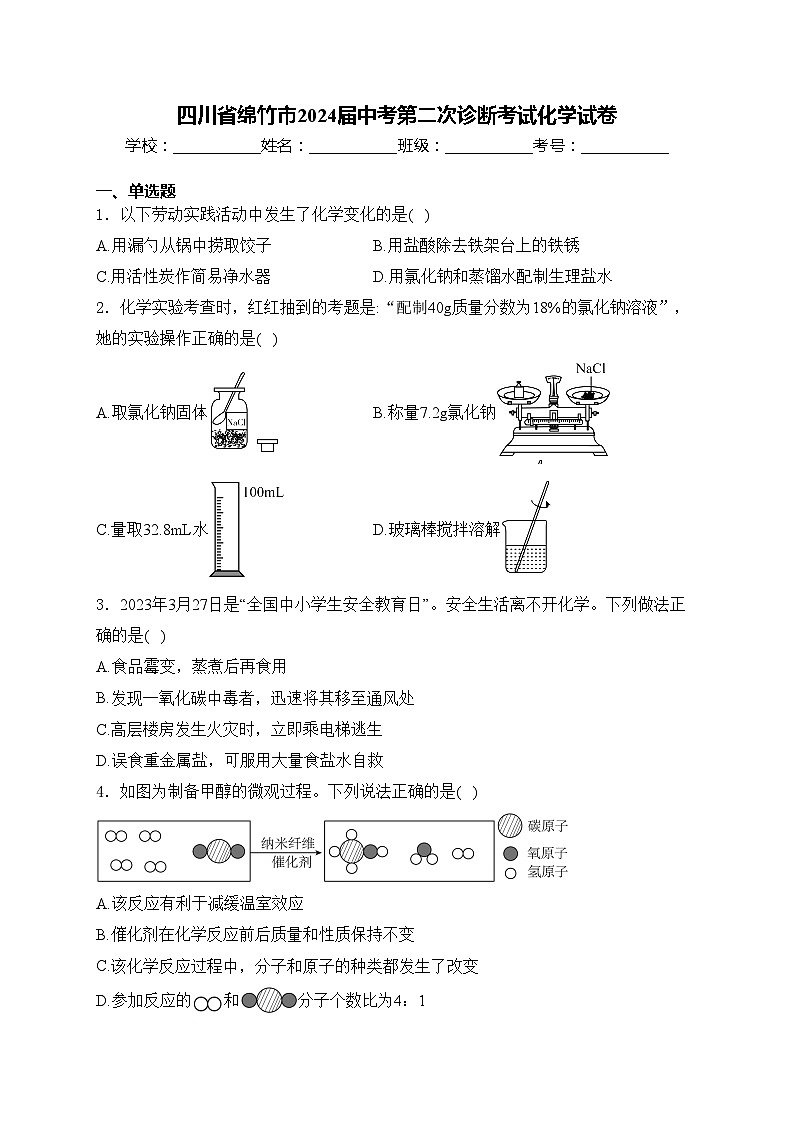
2.化学实验考查时,红红抽到的考题是:“配制40g质量分数为18%的氯化钠溶液”,她的实验操作正确的是( )
A.取氯化钠固体B.称量7.2g氯化钠
C.量取32.8mL水D.玻璃棒搅拌溶解
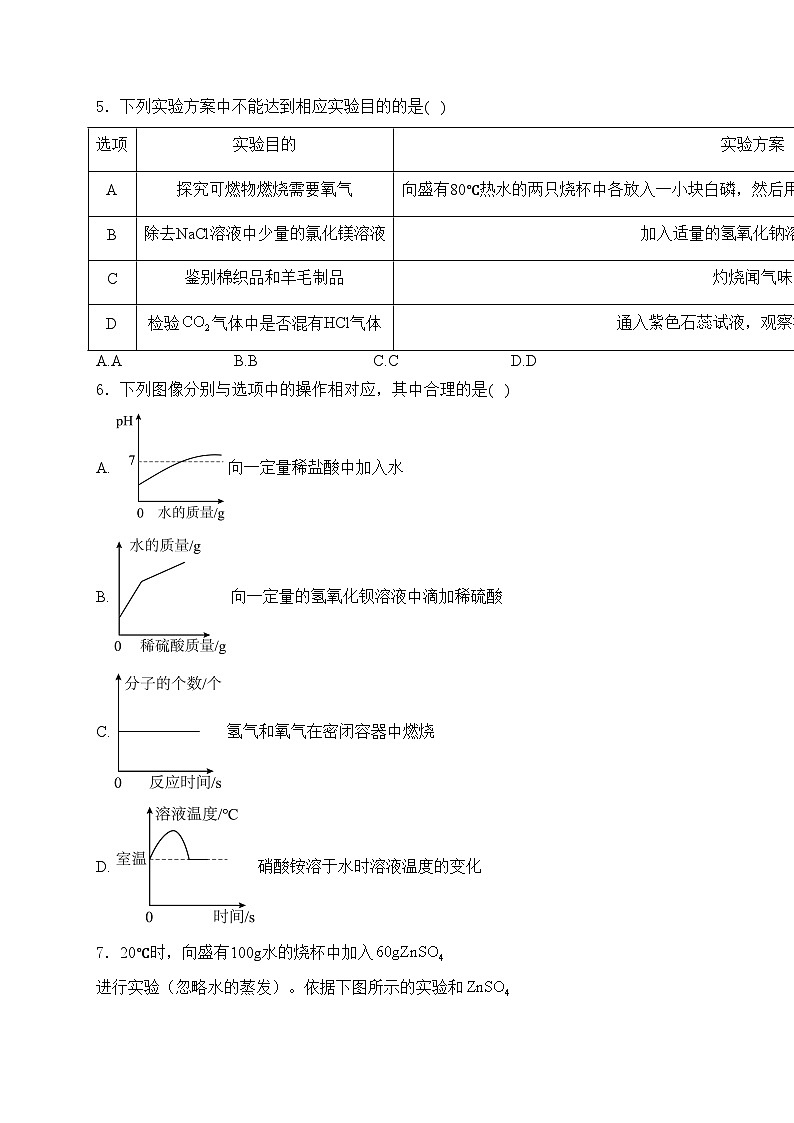
3.2023年3月27日是“全国中小学生安全教育日”。安全生活离不开化学。下列做法正确的是( )
A.食品霉变,蒸煮后再食用
B.发现一氧化碳中毒者,迅速将其移至通风处
C.高层楼房发生火灾时,立即乘电梯逃生
D.误食重金属盐,可服用大量食盐水自救
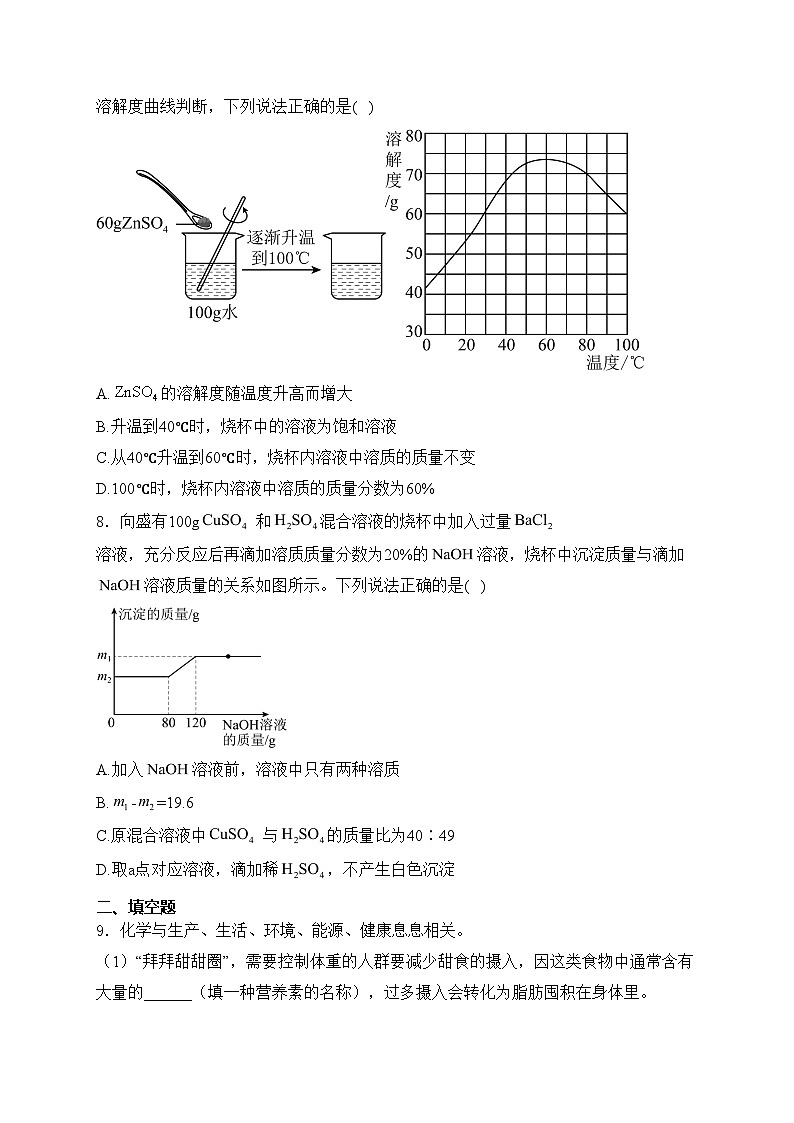
4.如图为制备甲醇的微观过程。下列说法正确的是( )
A.该反应有利于减缓温室效应
B.催化剂在化学反应前后质量和性质保持不变
C.该化学反应过程中,分子和原子的种类都发生了改变
D.参加反应的和分子个数比为4:1
5.下列实验方案中不能达到相应实验目的的是( )
A.AB.BC.CD.D
6.下列图像分别与选项中的操作相对应,其中合理的是( )
A.向一定量稀盐酸中加入水
B.向一定量的氢氧化钡溶液中滴加稀硫酸
C.氢气和氧气在密闭容器中燃烧
D.硝酸铵溶于水时溶液温度的变化
7.20℃时,向盛有100g水的烧杯中加入进行实验(忽略水的蒸发)。依据下图所示的实验和溶解度曲线判断,下列说法正确的是( )
A.的溶解度随温度升高而增大
B.升温到40℃时,烧杯中的溶液为饱和溶液
C.从40℃升温到60℃时,烧杯内溶液中溶质的质量不变
D.100℃时,烧杯内溶液中溶质的质量分数为60%
8.向盛有100g和混合溶液的烧杯中加入过量溶液,充分反应后再滴加溶质质量分数为20%的溶液,烧杯中沉淀质量与滴加溶液质量的关系如图所示。下列说法正确的是( )
A.加入溶液前,溶液中只有两种溶质
B.-=19.6
C.原混合溶液中与的质量比为40∶49
D.取a点对应溶液,滴加稀,不产生白色沉淀
二、填空题
9.化学与生产、生活、环境、能源、健康息息相关。
(1)“拜拜甜甜圈”,需要控制体重的人群要减少甜食的摄入,因这类食物中通常含有大量的______(填一种营养素的名称),过多摄入会转化为脂肪囤积在身体里。
(2)中国高铁车身主要采用的镍铬奥氏体不锈钢属于______材料。
(3)液氨有望成为新一代的绿色能源。氨气()在氧气中燃烧时可释放大量热,且生成氮气和水,请写出该反应的化学方程式______。
10.二氧化氯()可用于自来水消毒。以粗盐为原料生产的工艺主要包括:
①反应I是粗盐除杂;
②反应II是特殊条件下电解NaCl溶液制;
③反应Ⅲ是的制取。其中反应Ⅲ制取的化学方程式为:。
工艺流程如图,
(1)二氧化氯()中Cl的化合价为______。
(2)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,请写出其中所发生的中和反应的化学方程式:______。
(3)该流程中可循环利用的物质是水和______。
11.A~J分别为初中化学常见的十种物质,它们存在下图所示的转化关系。已知A为铁锈的主要成分,H的溶液呈蓝色,I为黑色固体,H的相对分子质量是I的两倍。常温下B、D、F、J均为无色气体,其中J是一种有刺激性气味的气体,其水溶液显碱性。(反应②、④的个别生成物已略去)
(1)写出D物质的化学式:D______。
(2)W组成中含有的阳离子是______(填离子符号)。
(3)反应②的基本反应类型是______反应。
(4)反应⑤的化学方程式为______。
三、实验题
12.化学是以实验为基础的学科,开展实验探究是学习化学的重要手段。
【实验探究一】
(1)写出仪器X名称______。
(2)实验室用装置B制取氧气,反应的化学方程式为______。若用F装置干燥实验室制取的二氧化碳,F中应盛有的药品名称为______。
(3)若用F装置收集氧气,验满方法是描述操作、现象和结论______。
【实验探究二】
通常情况下,1L水约能溶解。按如图所示装置进行与NaOH反应探究(装置气密性良好)。实验步骤为:打开止水夹K,将注射器乙中气体全部注入到盛有2mL40%的NaOH溶液(足量)的注射器甲中、关闭止水夹K,充分振荡。
(4)在整个实验过程中,注器甲的活塞的移动情况是______,最后该活塞所处的示数约为______mL,由此说明二氧化碳能与氢氧化钠反应。
参考答案
1.答案:B
解析:A、用漏勺从锅中捞取饺子,是因为饺子和其它物质的颗粒大小不同,不需要通过化学变化就能表现出来,A错误;B、用盐酸去除铁架台上铁锈,是因为盐酸显酸性,盐酸能与铁锈的主要成分氧化铁反应生成氯化铁和水,需要通过化学变化才能表现出来,B正确;C、用活性炭制作简易净水器,是因为活性炭具有吸附性,不需要通过化学变化就能表现出来,C错误;D、氯化钠溶于蒸馏水得到生理盐水,没有发生化学变化,D错误。故选B。
2.答案:D
解析:取用氯化钠固体时,瓶塞应倒放,A不符合题意;用托盘天平称量物品时,应遵循“左物右码”的原则,B不符合题意;量筒的选择,应遵循“大而近”的原则,应用50 mL的量筒量取32.8 mL的水,C不符合题意;溶解时,应用玻璃棒不断搅拌,加速溶解,D符合题意。
3.答案:B
解析:A、霉变食物高温蒸煮后能杀死活菌,但不能去除有毒物质,所以霉变食物高温蒸煮后也不能食用,选项错误;B、发现CO中毒者,迅速将其转移到室外通风处,然后在根据具体情况进行进一步处理,选项正确;C、电梯的供电系统在火灾中会随时断电或电梯因热的作用变形而使人被困在电梯内,选项错误;D、重金属盐能破坏人体的蛋白质,误食重金属盐中毒后,可服用大量富含蛋白质的食物自救,选项错误。故选B。
4.答案:A
解析:由微观反应示意图可知,该反应是由二氧化碳和氢气在纳米纤维催化剂的作用下反应生成和,该反应中有1个“”,没有参加反应,实际参加反应的示意图如图:。
A、该反应是由二氧化碳和氢气在纳米纤维催化剂的作用下反应生成和,有利于减缓温室效应,正确;B、在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂。催化剂在化学反应前后质量和化学性质保持不变,物理性质可能改变,错误;C、根据微观反应示意图可知,该化学反应过程中,分子的种类都发生了改变,原子的种类没有改变,错误;D、由实际参加反应微观反应示意图可知,参加反应的和分子个数比为3:1,错误。故选A。
5.答案:D
解析:A、向盛有80℃热水的两只烧杯中各放入一小块白磷,然后用导管对准其中一块白磷通入氧气,观察到通入氧气的白磷燃烧,未通入氧气的白磷不燃烧,变量是氧气,说明可燃物燃烧需要氧气,实验方案能达到实验目的;B、除去NaCl溶液中少量的氯化镁溶液,加入适量的氢氧化钠溶液,氯化镁与氢氧化钠溶液反应生成氯化钠和氢氧化镁,过滤除去氢氧化镁,得到氯化钠溶液,实验方案能到达实验目的;C、鉴别棉织品和羊毛制品,灼烧闻气味,有烧焦羽毛气味的是羊毛,没有烧焦羽毛气味的是棉织品,实验方案能达到实验目的;D、气体通入紫色石蕊试液,二氧化碳和水反应生成碳酸,碳酸使紫色石蕊试液变红,HCl气体溶于水形成盐酸,也能使紫色石蕊试液变红,实验方案不能达到实验目的;故选:D。
6.答案:B
解析:A、稀盐酸显酸性,pH小于7,无论如何稀释都不会等于或大于7,故A错误;B、氢氧化钡溶液中有水,因此未滴加稀硫酸就有水的质量,滴加稀硫酸后,稀硫酸和氢氧化钡反应生成硫酸钡和水,水的质量逐渐增加,直到将氢氧化钡反应完,继续滴加稀硫酸,水的质量增大,故B正确;C、氢气和氧气在密闭容器中燃烧,生成水,化学方程式为,微观上,点燃条件下,每2个氢分子和1个氧分子反应生成2个水分子,则分子的个数减少,至完全反应不再发生改变,故C错误;
D、硝酸铵溶于水,溶液温度降低,故D错误;
故选B。
7.答案:C
解析:A、根据溶解度曲线可知,0~60℃时,的溶解度随温度升高而增大,60℃以上,的溶解度随温度升高而减小,故选项说法错误;B、升温到40℃时,溶解度约是70g,烧杯中的溶液为不饱和溶液,故选项说法错误;C、从40℃升温到60℃时,没有晶体析出,溶质、溶剂质量都不变,所以烧杯内溶液中溶质的质量分数不变,故选项说法正确;
D、100°C时,烧杯内溶液中溶质的质量分数为:,故选项说法错误。故选:C。
8.答案:C
解析:A、向盛有100g和混合溶液的烧杯中加入过量溶液,分别发生反应、,所以加入溶液前,溶液中含有、、三种溶质,错误;
B、由图可知,-是与反应生成的沉淀质量,
,,解得,-=9.8,错误;
C、由图可知,前80g溶液与反应:,由B可知,生成9.8g沉淀,与溶液反应:,则原混合溶液中与的质量比为16g∶19.6g=40∶49,正确;
D、实验中加入过量溶液,与不反应,则a点对应的溶液中含有,所以取a点对应溶液,滴加稀,与反应生成沉淀和盐酸,立即出现白色浑浊,错误。
故选C。
9.答案:(1)糖类
(2)金属
(3)
解析:(1)“拜拜甜甜圈”是甜食,富含淀粉、砂糖,淀粉、砂糖属于糖类,故填:糖类。
(2)纯金属和合金都属于金属材料,镍铬奥氏体不锈钢是一种合金,因此属于金属材料。
(3)反应物为氨气和氧气,产物为氮气和水,反应条件为点燃,因此化学方程式为。
10.答案:(1)+4
(2)
(3)氯化钠(或者NaCl)
解析:(1)设二氧化氯中Cl元素的化合价为x,在二氧化氯中氧元素的化合价为-2价,根据化合物中各元素的正负化合价代数和为零,则有,。故填:+4。
(2)根据工艺流程图可知,溶液中加入了过量的NaOH和过量的试剂X,试剂X为,因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,用来除去溶液中的氯化钙,操作A为过滤。则溶液中的杂质为NaOH和,HCl和反应生成NaCl、和,属于复分解反应。HCl和NaOH反应生成NaCl和,属于中和反应,HCl和NaOH反应的化学方程式为。故填:。
(3)由题中信息可知,反应II是特殊条件下电解NaCl溶液制,而反应Ⅲ制取的化学方程式为:。结合流程图可知,该流程中可循环利用的物质是水和氯化钠。故填:氯化钠(或者NaCl)。
11.答案:(1)CO2
(2)
(3)置换
(4)
解析:A~J分别为初中化学常见的十种物质,已知A为铁锈的主要成分,可推出A为氧化铁,常温下B、D均为气体,A能与B在高温下反应生成C和D,可推出B为一氧化碳,D为二氧化碳,C为铁,H的溶液呈蓝色,H为铜盐溶液,C能与H反应生成G,可推出G为铜,G能与F在加热的条件下反应生成I,I为黑色固体,F为气体,可推出F为氧气,I为氧化铜,H的相对分子质量是I的两倍,可推出H为硫酸铜,E在通电的条件下转化为F,可推出E为水,W在加热的条件下反应生成D、E、J,J是无色气体,其中J是一种有刺激性气味的气体,其水溶液显碱性,可推出J为氨气,则W为碳酸氢铵,代入验证,符合题意。
(1)由分析可知,D为二氧化碳,化学式为:;
(2)W为碳酸氢铵,碳酸氢铵由铵根离子和碳酸氢根离子构成,铵根离子属于阳离子,离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故填:;
(3)反应②为铁和硫酸铜反应生成硫酸亚铁和铜,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
(4)反应⑤为铜和氧气在加热的条件下反应生成氧化铜,该反应的化学方程式为:。
12.答案:(1)分液漏斗
(2);浓硫酸
(3)将带火星的小木条防止b口处,观察到小木条复燃,则证明氧气已经集满
(4)先向左移,后向右移;2
解析:(1)由图可知,仪器X为分液漏斗;
(2)B装置为固液常温型发生装置,应选用过氧化氢溶液和二氧化锰混合物制氧,过氧化氢在二氧化锰作催化剂的条件下分解产生水和氧气,故方程式为:;
浓硫酸具有吸水性,且不与二氧化碳反应,所以可用于干燥二氧化碳,故若用F装置干燥实验室制取的二氧化碳,F中应盛有的药品名称为浓硫酸;
(3)氧气的密度比空气略大,若用F装置收集氧气,应长进短出,氧气具有助燃性,验满时将带火星的小木条防止b口处,观察到小木条复燃,则证明氧气已经集满;
(4)将注射器乙中气体全部注入到盛有NaOH溶液的注射器甲中,压强先增大,后二氧化碳和氢氧化钠反应生成碳酸钠和水,压强减小,故在①的整个实验过程中,注射器甲的活塞的移动情况是活塞先向左移后向右移,最后二氧化碳被全部吸收,该活塞所处的示数约为2mL,说明二氧化碳能与氢氧化钠反应。
选项
实验目的
实验方案
A
探究可燃物燃烧需要氧气
向盛有80℃热水的两只烧杯中各放入一小块白磷,然后用导管对准其中一块白磷通入氧气,观察现象
B
除去NaCl溶液中少量的氯化镁溶液
加入适量的氢氧化钠溶液,过滤
C
鉴别棉织品和羊毛制品
灼烧闻气味
D
检验气体中是否混有HCl气体
通入紫色石蕊试液,观察溶液是否变红
2024年四川省绵竹市中考第二次诊断考试化学试卷(原卷版+解析版): 这是一份2024年四川省绵竹市中考第二次诊断考试化学试卷(原卷版+解析版),文件包含2024年四川省绵竹市中考第二次诊断考试化学试卷原卷版docx、2024年四川省绵竹市中考第二次诊断考试化学试卷解析版docx等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。
2024年四川省绵竹市九年级第一次诊断考试化学试卷(原卷版+解析版): 这是一份2024年四川省绵竹市九年级第一次诊断考试化学试卷(原卷版+解析版),文件包含2024年四川省绵竹市九年级第一次诊断考试化学试卷原卷版docx、2024年四川省绵竹市九年级第一次诊断考试化学试卷解析版docx等2份试卷配套教学资源,其中试卷共14页, 欢迎下载使用。
四川省绵竹市2023—2024学年九年级上学期期末质量监测化学试卷: 这是一份四川省绵竹市2023—2024学年九年级上学期期末质量监测化学试卷,共21页。试卷主要包含了本试卷共10页,全卷闭卷考试,共100分等内容,欢迎下载使用。












