



2024年陕西省渭南市临渭区第二次中考模拟考试化学试题(原卷版+解析版)
展开九年级化学试题
注意事项:
1.本试卷分为第一部分(选择题)和第二部分(非选择题)。全卷共6页,总分60分。考试I间60分钟。
2.领到试卷和答题卡后,请用0.5 毫米黑色墨水签字笔,分别在试卷和答题卡上填写姓名和考证号,同时用2B铅笔在答题卡上填涂对应的试卷类型信息点(A或B)。
3.请在答题卡上各题的指定区域内作答,否则作答无效。
4.考试结束,本试卷和答题卡一并交回。
可能用到的相对原子质量:H—1 C—12 O—16 Cl--35.5 Ca---40
第一部分(选择题 共 18 分)
一、选择题(共9小题,每小题2分,计18分。每小题只有一个选项符合题意)
1. 崇尚科学,厚植爱国主义情怀。下列哪位科学家是我国制碱工业的先驱
A. 张青莲 B. 袁隆平
C. 侯德榜 D. 屠呦呦
【答案】C
【解析】
【详解】A、张青莲测定了一些相对原子质量的新值,不符合同意;
B、袁隆平改良杂交水稻,提高水稻产量,不符合同意;
C、侯德榜改良了制碱工艺,被称为中国制碱工业的先驱的化工专家,符合题意;
D、屠呦呦发现了青蒿素,不符合同意;
答案:C。
2. 诗歌是中华文明皇冠上的璀璨明珠。下列诗句与化学变化有关的是
A. 千锤万凿出深山,烈火焚烧若等闲 《石灰吟》
B. 欲渡黄河冰塞川,将登太行雪满山 《行路难》
C. 飞流直下三千尺,疑是银河落九天 《望庐山瀑布》
D. 八月秋高风怒号,卷我屋上三重茅 《茅屋为秋风所破歌》
【答案】A
【解析】
【详解】A、千锤万凿出深山,烈火焚烧若等闲 ,煅烧石灰石,有二氧化碳等新物质生成,属于化学变化;
B、欲渡黄河冰塞川,将登太行雪满山,结冰、下雪,只是水的状态的改变,无新物质生成,属于物理变化;
C、飞流直下三千尺,疑是银河落九天,描写的是瀑布,无新物质生成,属于物理变化;
D、八月秋高风怒号,卷我屋上三重茅 ,狂风怒号,卷走茅草,无新物质生成,属于物理变化。
故选A。
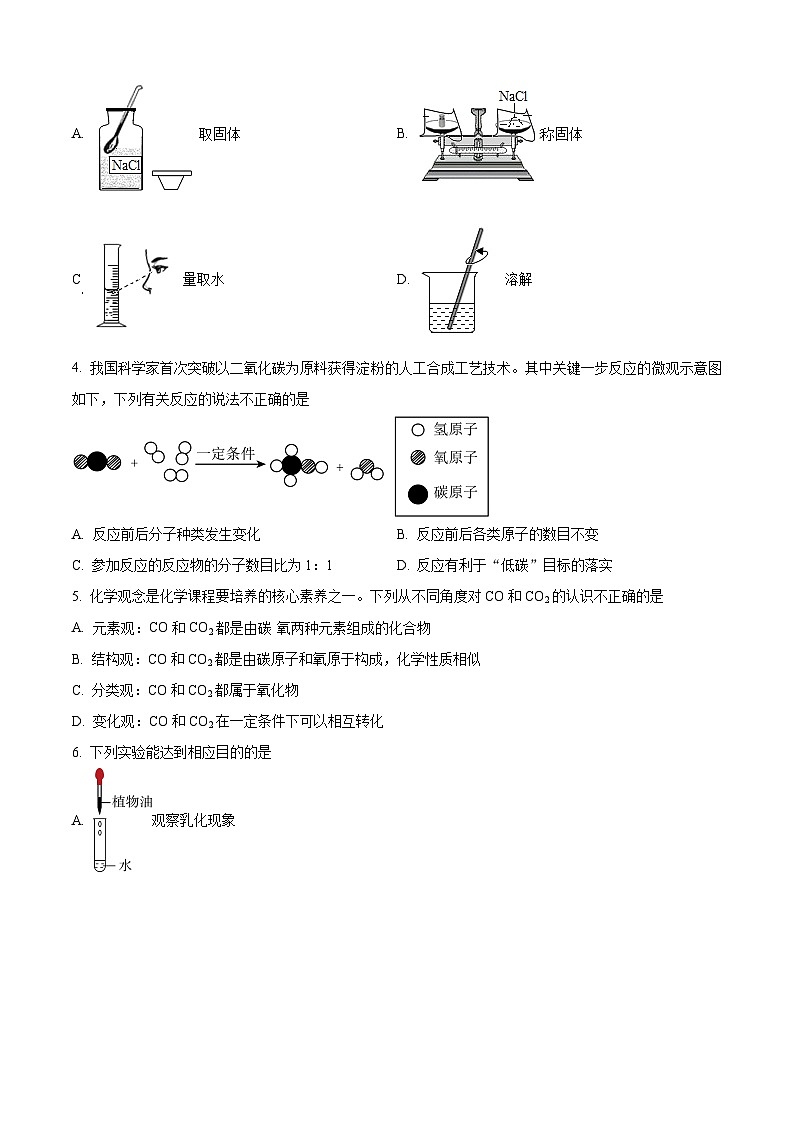
3. 欲配制质量分数为6%的NaCl溶液,下列有关操作正确的是( )
A. 取固体B. 称固体
C. 量取水D. 溶解
【答案】D
【解析】
【详解】A、取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,图中瓶塞没有倒放,图中所示操作错误;
B、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误;
C、量取液体时,视线与液体的凹液面最低处保持水平,图中俯视刻度,图中所示操作错误;
D、配制溶液时,溶解操作应在烧杯中进行,用玻璃棒不断搅拌,图中所示操作正确。故选D。
4. 我国科学家首次突破以二氧化碳为原料获得淀粉的人工合成工艺技术。其中关键一步反应的微观示意图如下,下列有关反应的说法不正确的是
A. 反应前后分子种类发生变化B. 反应前后各类原子的数目不变
C. 参加反应的反应物的分子数目比为1:1D. 反应有利于“低碳”目标的落实
【答案】C
【解析】
【分析】由图可知,该反应为二氧化碳和氢气在一定条件下反应生成甲醇和水,该反应的化学方程式为:。
详解】A、该反应有新物质生成,属于化学变化,反应前后分子种类发生了变化,不符合题意;
B、根据质量守恒定律,化学反应前后,原子的种类和数目不变,不符合题意;
C、由化学方程式可知,参加反应的反应物的分子数目比为:1:3,符合题意;
D、该反应消耗了二氧化碳,可减少二氧化碳的含量,有利于“低碳”目标的落实,不符合题意。
故选C。
5. 化学观念是化学课程要培养的核心素养之一。下列从不同角度对CO和CO2的认识不正确的是
A. 元素观:CO和CO2都是由碳 氧两种元素组成的化合物
B. 结构观:CO和CO2都是由碳原子和氧原于构成,化学性质相似
C. 分类观:CO和CO2都属于氧化物
D. 变化观:CO和CO2在一定条件下可以相互转化
【答案】B
【解析】
【详解】A、由化学式可知,一氧化碳和二氧化碳均是由C、O元素组成的纯净物,均属于化合物,选项正确;
B、同种分子化学性质相同,不同种分子化学性质不同,一氧化碳和二氧化碳的分子构成不同,所以两者化学性质不同,选项错误;
C、氧化物是由两种元素组成,其中一种元素是组成的化合物是于氧化物,一氧化碳和二氧化碳都是氧化物,选项正确;
D、一氧化碳燃烧生成二氧化碳,二氧化碳高温与碳反应生成一氧化碳,故CO和CO2在一定条件下可以相互转化 ,选项正确。
故选B。
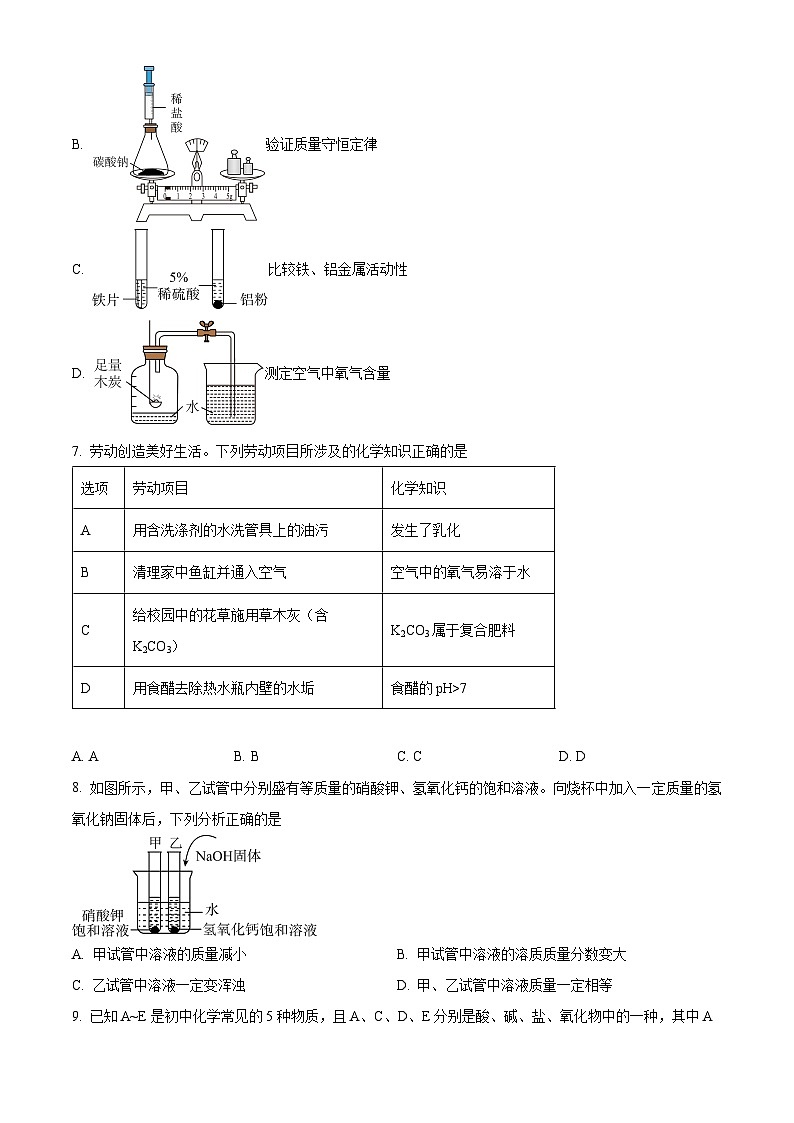
6. 下列实验能达到相应目的的是
A. 观察乳化现象
B. 验证质量守恒定律
C. 比较铁、铝金属活动性
D. 测定空气中氧气含量
【答案】B
【解析】
【详解】A、图中无乳化剂(如洗涤剂等),无法观察乳化现象。所以A实验不能达到相应目的。
B、碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,在密闭环境中二氧化碳不会逸出。只要少滴稀盐酸不使锥形瓶内压强过大即可。所以B实验能达到相应目的。
C、铁片与铝粉与5%稀硫酸反应速率不同,但不能比较铁、铝金属活动性,还应控制铁、铝的形状相同。所以C实验不能达到相应目的。
D、测定空气中氧气含量应用红磷作反应物,用足量木炭生成二氧化碳是气体占据了消耗的氧气体积,压强变化不明显。测定失败。所以D实验不能达到相应目的。
综上所述:选择B。
7. 劳动创造美好生活。下列劳动项目所涉及的化学知识正确的是
A. AB. BC. CD. D
【答案】A
【解析】
【详解】A. 用含洗涤剂的水洗管具上的油污,洗涤剂有乳化作用,将油污分散成小油滴除去,发生了乳化,正确。
B. 通入空气可以增加水中的含氧量,但空气中的氧气不易溶于水,错误。
C. 碳酸钾只含有氮磷钾中的钾元素,是钾肥。错误。
D. 用食醋去除热水瓶内壁的水垢是因为食醋pH<7,呈酸性,能和水垢中的碳酸钙、氢氧化镁等反应。错误。
故选:A。
8. 如图所示,甲、乙试管中分别盛有等质量的硝酸钾、氢氧化钙的饱和溶液。向烧杯中加入一定质量的氢氧化钠固体后,下列分析正确的是
A. 甲试管中溶液的质量减小B. 甲试管中溶液的溶质质量分数变大
C. 乙试管中溶液一定变浑浊D. 甲、乙试管中溶液质量一定相等
【答案】C
【解析】
【分析】硝酸钾的溶解度随温度升高而增大,氢氧化钙的溶解度随温度升高而减小。氢氧化钠溶于水,放热温度升高。
【详解】A、甲试管中硝酸钾溶解度变大,溶液会由饱和变成不饱和,溶液中溶质和溶剂都不变,溶液质量不变,选项错误;
B、甲试管中硝酸钾溶解度变大,溶液会由饱和变成不饱和,溶液中溶质和溶剂都不变,溶液溶质质量分数不变,选项错误;
C、乙试管中氢氧化钙溶解度变小,氢氧化钙饱和溶液中会析出氢氧化钙,溶液变浑浊,选项正确;
D、甲溶液由饱和变成不饱和,溶液质量不变,乙溶液有溶质析出,溶液质量变小,所以甲、乙试管中溶液质量不相等,选项错误;
故选C。
9. 已知A~E是初中化学常见的5种物质,且A、C、D、E分别是酸、碱、盐、氧化物中的一种,其中A是胃酸的主要成分,B是光合作用的原料,E常用于改良酸性土壤。它们相互转化的关系如图所示(“→”表示反应能一步实现,“—”表示相连物质间能发生反应,部分反应物、生成物和反应条件已省略)。下列说法错误的是
A. D是一种常见的溶剂B. A与E反应可生成D
C. D→E的反应过程放出热量D. C只能通过B和E反应生成
【答案】D
【解析】
【分析】A是胃酸的主要成分,则为HCl,属于酸;B是光合作用的原料,则为二氧化碳;E常用于改良酸性土壤,则为氢氧化钙,属于碱;A、C、D、E分别是酸、碱、盐、氧化物中的一种,则C、D分别为盐和氧化物中的一种,D能和二氧化碳反应,且D能转化为E,二氧化碳能和水反应,且氧化钙和水反应生成氢氧化钙,则D为水,属于氧化物;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,则C为碳酸钙,属于盐。
【详解】A、由分析可知,D为水,为最常见的溶剂,该选项说法正确;
B、A为HCl、E为氢氧化钙、D为水,盐酸和氢氧化钙反应生成氯化钙和水,该选项说法正确;
C、D为水、E为氢氧化钙,氧化钙和水反应生成氢氧化钙,该反应放出大量的热,该选项说法正确;
D、二氧化碳和氢氧化钙反应生成碳酸钙沉淀,但氢氧化钙和碳酸钠也能反应生成碳酸钙沉淀,该选项说法错误。
故选D。
第二部分(非选择题 共42分)
二、填空及简答题(共6小题,化学方程式2分,其余每空1分,计24分)
10. “禾下乘凉梦”是“杂交水稻之父”袁隆平院士的毕生夙愿。水稻从田间到饭桌,化学也做出了突出的贡献。回答下列问题:
(1)种植:为增强水稻的抗倒伏能力,我们常施用的KCl属于氮肥、磷肥、钾肥中的_____;
(2)储存:常用聚乙烯塑料制成真空包装袋来长期储存大米,该塑料属于_____(填“金属材料”或“合成材料”);
(3)运输:运输车辆使用的燃料主要来自石油,石油属于_____(填“可再生能源”或“不可再生能源”);
(4)食用:大米中的淀粉属于六大基本营养素中的_____。
【答案】(1)钾肥 (2)合成材料
(3)不可再生能源 (4)糖类
【解析】
【小问1详解】
KCl含有钾元素,属于钾肥;
【小问2详解】
塑料属于三大合成材料之一,所以聚乙烯塑料属于合成材料;
【小问3详解】
煤、石油、天然气属于不可再生能源,所以石油属于不可再生能源;
【小问4详解】
大米中的淀粉属于六大基本营养素中的糖类。
11. 我国提出在2030年前实现碳达峰,2060年前实现碳中和,彰显了大国责任与担当。如图是碳元素的二维价类图。
(1)A是化石燃料____________的主要成分。
(2)海洋生物吸收D转化为碳酸盐,其中F 是一种常用的补钙剂,化学式为____________
(3)碳及其化合物的转化过程均伴随着能量的变化,在一定条件下“D→C”的过程是___________(填“吸热”或“放热”)反应。
【答案】(1)天然气 (2)CaCO3
(3)吸热
【解析】
【小问1详解】
由图可知,A属于氢化物,且碳元素显-4价,故A是甲烷,甲烷是化石燃料天然气的主要成分;
【小问2详解】
F属于盐,碳元素显+4价,且F是一种常用的补钙剂,则F为碳酸钙,化学式为:CaCO3;
【小问3详解】
D属于氧化物,且碳元素显+4价,则D为二氧化碳,C属于氧化物,且碳元素显+2价,则C为一氧化碳,“D→C”的反应为二氧化碳和碳在高温下反应生成一氧化碳,是吸热反应。
12. “江南忆,最忆是杭州”,以“绿色、智能、节俭、文明”为理念的杭州亚运会赢得了高度赞誉。
(1)亚运会场馆地面加入石墨烯防滑剂,以提高地面的安全性和防滑性。石墨烯是石墨的单层结构,则石墨烯在物质分类中属于____________(填“单质”或“化合物”)。
(2)亚运会吉祥物琮琮、宸宸和莲莲主要由涤纶材料制成,涤纶属于___________(填“天然或“合成”)材料。
(3)亚运会期间启用加氢站助力“碳中和”,氢气做燃料能有效减少“碳排放”的原因是_______________(用化学方程式解释)。
【答案】(1)单质 (2)合成
(3)
【解析】
【小问1详解】
石墨烯是含有碳元素的纯净物,属于碳单质,故填:单质;
【小问2详解】
涤纶是合成纤维,合成纤维属于合成材料,故填:合成;
【小问3详解】
氢气和氧气点燃生成水,化学方程式是:。
13. 实验室从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料和金属铁、铜,实验过程如图:请回答:
(1)操作a的名称是_______。
(2)写出步骤②所涉及的化学反应方程_______。
(3)实验步骤②中除了加入稀硫酸外,还可选用的试剂是_______。
【答案】(1)过滤 (2)
(3)溶液
【解析】
【分析】根据题意,磁铁只能吸引铁,则A是铁,步骤2加入适量的稀硫酸会与镁反应生成硫酸镁和氢气,而铜不与酸反应,过滤后金属B是铜,溶液是硫酸镁最终蒸发结晶得到硫酸镁晶体,据此解题。
【小问1详解】
如图所示,该操作将固液分离,故该操作是过滤。
【小问2详解】
根据题意,该反应是镁和稀硫酸反应生成硫酸镁和氢气,化学方程式为:Mg+H2SO4=MgSO4+H2↑;
【小问3详解】
由于镁能把铜从它盐溶液中置换出来,为了得到硫酸镁,故可以加入硫酸铜溶液,这样镁和硫酸铜反应生成硫酸镁和铜,可以替代稀硫酸。
14. 向一支装有少量CuO的试管中依次加入下列物质,实验过程如图所示,回答下列问题。
(1)图A实验中加入过量稀H2SO4,观察到的现象是__________________。
(2)图B实验中有蓝色沉淀生成的反应的化学方程式为__________________。
(3)图D实验是向图C实验后所得溶液中插入新打磨的铝丝,反应一段时间后,取出铝丝,发现溶液为无色,则溶液中的溶质一定有_________________(填化学式)。
【答案】(1)黑色固体逐渐消失,溶液由无色变为蓝色
(2)
(3)Na2SO4、Al2(SO4)3
【解析】
【小问1详解】
氧化铜与硫酸反应生成硫酸铜和水,硫酸铜溶液为蓝色,则现象为黑色固体逐渐消失,溶液由无色变为蓝色。
【小问2详解】
硫酸铜能与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为。
【小问3详解】
由于氢氧化铜能与硫酸反应生成硫酸铜和水,铝丝能与硫酸反应生成硫酸铝和氢气,且铝能与硫酸铜反应生成硫酸铝和铜,一段时间后,溶液为蓝色,则说明硫酸铜和硫酸已完全反应,则此时溶液中的溶质有Na2SO4、Al2(SO4)3。
15. 根据如图甲所示硝酸钾的溶解度曲线回答下列问题。
(1)40℃时,将50g KNO3固体加入50g水中,充分溶解后恢复到原温度,所得溶液质量是__________ g;
(2)60℃时,向100g水中加入xg KNO3,固体形成溶液,再降温到20℃,析出固体的质量随时间的变化如图乙所示。
①x的数值是__________。
②该溶液降温过程中,在60 ℃、40℃、20℃时对应溶质质量分数分别为a、b、c,则三者的大小关系是____________.
(3)木块漂浮在40℃的KNO3的饱和溶液中(如图丙所示),烧杯底部有少量未溶解的固体剩余,将溶液降温至20℃,观察到烧杯底部的固体剩余物___________(填“增加”、“减少”或“不变”),烧杯中的小木块___________(填“上浮”或“下沉”)。
【答案】(1)81.95
(2) ①. 63.9 ②. a=b>c
(3) ①. 增加 ②. 下沉
【解析】
【小问1详解】
40℃时,硝酸钾的溶解度为63.9g,该温度下,将50g硝酸钾固体加入到50g水中,只能溶解31.95g,得到溶液的质量是:50g+31.95g=81.95g;
【小问2详解】
①由图可知,降温到20℃,析出固体的质量为32.3g,20℃时,硝酸钾的溶解度为31.6g,则x的数值是:31.6+32.3=63.9;
②60℃时,硝酸钾的溶解度为110g,即该温度下,100g水中最多溶解110g硝酸钾,则60℃时,形成的是不饱和溶液;40℃时,硝酸钾的溶解度为63.9g,即40℃时,该溶液恰好饱和,即40℃和60℃的溶液中溶质质量和溶剂质量相同,溶质质量分数相等,20℃时,有溶质析出,溶质质量减小,溶质质量分数减小,故该溶液降温过程中,在60℃、40℃、20℃时对应的溶质质量分数分别为a、b、c,则a=b>c;
【小问3详解】
将溶液降温至20℃,降温后,硝酸钾的溶解度减小,有溶质析出,故烧杯底部的固体剩余物增加;
降温后,有溶质析出,溶液溶质质量分数减小,溶液的密度变小,则小木块下沉。
三、实验及探究题(共2 小题,化学方程式2分,其余每空1分,计13分)
16. 下图是实验室制取气体常用的发生装置和收集装置,结合图示,回答下列问题:
(1)图中仪器甲的名称是______。
(2)若实验室用高锰酸钾制氧气,应在装置A的试管口______。
(3)若实验室用装置B、D组合制取氧气,其反应的化学方程式为______。若用装置E收集氧气,验满时,应将带火星的木条置于装置E的______处。(选填“a”或“b”)
(4)装置B、C均可用作实验室制取二氧化碳和氢气的发生装置,两者相比,装置C的优点是______。
【答案】(1)水槽 (2)放一小团棉花
(3) ①.
②. b
(4)随时控制反应的发生与停止
【解析】
【小问1详解】
仪器甲的名称为水槽;
【小问2详解】
若实验室用高锰酸钾制氧气,应在装置A的试管口放一小团棉花,防止加热时粉末状物质进入导管,堵塞导管;
【小问3详解】
若实验室用装置B、D组合制取氧气,B装置为固液常温型发生装置,即为过氧化氢在二氧化锰的催化下分解生成水和氧气,该反应的化学方程式为:;
由于氧气密度比空气大,若用装置E收集氧气,氧气应该从长管a处通入,验满时,应将带火星的木条置于装置E的b处,若木条复燃,则说明已收集满;
【小问4详解】
装置B、C均可用作实验室制取二氧化碳和氢气的发生装置,装置C中,当打开弹簧夹时,长颈漏斗内的液体在进入U形管,使U形管内液面上升到多孔隔板以上,与固体试剂接触,开始反应;当关闭弹簧夹时,产生的气体无法排出,在U形管上半部分聚积,使内部气压增大,将液体压回到长颈漏斗,使液面降到多孔塑隔板以下,使反应物相互分离,反应停止,故两者相比,装置C的优点是随时控制反应的发生与停止。
17. 食盐(主要成分为NaCl)是重要的调味品,炒菜时如果不放食盐,将食之无味。某化学兴趣小组的同学们对食盐展开了项目式探究。
项目一:鉴别工业用盐和食盐
【查阅资料】亚硝酸钠是一种工业用盐,有毒,有咸味,外形与食盐相似,水溶液呈碱性,与硝酸银溶液反应产生浅黄色沉淀。
【进行实验】同学们在某集贸市场买了一些散装盐,回到实验室后,取少量样品于烧杯中,向其中加入足量水,搅拌,使其充分溶解。
【实验小结】
(1)方案二中发生反应的化学方程式是___________________________。
【反思评价】
(2)①亚硝酸钠不能代替食盐用于烹调。
②上述方案中的方案一是错误的,该方案错误的原因是_______________________。
项目二:了解加碘食盐
【信息检索】碘是人体必需元素,因体内不能生成需从外界获取。人体缺碘会患 。
【交流讨论】
(3)加碘食盐是在食盐中加入一定量的碘酸钾 ,其中碘元素的化合价是___________。烹调时,需等食物熟后再加入加碘食盐,由此推测碘酸钾可能具有的一种性质是____________。
项目三:科学食用食盐
【交流讨论】
(4)摄入过量的食盐会使体重增加、身材走样,还可能会诱发高血压等疾病。在日常生活中,科学食用食盐的方法是________。
【答案】(1)
(2)不能尝药品的味道,以免中毒
(3) ①. +5 ②. 受热易分解
(4)适量摄取,尽量少吃含盐量高的食物(合理即可)
【解析】
【小问1详解】
方案二中发生反应为硝酸银与氯化钠反应生成氯化银沉淀和硝酸钠,方程式为:;
【小问2详解】
亚硝酸钠有毒,所以不能尝味道,以免中毒,且亚硝酸钠本身有咸味,故方案不合理;
【小问3详解】
碘酸钾中钾元素显+1价,氧元素显-2价,设碘元素化合价为x,根据化合物化合价正负代数和为0,(+1)+x+(-2×3)=0,x=+5;
烹调时,需等食物熟后再加入加碘食盐,由此推测碘酸钾的热稳定性差,受热易分解;
【小问4详解】
日常生活中,要合理适量摄取食用,尽量减少食用含盐量较高的食物。(合理即可)
四、计算与分析题(5分)
18. 在测定某碳酸钠样品纯度实验时,小明取一定质量的样品放入烧杯中,加入氯化钙溶液反应后过滤,实验过程和数据如图所示。
请计算:
(1)恰好完全反应时,生成沉淀的质量为_______g。
(2)所用氯化钙溶液的溶质质量分数_______。
【答案】(1)20 (2)设参加反应的氯化钙的质量为x,
x=22.2g
所用氯化钙溶液的溶质质量分数为;
答:所用氯化钙溶液的溶质质量分数为10%。
【解析】
小问1详解】
根据质量守恒定律可知,恰好完全反应时,生成沉淀的质量为:23g+222g-225g=20g;
【小问2详解】
见答案选项
劳动项目
化学知识
A
用含洗涤剂的水洗管具上的油污
发生了乳化
B
清理家中鱼缸并通入空气
空气中的氧气易溶于水
C
给校园中的花草施用草木灰(含K2CO3)
K2CO3属于复合肥料
D
用食醋去除热水瓶内壁的水垢
食醋的pH>7
方案
实验操作
实验现象
实验结论
方案一
品尝
有咸味
样品是食盐
方案二
取少量溶液于试管中,滴加硝酸银溶液
产生白色沉淀
方案三
取少量溶液于试管中,滴加酚酞溶液
溶液不变色
2024年陕西省渭南市合阳县初中学业水平第二次模拟考试化学试题(原卷版+解析版): 这是一份2024年陕西省渭南市合阳县初中学业水平第二次模拟考试化学试题(原卷版+解析版),文件包含2024年陕西省渭南市合阳县初中学业水平第二次模拟考试化学试题原卷版docx、2024年陕西省渭南市合阳县初中学业水平第二次模拟考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
2024年陕西省渭南市临渭区第二次中考模拟考试化学试题: 这是一份2024年陕西省渭南市临渭区第二次中考模拟考试化学试题,共6页。
2024年陕西省渭南市临渭区第二次中考模拟考试化学试题: 这是一份2024年陕西省渭南市临渭区第二次中考模拟考试化学试题,共6页。试卷主要包含了本试卷分为第一部分和第二部分,领到试卷和答题卡后,请用0,5 Ca---40,劳动创造美好生活等内容,欢迎下载使用。












