- 2025版高考化学一轮总复习教案第二章物质的量第六讲物质的量阿伏加德罗常数考点二阿伏加德罗常数及计算 教案 0 次下载
- 2025版高考化学一轮总复习教案第二章物质的量第七讲一定物质的量浓度溶液的配制考点一物质的量浓度 教案 0 次下载
- 2025版高考化学一轮总复习教案第三章金属及其化合物第八讲钠及其重要化合物碱金属考点一钠及其氧化物 教案 0 次下载
- 2025版高考化学一轮总复习教案第三章金属及其化合物第八讲钠及其重要化合物碱金属考点二碳酸钠和碳酸氢钠碱金属 教案 0 次下载
- 2025版高考化学一轮总复习教案第三章金属及其化合物第九讲铁及其重要化合物的性质和应用考点一铁的单质氧化物及氢氧化物 教案 0 次下载
2025版高考化学一轮总复习教案第二章物质的量第七讲一定物质的量浓度溶液的配制考点二一定物质的量浓度溶液的配制
展开知识梳理
1.主要仪器
(1)托盘天平:精确度为 0.1 g,称量前先 调零 ,称量时左盘放 物品 ,右盘放 砝码 。
(2)容量瓶
①构造及使用
②查漏操作
A.不能配制任意体积的溶液,只能配制容量瓶上规定容积的溶液;
B.不能将固体(或浓溶液)直接放在容量瓶中溶解(或稀释);
C.不能将过冷(或过热)的溶液转移到容量瓶中;
D.向容量瓶中注入液体时,一定要用玻璃棒引流,防止溶液洒落;玻璃棒末端应在容量瓶刻度线以下;
E.容量瓶不能用来长期贮存溶液。
(3)其他仪器:量筒、烧杯、 胶头滴管 、 玻璃棒 、药匙等。
2.配制一定物质的量浓度的溶液
以配制100 mL 1.0 ml·L-1 NaCl溶液为例
(1)主要仪器
天平、药匙、量筒、烧杯、 100 mL容量瓶 、玻璃棒、 胶头滴管 等。
(2)配制过程
3.配制一定物质的量浓度溶液的误差分析方法
误差分析中变量是m或V,一般情况要固定其一,分析另一物理量的变化对溶液浓度的影响:
4.定容操作中视线引起误差的分析
(1)定容时,仰视容量瓶的刻度线(如图1),导致溶液的体积偏大,则所配溶液的浓度偏低。
(2)定容时,俯视容量瓶的刻度线(如图2),导致溶液的体积偏小,则所配溶液的浓度偏高。
注意:①配制480 mL一定物质的量浓度溶液时,要选用500 mL的容量瓶。
②用容量瓶配制溶液时,必须先用蒸馏水洗净容量瓶,但可以不进行干燥。
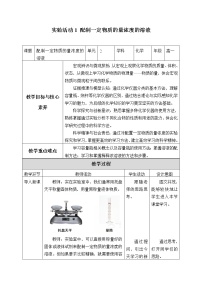
高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学设计: 这是一份高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学设计,共8页。
高中实验活动1 配制一定物质的量浓度的溶液教学设计: 这是一份高中实验活动1 配制一定物质的量浓度的溶液教学设计,共8页。
高中化学第三节 物质的量教学设计及反思: 这是一份高中化学第三节 物质的量教学设计及反思,共11页。