



福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷 (原卷版+解析版)
展开第I卷
一、选择题(每题仅一个正确答案,每题3分,共15题45分)
1. 如图是氟元素在元素周期表中的信息及原子结构示意图,下列表述错误的是
A. 氟属于非金属元素B. 氟原子核内有9个质子
C. 化学反应中氟原子易得电子D. 氟的相对原子质量为19.00g
2. 元素的化学性质主要取决于
A. 核电荷数B. 质量数和质子数
C. 原子的最外层电子数D. 相对原子质量
3. 门捷列夫的元素周期表奠定了现代化学和物理学的理论基础,下列关于元素周期表的叙述中正确的是
A. 周期表中有8个主族,8个副族
B. 目前使用的元素周期表中,最长的周期含有32种元素。
C. 短周期元素是指1-20号元素
D. 原子的最外层电子数都等于该元素所在的族序数
4. 无机非金属材料中,硅一直扮演着重要的角色。下列有关硅及其化合物的说法中正确的是
A. 最外层有四个电子,位于元素周期表的第三周期第VA族
B. 是酸性氧化物,可以与水反应:
C. 硅在自然界主要以硅酸盐和氧化物的形式存在
D. 光导纤维属于传统硅酸盐产品
5. 根据下列微粒结构示意图,有关说法不正确的是
① ② ③ ④ ⑤
A. 原子半径:①>②
B. 最高价氧化物对应的水化物酸性:④<⑤
C. 氢化物的稳定性:①<②
D. 微粒半径:②>③
6. 日本福岛核废水排海引起舆论风波,核废水中不只含有放射性氚,真正具有伤害性的,还有6种放射性元素,分别是碘、铯和铯、碳、钴和锶。下列叙述正确的是
A. 原子所含中子数与质子数之差为25B. 和互称为同素异形体
C. 铯的核外电子数为65D. 和的核外电子数之差为4
7. 下列说法正确是
A. 当L层上的电子数为奇数时,M层上不可能有电子
B. 同一主族中,相邻周期元素原子的核电荷数相差值一定为8或18或32
C. 同一周期中,随着核电荷数的增加,元素的原子半径逐渐增大
D. 同一周期中,IIA与IIIA族元素原子核电荷数都相差1
8. 下列曲线表示VIIA族元素某种性质随核电荷数的变化趋势,正确的是
A. B.
C. D.
9. 关于碱金属元素和卤族元素的下列说法错误的是
A. 由于钠和钾的原子结构极为相似,所以它们对应的碱都是强碱
B. 通过钠与钾分别与水反应的剧烈程度可知,碱金属原子核电荷数越多,金属性越强
C. 通过卤族单质与氢气反应所需要的反应条件,可以判断氯的非金属性比溴强
D. 卤族元素对应的氢化物的稳定性从强到弱的顺序为:HF<HCl<HBr<HI
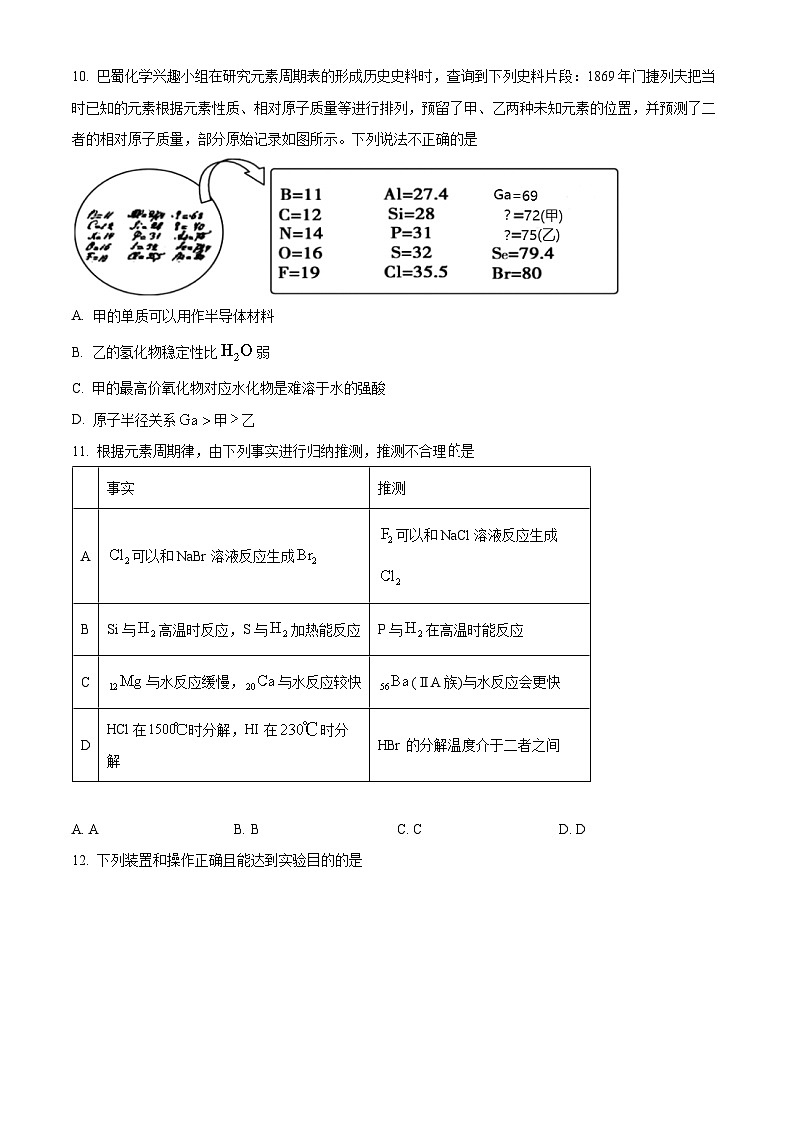
10. 巴蜀化学兴趣小组在研究元素周期表的形成历史史料时,查询到下列史料片段:1869年门捷列夫把当时已知的元素根据元素性质、相对原子质量等进行排列,预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如图所示。下列说法不正确的是
A. 甲的单质可以用作半导体材料
B. 乙的氢化物稳定性比弱
C. 甲的最高价氧化物对应水化物是难溶于水的强酸
D. 原子半径关系甲乙
11. 根据元素周期律,由下列事实进行归纳推测,推测不合理是
A. AB. BC. CD. D
12. 下列装置和操作正确且能达到实验目的的是
A. 利用图①装置进行纯碱中钠元素的焰色试验
B. 用图②装置分离水层和有机层,将从下层液体得到I2苯溶液
C. 用图③装置分离和固体
D. 用图④装置验证元素的非金属性:
13. 某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子是
A. K+、Na+、、B. Na+、、Cl-、
C. H+、Mg2+、、D. Ag+、K+、、Na+
14. 某同学取干海带经下列加工流程,从中提取I2.下列说法错误的是
已知:
A. 操作1中至少包括灼烧、溶解、过滤等主要过程
B. 试剂a可以是等氧化剂,试剂b可以是
C. 操作2和3均需用到分液漏斗,萃取振荡时应将分液漏斗下口向上倾斜,并不时放气
D. 可循环利用以有效提高干海带提碘的产率
15. 应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质。下列预测中正确的是
①第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
②砹(At)单质为有色固体,AgAt不溶于水也不溶于稀硝酸
③人们不但在过渡元素中寻找半导体材料,还在金属元素和非金属元素的交界处寻找优良的催化剂
④硫酸锶(SrSO4)是难溶于水的白色固体
⑤硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
A. ②④B. ②③④C. ①③⑤D. ②④⑤
第II卷
二、非选择题(共5题55分)
16. 结合下图所示元素周期表,回答下列问题:
(1)表中所列元素,属于短周期元素的有___________(填字母,下同);属于主族元素的有___________。
(2)f元素位于第___________周期第___________族。g元素位于第___________周期第___________族,i元素位于第___________周期第___________族。
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
A. 比较四种元素形成的最高价氧化物对应的水化物碱性强弱:j>c>d>e
B. 比较四种元素形成氢化物的难易程度以及氢化物的热稳定性:j
D. 将空气中久置的四种元素的块状单质分别放入水中,比较与水反应的剧烈程度:j>c>d>e
17. X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,X最外层电子数是内层电子数的2倍,Y的单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强。
(1)元素Y在元素周期表中的位置是___________。
(2)Z在氧气中完全燃烧的产物的化学式为___________。
(3)Y、W、Q的简单离子半径由大到小的顺序是___________(用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
①盛放盐酸和碳酸钙的仪器名称分别是:___________、___________;M为___________(填化学式),其作用是___________。
②能说明X元素的非金属性比硅元素强的实验现象是___________。
(5)元素Z与W相比,金属性较弱的是___________(填元素名称),请写出能证明这一结论的实验事实___________。(列举一条)
18. 如图是某化学课外小组利用氧化铝和二氧化硅的混合物制取高纯硅并探究氢氧化铝的两性的流程:
回答下列问题:
(1)高纯硅是优良的___________材料,二氧化硅可制作___________(一种高性能现代通信材料)。
(2)操作a和操作b的名称为___________,溶液A中含有铝的物质名称为___________。
(3)③的化学方程式为___________。
(4)④的离子方程式为___________。
(5)⑤的化学方程式为___________。
(6)氢氟酸可用于刻蚀玻璃化学方程式为___________。
19. 海洋是一个巨大资源宝库。在海洋中生长的海带,富含碘元素。某同学设计以下实验方案,从海带中提取。
(1)灼烧海带时,需要用到的瓷质实验仪器是___________。
(2)如将加双氧水改为加二氧化锰也可达到实验目的,写出向滤液中加入和稀硫酸发生反应的离子方程式:___________。
(3)试剂a可以是___________。
(4)I-和生成I2的离子方程式是___________。
(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是___________。
(6)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:___________。
20. 为验证卤素单质Cl2、Br2、I2氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
已知:稀溴水的颜色是黄色,浓溴水的颜色为红棕色。
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体对应的化学方程式是___________。
(2)B中溶液发生反应的离子方程式是___________。
(3)浸有NaOH溶液的棉花的作用是___________,反应的离子方程式为:___________。
(4)过程Ⅲ实验的目的是___________。
(5)为验证溴的氧化性强于碘,过程Ⅳ的操作是___________,现象是___________。
(6)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________(填化学式)。事实
推测
A
可以和NaBr溶液反应生成
可以和NaCl溶液反应生成
B
Si与高温时反应,S与加热能反应
P与在高温时能反应
C
与水反应缓慢,与水反应较快
(ⅡA族)与水反应会更快
D
HCl在时分解,HI在时分解
HBr的分解温度介于二者之间
福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷(学考)(原卷版+解析版): 这是一份福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷(学考)(原卷版+解析版),文件包含福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷学考原卷版docx、福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷学考解析版docx等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。
河南省郑州外国语学校2023-2024学年高一下学期3月月考化学试题(原卷版+解析版): 这是一份河南省郑州外国语学校2023-2024学年高一下学期3月月考化学试题(原卷版+解析版),文件包含河南省郑州外国语学校2023-2024学年高一下学期3月月考化学试题原卷版docx、河南省郑州外国语学校2023-2024学年高一下学期3月月考化学试题解析版docx等2份试卷配套教学资源,其中试卷共22页, 欢迎下载使用。
江苏省徐州华顿学校2023-2024学年 高一上学期 期中考试化学试卷(原卷版+解析版): 这是一份江苏省徐州华顿学校2023-2024学年 高一上学期 期中考试化学试卷(原卷版+解析版),文件包含精品解析江苏省徐州华顿学校2023-2024学年高一上学期期中考试化学试卷原卷版docx、精品解析江苏省徐州华顿学校2023-2024学年高一上学期期中考试化学试卷解析版docx等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。












