

江西省联考2024届高三新高考适应性测试化学试卷(无答案)
展开
这是一份江西省联考2024届高三新高考适应性测试化学试卷(无答案),共8页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.杭州亚运会首次实现亚运会“碳中和”,下列属于有机高分子材料的是( )
A.“大莲花”场馆的主体结构材料——钢 B.场馆顶部的覆盖膜——聚四氟乙烯
C.场地的防滑涂层——石墨烯 D.主火炬使用的可再生燃料——甲醇
2.关于反应,下列说法正确的是( )
A.分子中没有极性键 B.的模型和空间结构一致
C.的电子式为 D.分子之间的范德华力强于氢键
3.下图是一种改进的制备乙炔气体的装置。装置为自制仪器,下列仪器中与作用相同的是( )
A.漏斗 B.分液漏斗 C.滴液漏斗 D.布氏漏斗
4.火箭表面耐高温涂层的制备反应为。阿伏伽德罗常数的值为,下列说法正确的是( )
A.中共价键的数目为 B.中含有的中子数为
C.固体含有的数目为 D.消耗时,该反应中转移的电子数为
5.以下探究目的对应的实验方案最合适的是( )
A.A B.B C.C D.D
6.水系电池在碳循环方面具有广阔的应用前景。该电池的示意图如下,其中双极膜在工作时催化解离为和,并在直流电场的作用下分别向两级迁移。下列说法正确的是( )
A.放电时,电极为负极,发生还原反应
B.充电时,从电极通过双极膜到达催化电极发生反应
C.放电时,催化电极上的反应为
D.充电时,电极上的反应为
7.化合物是一种无机盐药物。已知为原子序数依次递增的短周期元素,同主族,同周期,基态原子轨道总电子数是轨道电子数的4倍,基态原子的未成对电子数相等。下列说法正确的是( )
A.离子半径: B.电负极:
C.简单氢氧化物沸点: D.难溶于水
8.荜茇酰胺是从中药荜茇中提取的一种有抗癌活性的天然生物碱,结构如下图所示.下列说法正确的是( )
A.分子中有3种官能团 B.双键均为顺式结构
C.分子式为 D.不能使酸性高锰酸钾溶液褪色
9.配合物的制备步骤如下:
I.称取,溶解于水中.
II.称取,溶解于水中,80℃加热,得到砖红色溶液.
III.将步骤II配置的溶液加入到溶液中,加热搅拌约
IV.当溶液析出少量固体时,冷却,过滤,洗涤,烘干,称重.
下列说法错误的是( )
A.步骤II中可使用水浴加热 B.步骤III中为控制反应速率,应逐滴加入
C.步骤II中发生了水解 D.步骤IV中为提高纯度,可用热水洗涤
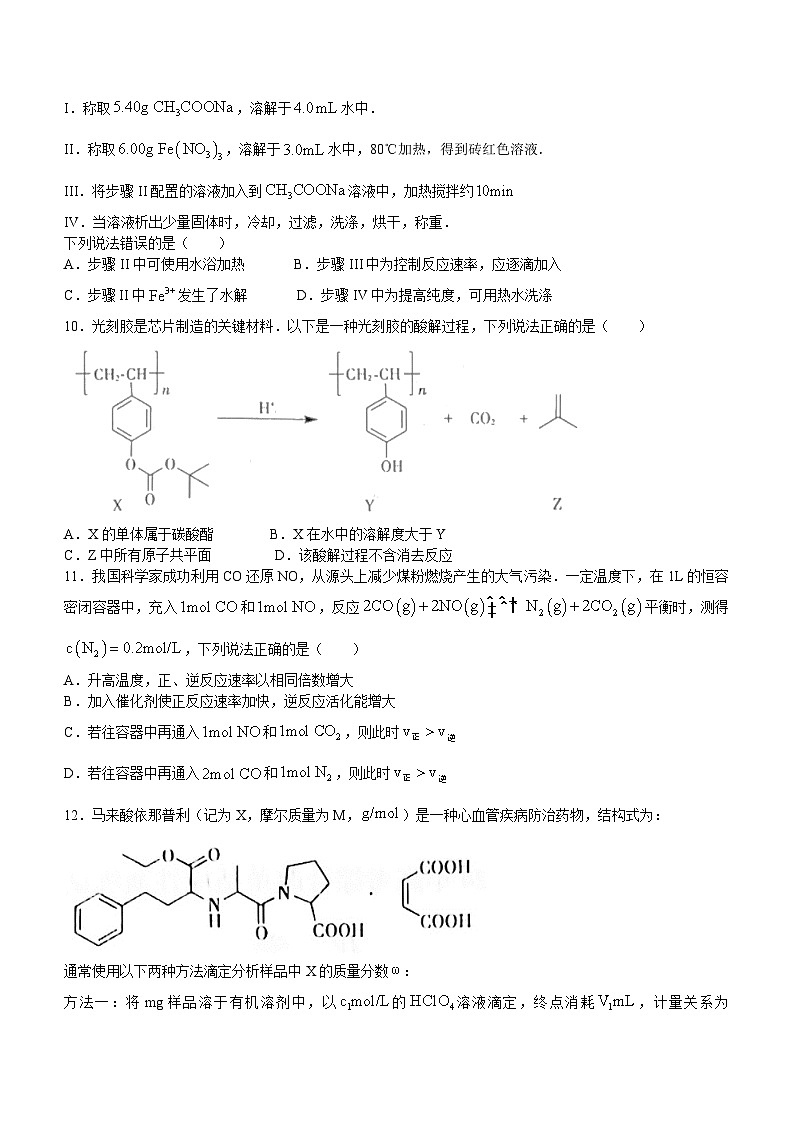
10.光刻胶是芯片制造的关键材料.以下是一种光刻胶的酸解过程,下列说法正确的是( )
A.X的单体属于碳酸酯 B.X在水中的溶解度大于Y
C.Z中所有原子共平面 D.该酸解过程不含消去反应
11.我国科学家成功利用CO还原NO,从源头上减少煤粉燃烧产生的大气污染.一定温度下,在1L的恒容密闭容器中,充入和,反应平衡时,测得,下列说法正确的是( )
A.升高温度,正、逆反应速率以相同倍数增大
B.加入催化剂使正反应速率加快,逆反应活化能增大
C.若往容器中再通入和,则此时
D.若往容器中再通入和,则此时
12.马来酸依那普利(记为X,摩尔质量为M,)是一种心血管疾病防治药物,结构式为:
通常使用以下两种方法滴定分析样品中X的质量分数:
方法一:将mg样品溶于有机溶剂中,以的溶液滴定,终点消耗,计量关系为;
方法二:将mg样品溶于水中,以的溶液滴定,终点消耗,计量关系为.
下列说法正确的是( )
A.方法一滴定终点时, B.方法一
C.方法二滴定终点时, D.方法二
13.朱砂(硫化汞)在众多先秦考古遗址中均有发现,其立方晶系型晶胞如下图所示,晶胞参数为anm,A原子的分数坐标为,阿伏加德罗常数的值为,下列说法正确的是( )
A.S的配位数是6 B.晶胞中B原子分数坐标为
C.该晶体的密度是 D.相邻两个Hg的最短距离为
14.一定温度下,水溶液中、、的分布分数与的关系如下图.例如.向浓度为的氨水中通入气体.已知该温度下,下列说法正确的是( )
A.通入时,
B.当时,
C.当时,
D.P点时溶液的值为8.3
二、非选择题:本题共4小题,共58分.
15.(14分)
锡在材料、医药、化工等方面有广泛的应用,锡精矿中主要有、S、、、等杂质元素.下图为锡的冶炼工艺流程.
已知:性质稳定,难溶于酸.
回答下列问题:
(1)锡的原子序数为50,其价层电子排布式为________,在元素周期表中位于________区.
(2)烟尘中的主要杂质元素是________(填元素符号).
(3)酸浸时,生成,该反应的离子方程式为________,为了提高铅的浸出率,最宜添加________(填标号).
A. B. C. D.
(4)还原时需加入过量的焦炭,写出该反应的化学方程式________.
(5)电解精炼时,以和少量作为电解液,电源的负极与________(填“粗锡”或“精锡”)相连;的作用是________、________.
(6)酸浸滤液中的可用沉淀,并通过与强碱反应获得,写出与熔融反应的化学方程式________.
16.(14分)
江西稀土资源丰富.硫酸铵作为一种重要的化工原料,可用于稀土的提取.初始投料比的混合物,其热分解过程如图所示:
已知该过程主要分为三个阶段,其中:
阶段Ⅱ反应:
阶段Ⅲ反应:
回答下列问题:
(1)中,的空间结构为________,中心原子的杂化类型为________.
(2)阶段Ⅰ不发生氧化还原反应,对应的化学方程式为________;图中阶段Ⅰ多次重复实验的实际失重均比理论值偏大,此误差属于________(填“偶然误差”或“系统误差”).
(3)阶段Ⅱ和Ⅲ都是吸热过程,且Ⅱ反应速率更快,下列示意图中能体现上述两反应能量变化的是________(填标号),判断的理由是________.
A. B. C. D.
(4)该热分解过程中,的作用为________.
(5)一定温度下,在真空刚性容器中,的分解过程会发生下列反应:
主反应
副反应
两个反应的平衡常数比值随反应温度升高而________(填“增大”,“减小”或“不变”);若平衡时总压为的体积分数为0.4,主反应的平衡常数________.
(6)在高温下可以自发分解,原因是________.
17.(15分)
乙酸乙酯在工业上有非常重要的作用。采用乙醇氧化脱氢法制备乙酸乙酯的反应原理及步骤如下:
I.将溶液加入至的三颈烧瓶中,冰盐浴条件下,加入乙醇。
II. 将溶于中,搅拌下逐滴加入三颈烧瓶中,反应温度控制在。
当混合物的粘度变大时,将温度升高到,继续反应。
III.将反应得到的绿色乳浊液用等量水稀释,分液,收集上层清液,纯化,干燥。
IV.分馏,收集馏分。
可答下列问题:
(1)步骤I中,使用冰盐浴()的原因是__________(填标号)。
A.增强乙醇还原性 B.有利于降温 C.减少乙醇挥发 D.减少硫酸挥发
(2)步骤II中,升温到的目的是__________
(3)步骤III中,上层清液中含有的主要杂质为__________、__________。
(4)步骤III中,纯化操作步骤为:先用__________、再用水洗涤。
(5)分馏装置如下图所示,玻璃仪器X的名称为__________;指出装置(不含夹持、加热等装置)中错误之处__________。
(6)相比于用浓硫酸催化乙酸和乙醇制备乙酸乙酯的方法,从反应条件角度评价该方法的优点是__________。
(7)为实现含铬废液的再生利用,可在含酸性废液中加入,写出该反应的离子方程式__________。
18.(15分)
盐酸芬戈莫德(H)是一种治疗多发性硬化症的新型免疫抑制剂,以下是其中一种合成路线(部分反应条件已简化)。
已知:i)
ii)
回答下列问题:
(1)化合物A中碳的2p轨道形成__________中心_________电子的大π键。
(2)由B生成C的反应类型为_________。
(3)试剂X的化学名称为_________。
(4)由D生成E的反应目的是_________。
(5)写出由E生成F的化学反应方程式_________。
(6)在C的同分异构体中,同时满足下列条件的可能结构共有_________种(不含立体异构)
a)含有苯环和硝基;
b)核磁共振氢谱显示有四组峰,峰面积之比为6:2:2:1。
上述同分异构体中,硝基和苯环直接相连的结构简式为_________。
(7)参照上:述反应路线,以和为原料,设计合成的路线_________(无机试剂任选)。实验方案
探究目的
A
向溶液中加入金属
比较和的还原能力
B
分别向稀硝酸和稀醋酸中加入铜粉
比较稀硝酸和稀醋酸的酸性强弱
C
将浓硫酸滴入乙醇中,加热至,生成的气体通入酸性重铬酸钾溶液
验证乙烯具有还原性
D
向溶液中同时通入和
比较和的氧化能力
相关试卷
这是一份广西联考2024届高三新高考适应性测试化学试卷(含答案),共11页。试卷主要包含了5 Cu-64, 黑火药的爆炸反应为, 反应常被用于除去水中残余氯等内容,欢迎下载使用。
这是一份甘肃省联考2024届高三新高考适应性测试化学试卷(含答案),共10页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份2024江西省“三新”协同教研共同体高三上学期12月联考化学试卷,共13页。









