
福建省厦门市第一中学2023-2024学年高三上学期第二次月考化学试卷(Word版附答案)
展开2.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cu-64 Se-79 Bi-209
一、选择题(本题共10小题,每小题4分,共40分,每小题只有一个选项符合题意)
1.新材料的发明与制造,推动着人类社会的进步和发展。下列有关材料的说法正确的是( )
A.电阻率低、热导率高的石墨烯可用于制作超级导电材料
B.用来生产电闸、灯口等产品的酚醛树脂属于聚酯类化合物
C.冬奥场馆建筑应用了新材料碲化镉发电玻璃,碲和镉均属于过渡元素
D.可用聚氯丙烯为原料制作医用外科口罩
2.下列化学用语或图示表达不正确的是( )
A.金刚石的晶体结构:
B.基态溴原子电子占据最高能级的电子云轮廓图:
C.乙炔的球棍模型:
D.的模型为
3.为阿伏加德罗常数的值。下列有关说法正确的是( )
A.标准状况下,氮气中含有个中子
B.晶体中含有的硅氧键数目为
C.浓硝酸热分解生成、共时,转移电子数为
D.的溶液中含数目小于
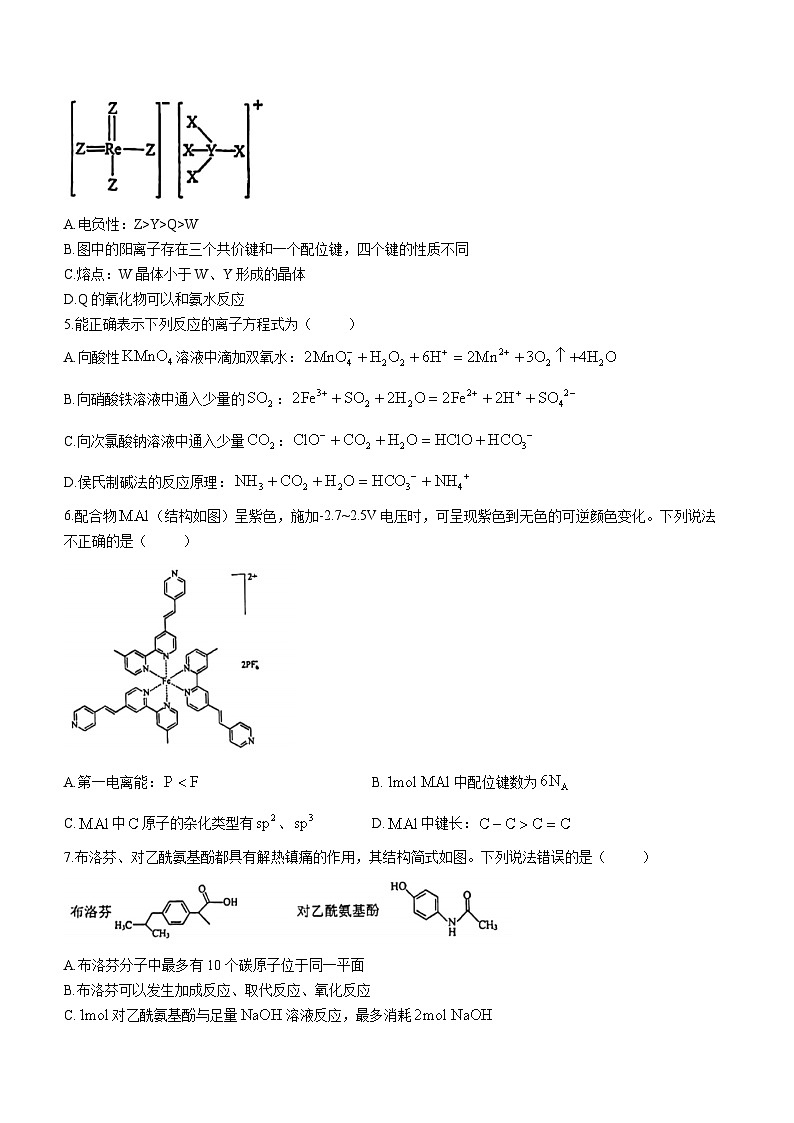
4.2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼()是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是( )
A.电负性:Z>Y>Q>W
B.图中的阳离子存在三个共价键和一个配位键,四个键的性质不同
C.熔点:W晶体小于W、Y形成的晶体
D.Q的氧化物可以和氨水反应
5.能正确表示下列反应的离子方程式为( )
A.向酸性溶液中滴加双氧水:
B.向硝酸铁溶液中通入少量的:
C.向次氯酸钠溶液中通入少量:
D.侯氏制碱法的反应原理:
6.配合物(结构如图)呈紫色,施加-2.7~2.5V电压时,可呈现紫色到无色的可逆颜色变化。下列说法不正确的是( )
A.第一电离能:B.中配位键数为
C.中原子的杂化类型有、D.中键长:
7.布洛芬、对乙酰氨基酚都具有解热镇痛的作用,其结构简式如图。下列说法错误的是( )
A.布洛芬分子中最多有10个碳原子位于同一平面
B.布洛芬可以发生加成反应、取代反应、氧化反应
C.对乙酰氨基酚与足量溶液反应,最多消耗
D.对乙酰氨基酚分子中含有的键数目为
8.实验推理法就是在实验的基础上加以科学推理,从而得出正确结论的方法。利用下图所示装置,a~d中加入试剂见下表,下列实验设计合理且对c中实验现象的预测及分析均正确的是( )
9.利用光伏电池与膜电解法制备溶液的装置如图所示。下列说法不正确的是( )
A.该光伏电池可将光能转化为电能
B.该离子交换膜为阳离子交换膜
C.电解池中阳极发生氧化反应,电极反应式为
D.电路中有电子通过时,阴极室溶液质量减少
10.络合平衡是广泛存在于自然界中的平衡之一,、、之间存在络合平衡:
①,平衡常数为;
②,平衡常数为,且大于。
时,在水溶液中,、之间关系如图所示,其中,代表、,下列叙述正确的是( )
A.直线代表与关系
B.c点条件下,能生成,不能生成
C.在含相同浓度的和溶液中滴加稀溶液,先生成
D.的平衡常数为
二、非选择题(共4题,60分)
11.铋酸钠()是一种可测定锰的强氧化剂。由辉铋矿(主要成分为,含、、等杂质)制备的工艺流程如下:
已知:①易水解,难溶于冷水,与热水反应,不溶于水。
②“氧化浸取”时,硫元素转化为硫单质。
③常温下,有关金属离子开始沉淀和沉淀完全的如表:
回答下列问题:
(1)基态的电子轨道表示式为____________。“滤渣1”的主要成分为_____________(填化学式)。
(2)“氧化浸取”过程中,需要控制温度不超过40℃的原因是____________,发生反应的化学方程式为____________。
(3)已知,中配体的空间结构为_____________,键角:______(填“>”、“<”或“=”),原因是_____________。
(4)“氧化”过程发生反应的离子方程式为____________。
(5)取制得的产品,加入足量稀硫酸和稀溶液,发生反应:
,完全反应后再用的标准溶液滴定生成的,当溶液紫红色恰好褪去时,消耗标准溶液,则产品的纯度为___________________%。
(6)我国科学家对新型二维半导体芯片材料——的研究取得了突破性进展。的晶胞结构中的位置如图所示(略去、),已知晶胞为竖直的长方体,高为,晶体密度为。设为阿伏加德罗常数的值,则晶胞底边边长_______________(填含、、的计算式,不必化简)。
12.的转化和利用是实现碳中和的有效途径。其中转换为被认为是最可能利用的路径,该路径涉及反应如下:
反应I:
反应Ⅱ:
请回答下列问题:
(1)反应I在______________(填“高温”“低温”或“任意温度”)下可以自发进行。
(2)在特定温度下,由稳定态单质生成化合物的焓变叫该物质在此温度下的标准生成焓()。下表为几种物质在的标准生成焓,则反应Ⅱ的___________
(3)在催化剂条件下,反应I的反应机理和相对能量变化如图(吸附在催化剂表面上的粒子用*标注,为过渡态):
完善该反应机理中相关的化学反应方程式:__________________;以为过渡态的反应,其正反应活化能为_________。
(4)在恒温恒压下,和按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
已知:a.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
b.
①在普通反应器(A)中,下列不能作为反应(反应I和反应 = 2 \* ROMAN II)达到平衡状态的判据是_____________(填标号)。
A.气体的密度不再变化B.气体的压强不再改变
C.D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是______________。
③在反应器(B)中,的平衡转化率明显高于反应器(A),可能的原因是___________。
④岩反应器(A)中初始时,反应Ⅱ的化学平衡常数(Ⅱ)=_____________(用最简的分数表示)。
13.实验小组制备,并探究其性质。
1.制备
(1)仪器a的名称是___________;气体b的化学式为________。用漏斗代替导管除了可以防倒吸,还具有的目的是___________。
Ⅱ.探究的性质
(2)查阅资料发现,溶液迅速变为棕色是因为生成了离子,来源于体系中生成的一种不稳定的酸_________(填化学式)分解。已知棕色溶液变浅是由于生成了,反应的离子方程式是_________。
(3)最终棕褐色溶液的成分是,测得装置中混合溶液体积为,设计如下实验测定其组成。
资料:充分反应后,全部转化为。
①与的结合能力:_________(填“>”或“<”)
②加入的作用是______________。
③由上述数据可知中_________(用含、的代数式表示)。
14.南京邮电大学有机电子与信息显示国家重点实验马延文教授课题组合成一种具有自修复功能的新型聚合物电解质,其部分合成流程如图所示,回答下列问题:
(1)A中官能团的名称是_____________;F→G的反应类型是_________;F的化学式为______________。
(2)溴乙烷难溶于水,而C(2—溴乙醇)能与水互溶,其原因是_____________。
(3)写出B→D的化学方程式:_____________;吡啶的作用是_____________。(已知:吡啶的结构简式为,具有芳香性和弱碱性)
(4)T是A的同分异构体,T同时具备下列条件的稳定结构有______________种(已知羟基连在双键的碳原子上不稳定,不考虑立体异构)。
①能发生银镜反应;
②与钠反应生成。
其中,在核磁共振氢谱上有3组峰且峰的面积比为1:1:4的结构简式为________________;含手性碳原子的结构简式为___________________________(写一种即可)。
厦门一中2024届高三年化学科1月模拟考试卷
参考答案
1-5ABCCC6-10BABBD
11.(17分)(1)(1分)和(2分)
(2)防止盐酸挥发和双氧水分解(2分)(2分)
(3)三角锥形(1分)<(1分)二者中心原子的为杂化,孤电子对数目:二对,一对,孤电子对越多,斥力越大,键角越小。(2分)
(4)(2分)
(5)65.8(2分)
(6)(2分)
12.(14分)(1)低温(1分)(2)+41(2分)
(3)(1分)1.3(2分)
(4)BC(2分)反应I为放热反应,反应Ⅱ为吸热反应,温度升高,反应I的化学平衡逆向移动,反应Ⅱ的化学平衡正向移动(2分)
反应器B中分子筛能催化反应I而不能催化反应Ⅱ且能分离出部分水蒸气,促使反应I化学平衡正向移动(2分)(2分)
13.(13分)(1)分液漏斗(1分);(2分);增大接触面积,加快反应速率使其充分反应(1分)
(2)(1分);(2分)
(3)①>(2分)
②与形成稳定的无色物质,既掩蔽的颜色,又避免与氢氧化钠反应造成实验干扰(2分)
③(2分)
14.(16分)(1)羧基、碳碳双键(2分)加聚反应(1分)(2分)
(2)2—溴乙醇能与水形成分子间氢键,溴乙烷不能与水形成分子间氢键(2分)
(3)(也可以把吡啶写在方程式里)(2分,把吡啶写在方程式里也得分)
吸收副产物,促进反应向正反应方向进行(1分)
(4)5(2分)(2分)或(2分)
a
b
c
d
c中实验现象的预测及分析
A
较浓硫酸
溶液
溶液
溶液中产生淡黄色沉淀,说明具有酸性氧化物性质和氧化性
B
稀
超细大理石
溶液
无试剂
溶液中产生白色沉淀,说明非金属性
C
浓氨水
碱石灰
溶液
和水
溶液中先产生蓝色沉淀,沉淀再溶解,说明能溶于浓氨水
D
溴乙烷
的乙醇溶液
酸性溶液
苯
溶液深紫色褪去,说明溴乙烷发生消去反应产生烯烃
金属离子
开始沉淀的
7.6
2.7
4.8
4.5
沉淀完全的
9.6
3.7
6.4
5.5
物质
0
-394
-111
-242
平衡转化率
甲醇的选择性
达到平衡时间()
普通反应器(A)
25.0%
80.0%
10.0
分子筛膜催化反应器(B)
a>25.0%
100.0%
8.0
装置
操作
现象
取溶液于试剂瓶中,加入几滴溶液酸化,再加入溶液,迅速塞上橡胶塞,缓缓通入足量
i.溶液迅速变为棕色
ii.棕色溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色
= 3 \* rman iii.最终形成棕褐色溶液
福建省厦门大学附属实验中学2023-2024学年高一上学期第二次月考化学试卷(Word版附答案): 这是一份福建省厦门大学附属实验中学2023-2024学年高一上学期第二次月考化学试卷(Word版附答案),共9页。试卷主要包含了金属钠制取氧化钠通常利用反应等内容,欢迎下载使用。
福建省三明第一中学2023-2024学年高三上学期12月月考化学试题(Word版附答案): 这是一份福建省三明第一中学2023-2024学年高三上学期12月月考化学试题(Word版附答案),共11页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
福建省厦门市翔安第一中学2023-2024学年高一上学期第二次月考试化学试卷(Word版附解析): 这是一份福建省厦门市翔安第一中学2023-2024学年高一上学期第二次月考试化学试卷(Word版附解析),共16页。试卷主要包含了5 Fe, 根据下列反应的方程式等内容,欢迎下载使用。












