



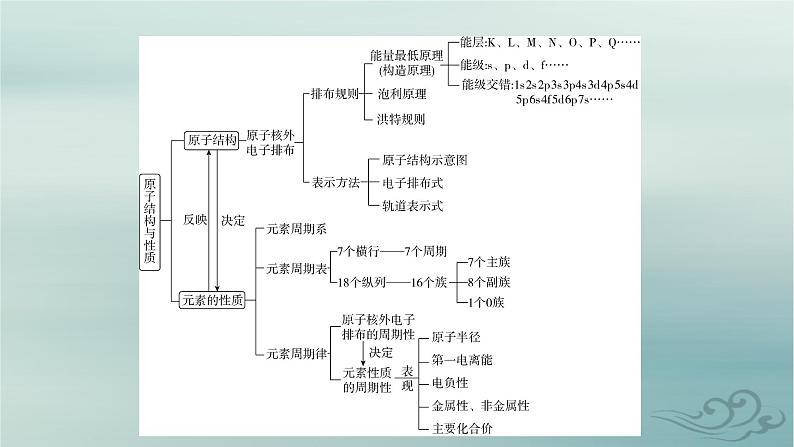



- 新教材适用2023_2024学年高中化学第1章原子结构与性质微专题1核外电子排布的规范书写与应用课件新人教版选择性必修2 课件 0 次下载
- 新教材适用2023_2024学年高中化学第1章原子结构与性质微专题2元素推断与元素周期律的综合应用课件新人教版选择性必修2 课件 0 次下载
- 新教材适用2023_2024学年高中化学第1章原子结构与性质第1节原子结构第1课时能层与能级基态与激发态原子光谱课件新人教版选择性必修2 课件 0 次下载
- 新教材适用2023_2024学年高中化学第1章原子结构与性质第1节原子结构第2课时构造原理与电子排布式电子云与原子轨道课件新人教版选择性必修2 课件 0 次下载
- 新教材适用2023_2024学年高中化学第1章原子结构与性质第1节原子结构第3课时泡利原理洪特规则能量最低原理课件新人教版选择性必修2 课件 0 次下载
化学选择性必修2第一节 原子结构示范课课件ppt
展开1.(2022·海南统考高考真题)钠和钾是两种常见金属,下列说法正确的是( )A.钠元素的第一电离能大于钾B.基态钾原子价层电子轨道表示式为 C.钾能置换出NaCl溶液中的钠D.钠元素与钾元素的原子序数相差18
2.(2022·江苏高考真题)工业上电解熔融Al2O3和冰晶石(Na3AlF6)的混合物可制得铝。下列说法正确的是( )A.半径大小:r(Al3+)
解析:X、Y、Z、R、Q是原子序数依次增大的五种短周期主族元素,由两种化合物的结构示意图可知,X、Y、Z、R、Q形成共价键的数目分别为4、3、2、1、5,则五种元素分别为C元素、N元素、O元素、F元素、P元素。由两种化合物的结构示意图可知,化合物中磷原子的最外层电子数为10,不满足最外层8电子稳定结构,故A错误;C元素、N元素、O元素、F元素、P元素中位于元素周期表右上角的氟元素的非金属性最强,元素的非金属性越强,简单氢化物的稳定性最强,故B正确;红棕色二氧化氮转化为无色四氧化二氮的反应为放热反应,降低温度,平衡向正反应方向移动,气体的颜色变浅,则将装有二氧化氮气体的透明密闭容器浸入冰水中,气体颜色变浅,故C正确;氧气和臭氧是氧元素形成的不同种单质,互为同素异形体,臭氧层破坏会造成环境污染,则臭氧在大气中的含量与环境污染密切相关,故D正确。故选A。
4.(2022·湖南高考真题)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是( )A.原子半径:X>Y>ZB.非金属性:Y>X>WC.Z的单质具有较强的还原性D.原子序数为82的元素与W位于同一主族
解析:由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C元素、Y为O元素、Z为F元素、W为Si元素。同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O>F,故A正确;同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;原子序数为82的元素为铅元素,与硅元素都位于元素周期表第ⅣA族,故D正确。故选C。
5.(1)(2022·全国乙高考真题)氟原子激发态的电子排布式有_____,其中能量较高的是_____。(填标号)a.1s22s22p43s1 b.1s22s22p43d2c.1s22s12p5 d.1s22s22p33p2(2)(2022·全国甲高考真题)基态F原子的价电子排布图(轨道表示式)为____________________。
(3)(2022·全国甲高考真题)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填标号),判断的根据是________________________________________ ________________________________________________________________________________;第三电离能的变化图是_______(填标号)。
同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高
(4)(2022·山东高考真题)基态Ni原子的价电子排布式为__________,在元素周期表中的位置为_________________。解析:(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5。1s22s22p43s1,基态氟原子2p能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;1s22s22p43d2,核外共10个电子,不是氟原子,b错误;1s22s12p5,核外共8个电子,不是氟原子,c错误;1s22s22p33p2,基态氟原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确。故选ad;而同一原子3p能级的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,故选d。
(2)F为第9号元素其电子排布为1s22s22p5,则其轨道表示式为 。(3)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此C、N、O、F四种元素的第一电离能从小到大的顺序为C
6.(1)(2022·海南统考高考真题)基态O原子的电子排布式_____________________,其中未成对电子有______个。(2)(2022·河北高考真题)基态S原子的价电子中,两种自旋状态的电子数之比为________________。(3)(2022·河北高考真题)Cu与Zn相比,第二电离能与第一电离能差值更大的是________,原因是____________________________________ ________________________________________________________________________________________________________________________________________________________。
1s22s22p4(或[He]2s22p4)
Cu的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,Zn的第二电离能失去的是4s1的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,其与4s1电子能量差值更大
(4)(2022·湖南高考真题)基态Se原子的核外电子排布式为[Ar] _____________。(5)(2022·湖南高考真题)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:富马酸亚铁中各元素的电负性由大到小的顺序为______________。
解析:(1)O为8号元素,其基态O原子核外有8个电子,因此基态O原子的电子排布式为1s22s22p4或[He]2s22p4,其2p轨道有2个未成对电子,即O原子有2个未成对电子。(2)基态S的价电子排布式为3s23p4,根据基态原子电子排布规则,两种自旋状态的电子数之比为12或21。(3)铜元素的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,锌元素的第二电离能失去的是4s1的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,其与4s1电子能量差值更大,所以铜与锌相比,第二电离能与第一电离能差值更大的是铜元素。
人教版 (2019)选择性必修3第二节 烯烃 炔烃评课ppt课件: 这是一份人教版 (2019)选择性必修3第二节 烯烃 炔烃评课ppt课件,共21页。PPT课件主要包含了第二节烯烃炔烃,新课情景呈现,课前素能奠基,碳碳双键,2乙烯的结构特点,sp2,同一平面内,CnH2n,液态或固态,nCO2+nH2O等内容,欢迎下载使用。
化学选择性必修3第一节 烷烃教课课件ppt: 这是一份化学选择性必修3第一节 烷烃教课课件ppt,共21页。PPT课件主要包含了第一节烷烃,新课情景呈现,课前素能奠基,sp3,CnH2n+2,液态或固态,易溶于,CH2,CH3,CH2CH3等内容,欢迎下载使用。
高中化学第一节 原子结构评课课件ppt: 这是一份高中化学第一节 原子结构评课课件ppt,共36页。PPT课件主要包含了跟踪训练,哑铃形,Na+,纺锤哑铃,PCl3+等内容,欢迎下载使用。













