






苏教版 (2019)必修 第一册第三单元 从微观结构看物质的多样性完美版ppt课件
展开1. 了解同素异形现象与同素异形体概念。2. 知道有机化合物存在同分异构现象,了解同分异构与同分异构体概念。3. 了解不同的晶体类型的性质。以不同类型的晶体为例,认识物质的多样性与微观结构的关系。
研究证明,金刚石和石墨在氧气中完全燃烧产物都只有二氧化碳,一定条件下,金刚石和石墨能相互转化,由此可以说明,它们都是由同一种元素形成的不同的单质,化学上把由同一种元素能形成几种不同单质的现象称为同素异形现象,这几种单质互称同素异形体。
活动一:探究同素异形现象
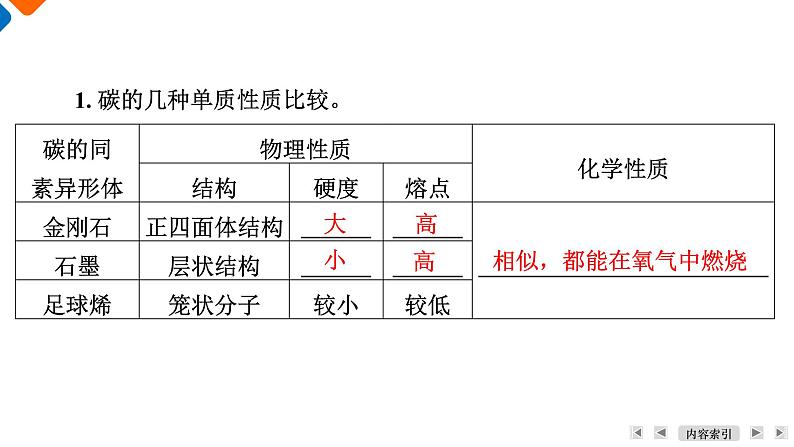
1. 碳的几种单质性质比较。
相似,都能在氧气中燃烧
活动二:探究同分异构现象
1. 找出正丁烷与异丁烷的结构组成上的异同和性质差异,正丁烷和异丁烷是否是同一种物质?【答案】 组成相同,分子式相同,结构不同,沸点不同,正丁烷与异丁烷不属于同一种物质。
3. 乙醇(沸点为78 ℃)和二甲醚(沸点为-23 ℃)互为同分异构体,它们的分子式都是C2H6O。观察它们的分子结构模型,分析两者间有什么差异。
【答案】 两者分子中的氧原子连接的原子不同,乙醇中含 C—OH,二甲醚中含有C—O—C,所以两者分子式相同,结构不同,属于同分异构体。
4. 列表比较同素异形体、同分异构体、同位素。
下图是生活中常见的晶体:
活动三:认识晶体与非晶体
1. 它们外观上有何特点?晶体外观为什么有这种特点?【答案】 具有规则几何外形,是因为内部的构成微粒呈有规则的重复排列。2. 不同类型的晶体构成微粒有哪几种?【答案】 有的晶体构成微粒是原子、有的是分子、有的是离子。
3. 固态物质都是晶体吗?【答案】 不是,自然界的固态物质有晶体和非晶体之分。4. 人们把晶体分为离子晶体、分子晶体、共价晶体、金属晶体的依据是什么?【答案】 晶体分为四种不同类型,依据是构成晶体的基本微粒和作用力不同。
1. 观察氯化钠晶体的结构。(1) 氯化钠是离子化合物,属于离子晶体,其构成微粒是什么? 离子晶体中微粒间作用力是什么?【答案】 氯化钠的构成微粒是钠离子和氯离子。离子晶体中离子间通过离子键结合。
活动四:认识不同的晶体
(2) 离子晶体中有无单个分子?讨论其熔、沸点高低、导电性。【答案】 无单个分子存在,NaCl不表示分子式。离子晶体一般熔、沸点较高,硬度较大,水溶液或者熔融状态下均导电,固态时不导电。
2. 观察干冰晶体和晶胞结构。(1) 干冰的构成微粒是什么?靠什么作用力形成晶体?干冰属于什么晶体?【答案】 干冰的构成微粒是CO2分子。通过分子间作用力使CO2分子聚集形成干冰,属于分子晶体。
(2) 分子晶体的构成微粒是什么?分子间结合成晶体的作用力是什么?一般有哪些相似的物理性质?【答案】 分子晶体的构成微粒是分子,通过分子间作用力形成晶体。分子晶体一般熔、沸点均较低,由于不存在离子,固、液态时均不导电。
3. 下图是水晶项链的晶体结构,观察其晶体模型。(1) 水晶中原子间通过共价键结合成空间网状结构,属于共价晶体,写出该晶体的化学式。该晶体中含分子吗?构成微粒是什么?原子靠什么作用力结合形成晶体?【答案】 化学式为SiO2,该晶体中不含分子,构成微粒是硅原子和氧原子,靠共价键构成共价晶体。
(2) 共价晶体中构成的微粒是什么?作用力是什么?有哪些共同的物理性质?【答案】 共价晶体中构成的微粒是原子,作用力是共价键,共价晶体一般熔、沸点高,硬度大。(3) 还有哪些晶体属共价晶体,举例说明。【答案】 金刚石、单晶硅、碳化硅等均为共价晶体,都是空间网状结构。
4. 学习教材关于金属晶体和液晶的描述,回答下列问题。(1) 金属固态时均为金属晶体,金属晶体有哪些共同的性质? 【答案】 金属晶体一般有金属光泽,能导电传热,具有延展性。(2) 液晶是一种介于晶体状态和液态之间的一种中间态物质,有什么特殊性质和应用?【答案】 兼有液体和晶体的某些特点,表现出一些独特的性质,在信息技术领域有重要的应用。
1. 下列各组物质中,属于同素异形体的是( )A. 16O和18O B. 红磷、白磷C. 二氧化硫、三氧化硫 D. 二氧化碳、干冰
【解析】 16O与18O互为同位素,A错误;红磷和白磷是由磷元素组成的不同的单质,B正确;SO2与SO3是不同的硫的氧化物,C错误;干冰是CO2的固态存在形式,D错误。
2. (2022·连云港期末)碳原子成键的多样性、同分异构现象等是有机化合物种类繁多的原因。乙醇和二甲醚的结构式如图所示。下列关于上述两种物质的说法正确的是( )A. 分子式不同 B. 互为同素异形体C. 碳氧键(C—O)数目相同 D. 性质有差异因分子结构不同
3. 下列不属于晶体的特点的是( )A. 具有规则的几何外形 B. 具有固定的沸点C. 具有固定的熔点 D. 一定是无色透明的固体【答案】 D
4. (2023·徐州邳州期末)下列说法正确的是( )A. 石墨烯、金刚石和C70互为同素异形体 B. 16O2与 18O2互为同位素
【解析】 石墨烯、金刚石、C70均为碳的单质,互为同素异形体,A正确; 16O2与 18O2为单质,不是原子,不互为同位素,B错误;为U元素的三种核素,互为同位素,C错误;三者相对分子质量不同,相同条件下密度不同,D错误。
5. (2022·淮安高一期末)下列有关碳及其化合物的说法中,正确的是( )A. 12C、13C、14C是碳元素的三种核素B. 干冰与二氧化碳气体互为同素异形体C. 石墨转化为金刚石改变了碳原子的排列方式,是物理变化D. 石墨和石墨烯都是由碳元素形成的单质,性质完全相同【答案】 A
6. SiCl4的分子结构与CCl4类似,对其做出如下推测,其中错误的是( )A. SiCl4晶体是分子晶体 B. 常温常压下SiCl4是气体C. SiCl4的分子内部原子以共价键结合 D. SiCl4熔点高于CCl4
【解析】 SiCl4与CCl4结构相似,CCl4属于分子晶体,则SiCl4晶体是分子晶体,A正确;SiCl4与CCl4结构相似,都可以形成分子晶体,前者相对分子质量较大,其分子间作用力较大,常温常压下CCl4是液体,则SiCl4是液体,B错误;CCl4分子是由极性键形成的非极性分子,则SiCl4分子是由极性键形成的非极性分子,C正确;分子晶体的相对分子质量越大,熔点越高,则SiCl4熔点高于CCl4,D正确。
7. 下列叙述正确的是( )A. 14C中含有14个中子 B. 1H、2H、3H是同一种核素C. H2O与D2O互称同位素 D. C60、金刚石、石墨均为碳的同素异形体【答案】 D
8. (2023·徐州期末)下列有关说法正确的是( )A. 二氧化硅和干冰都属于共价晶体B. C60和C70是具有相同质子数的不同核素C. 冰和氧化钠熔化时克服相同类型的化学键D. H2NCH2COOH和CH3CH2NO2互为同分异构体
【解析】 干冰是固态CO2,属于分子晶体,A错误;C60、C70为碳的单质,不是核素,B错误;冰熔化时克服的氢键和分子间作用力,氧化钠熔化时克服的是离子键,C错误。
9. 下列物质中,互为同分异构体的有________(填序号,下同);互为同素异形体的有________;属于同位素的有________。
【解析】 ②与④分子式相同,结构不同,互为同分异构体;③与⑤是由氧元素组成的不同单质,互为同素异形体;⑥与⑧是质子数相同、中子数不同的原子,互为同位素。
(1) ________互称为同位素。(2) ________为酸性氧化物。(3) ________的质量数相等,但不能互称为同位素。(4) __________互称为同素异形体。
化学苏教版 (2019)第三单元 防治二氧化硫对环境的污染精品课件ppt: 这是一份化学苏教版 (2019)第三单元 防治二氧化硫对环境的污染精品课件ppt,共29页。PPT课件主要包含了学习目标,活动方案,活动二酸雨及其防治,课堂反馈等内容,欢迎下载使用。
高中化学苏教版 (2019)必修 第一册第二单元 硫及其化合物的相互转化精品ppt课件: 这是一份高中化学苏教版 (2019)必修 第一册第二单元 硫及其化合物的相互转化精品ppt课件,共37页。PPT课件主要包含了学习目标,活动方案,课堂反馈等内容,欢迎下载使用。
苏教版 (2019)第三单元 人类对原子结构的认识评优课课件ppt: 这是一份苏教版 (2019)第三单元 人类对原子结构的认识评优课课件ppt,共35页。PPT课件主要包含了学习目标,活动方案,课堂反馈等内容,欢迎下载使用。













