


高考化学高频考点小题突破训练6化学反应速率与平衡 含解析
展开化学反应速率与平衡
1、在密闭容器中进行反应:![]()
![]()
![]() ,有关下列图像说法不正确的是( )
,有关下列图像说法不正确的是( )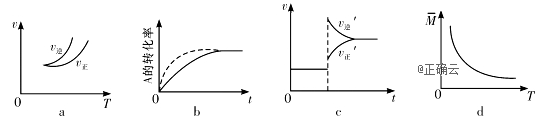
A.依据图a可判断正反应为放热反应
B.在图b中,虚线可表示使用了催化剂
C.若正反应的![]() ,图c可表示升高温度使平衡向逆反应方向移动
,图c可表示升高温度使平衡向逆反应方向移动
D.由图d中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的![]()
2、对于可逆反应![]() ,若其他条件都不变,只是在反应前是否加入催化剂,可得到如下两种
,若其他条件都不变,只是在反应前是否加入催化剂,可得到如下两种![]() 图像,下列判断正确的是( )
图像,下列判断正确的是( )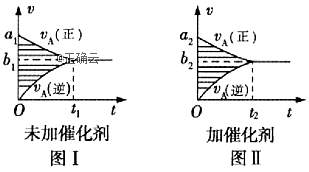
A.![]() ,
,![]()
B.![]() ,
,![]()
C.两图中阴影部分面积相等
D.图II中阴影部分面积更大
3、在一定条件下A2和B2可发生反应:A2(g)+3B2(g) ![]() 2AB3(g)。图1表示在一定温度下此反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时A2的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B2的起始物质的量对此反应平衡的影响。下列说法错误的是( )
2AB3(g)。图1表示在一定温度下此反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时A2的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B2的起始物质的量对此反应平衡的影响。下列说法错误的是( )
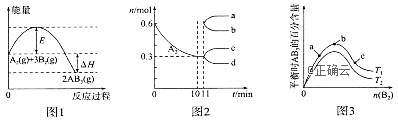
A. 该反应在低于某一温度时能自发进行
B. 10min内该反应的平均速率v(B2)=0.045mol/(L·min)
C. 11min时,其他条件不变,压缩容器容积至1L,n(A2)的变化趋势如图2中曲线d所示
D. 图3中T1<T2,b点对应状态下A2的转化率最高
4、对于可逆反应A(g)+2B(g) ![]() 2C(g) ΔH>0,下列图象中正确的是( )
2C(g) ΔH>0,下列图象中正确的是( )
A. 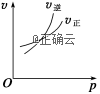
B. 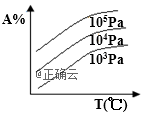
C. 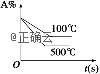
D. 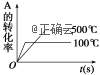
5、下列图示与对应的叙述相符的是( )
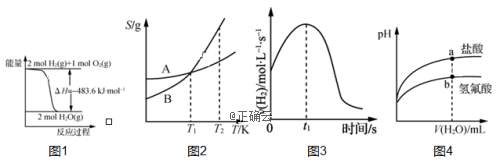
A.图1表示H2与O2发生反应过程中的能量变化,则H2O(g)===H2(g)+![]() O2(g)的ΔH=-241.8kJ·mol-1
O2(g)的ΔH=-241.8kJ·mol-1
B.图2表示A、B两物质的溶解度随温度变化情况,将T1K时A、B的饱和溶液分别升温至T2K时,溶质的质量分数B>A
C.图3表示镁条放入盐酸中生成氢气速率随时间的变化,0—t1反应速率加快的原因可能是该反应为放热反应
D.图4表示常温下稀释pH相同的氢氟酸与盐酸时溶液pH与加入水体积的关系,则氢氟酸为弱酸,且a点Kw的数值比b点的大
6、H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )
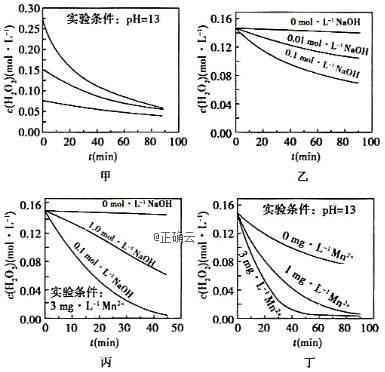
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
7、下列叙述与图像对应相符的是( )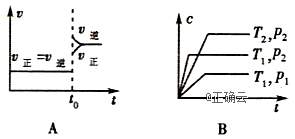

A.对于达到平衡状态的反应N2(g)+3H2(g)![]() 2NH3(g),在t0时刻充入了一定量的NH3,平衡逆向移动
2NH3(g),在t0时刻充入了一定量的NH3,平衡逆向移动
B.p2>p1,T1>T2
C.该图象表示的反应方程式为2A=B+3C
D.
对于反应2X(g)+3Y(g)![]() 2Z(g) ΔH<0,y可以表示Y的百分含量
2Z(g) ΔH<0,y可以表示Y的百分含量
8、在密闭容器中,反应2X(g)+Y2(g) ![]() 2XY(g) ΔH <0,达到甲平衡。在仅改变某一条件后,达到乙平衡,下列分析正确的是( )
2XY(g) ΔH <0,达到甲平衡。在仅改变某一条件后,达到乙平衡,下列分析正确的是( )
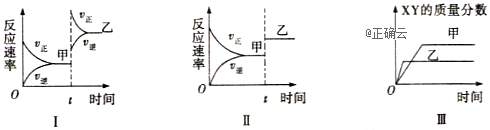
A.图Ⅰ中,甲、乙的平衡常数分别为K1、K2,则K1<K2
B.图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低
C.图Ⅱ中,t时刻增大了压强
D.图Ⅲ是反应分别在甲、乙条件下达到平衡,说明乙温度高于甲
9、一定条件下,某容积固定的密闭容器中发生反应:2NO2(g)![]() O2(g)+2NO(g) ΔH>0,达到平衡状态后,改变其中一个条件X,则Y随X的变化情况符合图中曲线的是( )
O2(g)+2NO(g) ΔH>0,达到平衡状态后,改变其中一个条件X,则Y随X的变化情况符合图中曲线的是( )
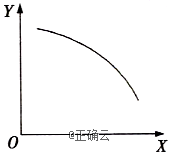
①当X表示温度时,Y表示NO2的物质的量
②当X表示压强时,Y表示NO2的转化率
③当X表示反应时间时,Y表示混合气体的密度
④当X表示NO2的物质的量时,Y表示O2的物质的量
A.①② B.①④ C.②③ D.③④
10、根据相应的图像,判断下列相关说法正确的是( )
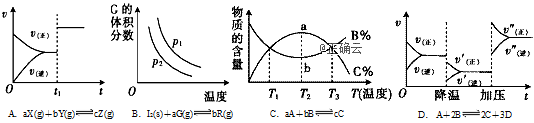
A.t1时改变某一条件,如图所示,则改变的条件一定是加入催化剂
B.反应达到平衡时,外界条件对平衡的影响如图所示,则该反应为放热反应
C.从加反应物开始,物质的百分含量与温度的关系如图,则该反应为吸热反应
D.反应速率和反应条件的变化如图所示,则该反应为放热反应,若A、B、C是气体,则D为固体或液体
11、对下列图像的描述正确的是( )
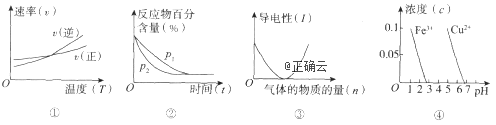
A.根据图①可判断反应A2(g)+3B2(g)![]() 2AB3(g)的△H>0
2AB3(g)的△H>0
B.图②可表示压强(p)对反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响
3C(g)+D(s)的影响
C.图③可表示向醋酸溶液通入氨气时,溶液导电性随氨气量的变化
D.根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3-5
12、CO2经催化加氢可合成乙烯:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)。0.1MPa时,按n(CO2):n(H2)=1:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图所示。下列叙述不正确的是( )
C2H4(g)+4H2O(g)。0.1MPa时,按n(CO2):n(H2)=1:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图所示。下列叙述不正确的是( )
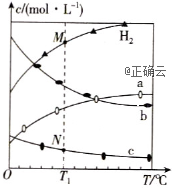
A.该反应的ΔH<0
B.曲线b代表H2O
C.N点和M点所处状态的c(H2)不一样
D.其他条件不变,T1℃、0.2MPa下反应达到平衡时c(H2)比M点的大
13、根据相应的图像,判断下列相关说法正确的是( )
A. 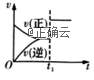
aX(g)+bY(g)![]() cZ(g)
cZ(g)
t1时改变某一条件,如图所示,则改变的条件一定是加入催化剂
B. 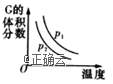
I2(s)+aG(g)![]() bR(g)
bR(g)
反应达到平衡时,外界条件对平衡的影响如图所示,则该反应为放热反应
C. 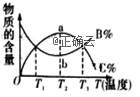
aA+bB![]() cC
cC
从加反应物开始,物质的百分含量与温度的关系如图,则该反应为吸热反应
D.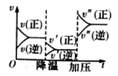
A+2B![]() 2C+3D
2C+3D
反应速率和反应条件的变化如图所示,则该反应为放热反应,若A、B、C是气体,则D为固体或液体
14、I2在KI溶液中存在平衡:I2(aq)+I-(aq)![]()
![]() (aq),某I2、KI混合溶液中,温度T与平衡时c(
(aq),某I2、KI混合溶液中,温度T与平衡时c(![]() )的关系如图。下列说法不正确的是( )
)的关系如图。下列说法不正确的是( )
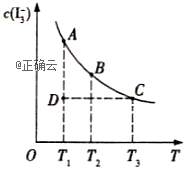
A.反应I2(aq)+I-(aq)![]()
![]() (aq)的ΔH>0
(aq)的ΔH>0
B.若温度为T1、T2时对应的平衡常数分别为K1、K2,则K1>K2
C.当反应进行到状态D时,一定有v正>v逆
D.状态A与状态B相比,状态A的c(I2)小
15、有某可逆反应![]()
![]()
![]() ;△H=Q kJ/mol。如图表示外界条件(温度、压强)的变化对上述反应的影响。下列判断正确的是( )
;△H=Q kJ/mol。如图表示外界条件(温度、压强)的变化对上述反应的影响。下列判断正确的是( )
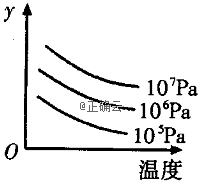
A.a+b<c时,y轴表示平衡混合气中C的质量分数
B.a+b>c时,y轴表示平衡混合气的平均摩尔质量
C.Q>0时,y轴表示达到平衡时B的转化率
D.Q>0时,y轴表示达到平衡时A的浓度
答案
1.D
解析:A、交点处![]() ,随着温度增大
,随着温度增大![]() ,平衡逆向移动,可判断正反应为放热反应,A正确;B、使用催化剂不改变反应限度,但缩短到达平衡的时间,B正确;C、若正反应的
,平衡逆向移动,可判断正反应为放热反应,A正确;B、使用催化剂不改变反应限度,但缩短到达平衡的时间,B正确;C、若正反应的![]() ,升高温度
,升高温度![]() 都增大,但
都增大,但![]() ,C正确;D、混合气体的平均相对分子质量
,C正确;D、混合气体的平均相对分子质量![]() ,根据质量守恒
,根据质量守恒![]() 是不变的,结合图像T升高,M减小,正反应的
是不变的,结合图像T升高,M减小,正反应的![]() ,D错误;选D。
,D错误;选D。
2.C
解析:加入催化剂,反应速率增大,但催化剂只影响反应速率,不影响平衡移动。加入催化剂时,正、逆反应速率都增大,缩短了达到平衡的时间,由此可得,![]() ,
,![]() ,
,![]() 。阴影部分面积为反应物浓度的变化量,由于催化剂不影响平衡移动,故两图中阴影部分面积相等。
。阴影部分面积为反应物浓度的变化量,由于催化剂不影响平衡移动,故两图中阴影部分面积相等。
3.D
A. 体系的自由能△G=△H-T△S,根据图示可知,该反应为放热反应,△H<0,由于该反应的正反应是气体体积减小的反应,所以△S<0。当温度较低时,△G=△H-T△S <0,反应能够自发进行;当温度较高时,T△S>△H,即△G>0,反应不能自发进行,A正确;
B.10min内该反应的平均速率v(A2)=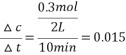 mol/(L·min),根据方程式可知v(B2)=3v(A2)=0.045mol/(L·min),B正确;
mol/(L·min),根据方程式可知v(B2)=3v(A2)=0.045mol/(L·min),B正确;
C.11min时,其他条件不变,压缩容器容积至1L,由于物质的浓度增大,化学平衡正向移动,不断消耗A2,所以n(A2)的物质的量会进一步减少,n(A2)变化趋势如图2中曲线d所示,C正确;
D.在温度不变时,增大某种反应物的浓度,化学平衡正向移动,可以使其它反应物的转化率提高,故当T1<T2,c点由于n(B2)最大,故其对应状态下A2的转化率最高,D错误;
故合理选项是D
4.C
5.C
6.D
解析:由图甲可知,起始时H2O2的浓度越小,曲线下降越平缓,说明反应速率越慢,A项错误;OH-的浓度越大,pH越大,即0.1mol·L-1 NaOH对应的pH最大,曲线下降最快,即H2O2分解最快,B项错误;由图丙可知,相同时间内,0.1mol·L-1 NaOH条件下H2O2分解最快,0mol·L-1 NaOH条件下H2O2分解最慢,而1.0mol·L-1 NaOH条件下H2O2的分解速率处于中间,C项错误;由图丁可知,Mn2+越多,H2O2的分解速率越快,说明Mn2+对H2O2分解速率影响较大,D项正确。
7.B
解析: 由A图可以看出平衡逆向移动,如果在t0时刻充入了一定量的NH3,则v正应与平衡点相连,A项错误;由“先拐先平”知,p2>p1,T1>T2,B项正确;C图表示的是可逆反应,C项错误;温度升高,平衡将逆向移动,Y的百分含量将增大,D项错误.
8.D
解析:若升高温度,则平衡向逆反应方向移动,平衡常数应减小,故图Ⅰ中t时刻改变的条件不可能是升高温度,可能是增大压强,由于温度不变,平衡常数不变,故A项错误;图Ⅱ表示加入催化剂,正、逆反应速率同等程度增大,平衡不移动,故反应物的转化率不变,B项错误;增大压强,平衡向正反应方向移动,图Ⅱ中反应速率增大,平衡不发生移动,故改变的条件肯定不是增大压强,故C项错误;乙先达到平衡,说明乙的反应速率快,故乙温度高于甲,D项正确.选D.
9.A
解析: 升高温度,平衡向正反应方向移动,NO2的物质的量减小,①正确;增大压强,平衡向逆反应方向移动,NO2的转化率减小,②正确;达到平衡后,随着时间的变化,混合气体的密度不变,③不正确;增大NO2的物质的量,使容积固定的密闭容器中NO2的浓度增大,平衡向正反应方向移动,则O2的物质的量增大,④不正确.
10.D
11.D
解析:A选项错误,根据图象,随着温度的升高,逆反应速率加快的程度大于正反应速率加快程度,所以可判断该反应应该是放热反应,△H〈0
B选项错误,首先是不清楚P1和P2的相对大小,无法判断。其次对于两个不同的压强环境,达到平衡后,反应物的百分含量在其他条件不变的情况下应该有所差别,图上并未表示出来。
C选项错误,醋酸中通入氨气会生成易溶于水的强电解质醋酸铵,离子浓度会增加,导电能力不会一开始就出现降低的情况。
D选项正确。
12.C
解析:A项,由图像可知H2的浓度随温度的升高逐渐增大,说明升高温度平衡逆向移动,正反应是放热反应,即ΔH<0,正确;B项,由图可知a表示CO2,b表示H2O,c表示C2H4,正确;C项,M、N点都代表温度为T1,时,按![]() ,投料时的平衡状态,所以M、N点状态的c(H2)相同,错误;D项,根据勒夏特列原理,压强增大,虽然平衡向右移动,但所有物质的浓度均增大,正确。
,投料时的平衡状态,所以M、N点状态的c(H2)相同,错误;D项,根据勒夏特列原理,压强增大,虽然平衡向右移动,但所有物质的浓度均增大,正确。
13.D
14.A
解析: A项,由图中曲线的变化趋势可知,当温度升高时, ![]() 的物质的量浓度减小,说明升温平衡逆向移动,该反应的正反应为放热反应,即ΔH<0,故A项不正确;B项,升高温度,平衡向逆反应方向移动,平衡常数减小,T1<T2,则K1>K2,故B项正确;C项,当反应进行到状态D时,反应未达到平衡状态,反应向生成
的物质的量浓度减小,说明升温平衡逆向移动,该反应的正反应为放热反应,即ΔH<0,故A项不正确;B项,升高温度,平衡向逆反应方向移动,平衡常数减小,T1<T2,则K1>K2,故B项正确;C项,当反应进行到状态D时,反应未达到平衡状态,反应向生成![]() 的方向进行,则v正>v逆,故C项正确;D项,状态B相当于在状态A的基础上升高温度,平衡向逆反应方向移动,则状态B的c(I2)大,故D项正确.
的方向进行,则v正>v逆,故C项正确;D项,状态B相当于在状态A的基础上升高温度,平衡向逆反应方向移动,则状态B的c(I2)大,故D项正确.
15.B
高考化学高频考点小题突破训练12离子反应 含解析: 这是一份高考化学高频考点小题突破训练12离子反应 含解析,共5页。试卷主要包含了下列化学过程及其表述正确的是等内容,欢迎下载使用。
高考化学高频考点小题突破训练10实验基础操作 含解析: 这是一份高考化学高频考点小题突破训练10实验基础操作 含解析,共8页。试卷主要包含了实验室中某些气体的制取,下列实验操作或装置正确的是等内容,欢迎下载使用。
高考化学高频考点小题突破训练7水溶液中的离子平衡 含解析: 这是一份高考化学高频考点小题突破训练7水溶液中的离子平衡 含解析,共11页。试卷主要包含了下列图示与对应的叙述相符的是,下列图像与对应叙述相符的是,常温下,浓度均为c0等内容,欢迎下载使用。












