


高考化学高频考点小题突破训练7水溶液中的离子平衡 含解析
展开水溶液中的离子平衡
1、电导率是以数字表示的溶液传导电流的能力,电导率越大,溶液导电能力越强。常温下用![]() 盐酸分别滴定10.00mL浓度均为
盐酸分别滴定10.00mL浓度均为![]() 的NaOH溶液和二甲胺
的NaOH溶液和二甲胺![]() 溶液{二甲胺在水中的电离与氨相似,已知在常温下
溶液{二甲胺在水中的电离与氨相似,已知在常温下![]() },利用传感器测得滴定过程中溶液的电导率如图所示。下列说法错误的是( )
},利用传感器测得滴定过程中溶液的电导率如图所示。下列说法错误的是( )
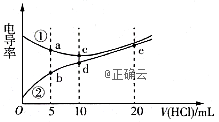
A.①代表滴定NaOH溶液的曲线,②代表滴定![]() 溶液的曲线
溶液的曲线
B.b、c、e三点的溶液中,水的电离程度最大的是e点
C.盐酸滴定二甲胺溶液的实验中选择甲基橙作指示剂比选酚酞误差更小
D.d点溶液中:![]()
2、常温下,向10mL 0.1mol·L-1的某一元弱酸HR溶液中逐渐滴入0.1mol·L-1的氨水,所得溶液pH及导电能力变化如图。下列分析不正确的是( )
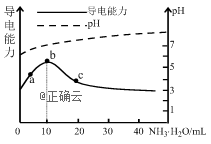
A.b、c两点水的电离程度:b>c
B.c点溶液:c(OH-)>c(H+)
C.b点溶液pH5.5,此时酸碱恰好中和
D.在a、b间任一点,溶液中一定有:c(R−)+c(OH−)=c(![]() )+c(H+)
)+c(H+)
3、下列图示与对应的叙述相符的是( )
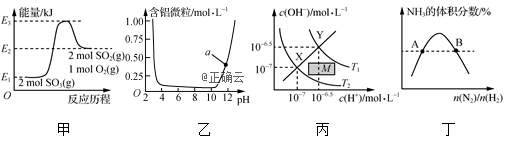
A. 由图甲可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1
B. 图乙表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+
C. 图丙表示温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足
c(H+)>c(OH-)
D. 图丁表示反应N2(g)+3H2(g) ![]() 2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
4、常温下,稀盐酸和氨水按不同体积比混合得到四种溶液,各取20mL溶液,用0.1mol•L﹣1 NaOH溶液滴定,溶液的pH随NaOH溶液的体积变化如图所示,下列说法正确的是( )
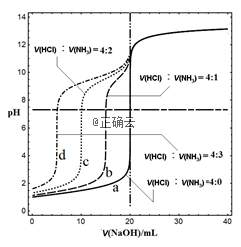
A. 滴至pH=7时,四种溶液中均存在c(Na+)=c(Cl﹣)
B. 原盐酸的浓度是0.1mol•L﹣1
C. V(NaOH)=10mL,溶液中Na+浓度a>b
D. 当V(NaOH)>20mL时,四种溶液的pH相同,溶液中的![]() 浓度近似相等
浓度近似相等
5、常温下,分别取未知浓度的HA和MOH溶液,加水稀释至原来体积的n倍。稀释过程中,两溶液的pH变化如图所示。下列叙述正确的是( )

A. HA为弱酸,MOH为强碱
B. 水的电离程度:X>Y=Z
C. 若升高温度,Y、Z点对应溶液的pH均减小
D. 将Y点与Z点对应溶液以体积比为1:10混合,所得溶液中:c(M+)>c(A-)>c(OH-)>c(H+)
6、下列图像与对应叙述相符的是( )
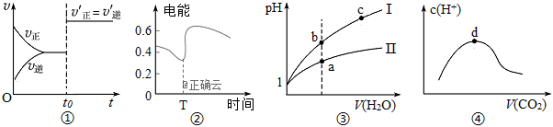
A.图①表示已达平衡的某反应在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂
B.图②表示Zn、Cu稀硫酸构成的原电池在工作过程中电流强度的变化,在T时加入了H2O2
C.图③表示同温度下、同体积pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸
D.图④表示向NaOH溶液中通入CO2,溶液中水电离出的c(H+)变化曲线,则最高点d处c(Na+)>c(OH-)>c(CO32-)>c(HCO3-) >c(H+)
7、常温下,浓度均为c0、体积均为V0的MOH和ROH两种碱液分别加水稀释至体积为V,溶液pH随lg![]() 的变化如图甲所示;当pH=b时,两曲线出现交叉点x,如图乙所示。下列叙述正确的是( )
的变化如图甲所示;当pH=b时,两曲线出现交叉点x,如图乙所示。下列叙述正确的是( )
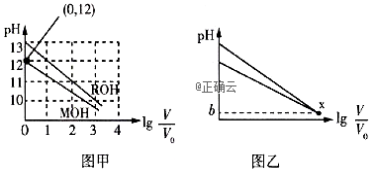
A.c0、V0均不能确定其数值大小
B.电离常数Kb(MOH)≈1.1×10-4
C.X点处两种溶液中水的电离程度相等
D.lg![]() 相同时,将两种溶液同时升高相同的温度,则
相同时,将两种溶液同时升高相同的温度,则![]() 增大
增大
8、常温下,向某浓度的草酸(H2C2O4)溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2C2O4、![]() 、
、![]() 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法不正确的是( )
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法不正确的是( )

A.草酸氢钾溶液中存在3个平衡
B.pH=2.7的溶液中, ![]()
C.将相同物质的量的KHC2O4和K2C2O4固体完全溶于水所得混合液的pH为4.2
D.滴定过程中水的电离程度:A点<B点
9、常温下,用0.10mol·L-1的NaOH溶液滴定20.00mL浓度为0.10mol·L-1的HX溶液所得滴定曲线如下图(忽略溶液体积变化)。下列说法正确的是( )

A. 常温下K(HX)≈1×10-12
B. a点所示的溶液中:c(Na+)>c(X-)>c(OH-)=c(H+)
C. c点所示的溶液中:c(Na+)+c(HX)+c(X-)=0.10mol·L-1
D. 相同条件下,X-的水解能力弱于HX的电离能力
10、常温下,将0.1mol·L-1 NaOH溶液分别滴加到0.1mol·L-1 HA溶液和HB溶液中,两混合溶液中离子浓度与pH的变化关系如图所示,下列说法不正确的是( )
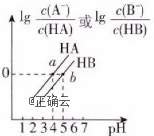
A.Ka(HB)<Ka(HA)
B.a点时,c(A-)=c(HA)>c(Na+)>c(H+)>c(OH-)
C.常温下,0.1mol·L-1 NaA溶液的pH大于0.1mol·L-1 NaB溶液的pH
D.向HB溶液中加入NaOH溶液,混合溶液中![]() (已知:
(已知: ![]() )
)
11、室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )
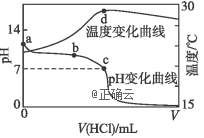
A.a点由水电离出的c(OH-)=1.0×10-14mol·L-1
B.b点:c(![]() )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
C.c点:c(Cl-)>c(![]() )
)
D.d点:达到滴定终点
12、如图表示的是难溶氢氧化物在不同pH下的溶解度(S),下列说法正确的是( )

A.pH=3时溶液中铁元素的主要存在形式是Fe3+
B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法除去
C.若要分离溶液中的Fe3+和Cu2+,可调节溶液的pH为4
D.若向含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀
13、常温时,![]() 和
和![]() (钨酸钙)的沉淀溶解平衡曲线如图所示。下列分析不正确的是( )
(钨酸钙)的沉淀溶解平衡曲线如图所示。下列分析不正确的是( )
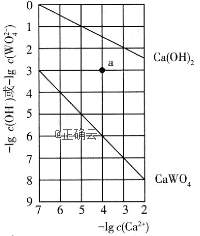
A.常温时,![]()
B.a点可以表示![]() 不饱和溶液或
不饱和溶液或![]() 悬浊液
悬浊液
C.常温时这两种物质的饱和溶液中![]() 相等
相等
D.加热饱和![]() 溶液有白色沉淀出现
溶液有白色沉淀出现
14、某温度下,难溶物FeR的水溶液中存在平衡FeR(s)![]() Fe2+(aq)+R2-(aq),其沉淀溶解平衡曲线如图所示。下列说法正确的是( )
Fe2+(aq)+R2-(aq),其沉淀溶解平衡曲线如图所示。下列说法正确的是( )
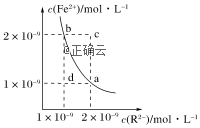
A.可以通过升温实现由a点变到c点
B.b点对应的Ksp等于a点对应的Ksp
C.d点可能有沉淀生成
D.该温度下,Ksp=4×10-18
15、已知锌及其化合物的性质与铝及其化合物相似。如图横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4 ]2-的物质的量浓度的对数。25℃时,下列说法中不正确的是( )
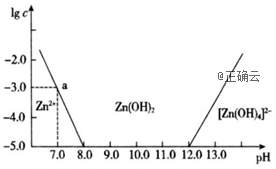
A.往ZnCl2溶液中加入过量氢氧化钠溶液,反应的离子方程式为Zn2++4OH-=[Zn(OH)4]2-
B.若要从某废液中完全沉淀Zn2+,通常可以调控该溶液的pH在8.0—12.0之间
C.pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108
D.该温度时,Zn(OH)2的溶度积常数(Ksp)为1×l0-10
答案
1.B
解析:A项,对比滴定前二者的电导率,可知①对应的是强碱,正确;B项,b点溶液中溶质为等物质的量的![]() 和
和![]() ,且
,且![]() ,
,![]() 的水解程度小于
的水解程度小于![]() 的电离程度,
的电离程度,![]() 电离生成的
电离生成的![]() 抑制水的电离,c点溶液中溶质为NaCl,对水的电离无影响,e点溶液中溶质为等物质的量的
抑制水的电离,c点溶液中溶质为NaCl,对水的电离无影响,e点溶液中溶质为等物质的量的![]() 和HCl,HCl为强酸,其完全电离出的
和HCl,HCl为强酸,其完全电离出的![]() 抑制水的电离,所以b、c、e三点的溶液中,水的电离程度最大的是c点,错误;C项,盐酸滴定二甲胺溶液时,滴定终点溶液显酸性,甲基橙的变色范围是3.1~4.4,酚酞的变色范围是8.2~10.0,因此使用甲基橙作指示剂误差更小,正确;D项,d点溶液中,溶质为
抑制水的电离,所以b、c、e三点的溶液中,水的电离程度最大的是c点,错误;C项,盐酸滴定二甲胺溶液时,滴定终点溶液显酸性,甲基橙的变色范围是3.1~4.4,酚酞的变色范围是8.2~10.0,因此使用甲基橙作指示剂误差更小,正确;D项,d点溶液中,溶质为![]() ,
,![]() ,d点溶液中存在质子守恒:
,d点溶液中存在质子守恒:![]() ,所以
,所以![]() ,正确。
,正确。
2.C
3.C
4.B
A.根据电荷守恒,滴至pH=7时,c(H+)=c(OH-),则a溶液中c(Na+)=c(Cl﹣);b、c、d三种溶液中c(Na+)+c(![]() )=c(Cl﹣),故A错误;
)=c(Cl﹣),故A错误;
B.a溶液中稀盐酸和氨水按4:0的比例混合,溶液中只含盐酸,当滴入0.1mol•L﹣1NaOH溶液20mL时溶液呈中性,则盐酸的浓度为0.1mol•L﹣1,故B正确;
C. V(NaOH)=10mL,由于向a和b中加入的氢氧化钠的量相同,则溶液中Na+浓度a=b,故C错误;
D.当V(NaOH)>20mL时,根据电荷守恒,溶液中均存在 c(Na+)+ c(![]() )+ c(H+)=c(OH-)+c(Cl﹣)。四种溶液中加入的氢氧化钠均相同,则溶液中的c(Na+)均相同,因为四种溶液的pH相同,则四种溶液中的c(H+)和c(OH-)均相同,又因为四种溶液中稀盐酸和氨水混合比例不同,则溶液中c(Cl-)大的,c(
)+ c(H+)=c(OH-)+c(Cl﹣)。四种溶液中加入的氢氧化钠均相同,则溶液中的c(Na+)均相同,因为四种溶液的pH相同,则四种溶液中的c(H+)和c(OH-)均相同,又因为四种溶液中稀盐酸和氨水混合比例不同,则溶液中c(Cl-)大的,c(![]() )小,则溶液中
)小,则溶液中![]() 浓度不相等,故D错误。答案选B
浓度不相等,故D错误。答案选B
5.D
根据图象可知,稀释过程中,HA溶液的体积变化10n倍,溶液的pH变化n个单位,说明HA为强酸;而MOH溶液的体积变化10n倍,溶液的pH变化小于n个单位,说明MOH为弱碱,
A.根据分析可知,HA为强酸,MOH为弱碱,故A错误;
B.X点水电离出的氢离子浓度是10-9mol/L,Y点水电离出的氢离子浓度是10-10mol/L,Z点水电离出的氢离子浓度是10-9mol/L,所以水的电离程度X=Z>Y,故B错误;
C.升高温度,水的离子积增大,Y点氢离子浓度基本不变,则其pH不变;Y点氢离子浓度增大,则Y点溶液pH减小,故C错误;
D.Y点pH=4,氢离子浓度为10-4mol/L,HA的浓度为10-4mol/L;Z点pH=9,氢氧根离子浓度为10-5mol/L,MOH为弱碱,则MOH的浓度大于10-5mol/L,将Y点与Z点对应溶液以体积比为1:10混合,由于MOH过量,混合液呈碱性,则c(OH-)>c(H+),结合电荷守恒可知:c(M+)>c(A-),溶液中离子浓度大小为:c(M+)>c(A-)>c(OH-)>c(H+),故D正确;
故选:D
6.B
7.C
解析:选项A,通过图甲中两种碱溶液的曲线变化可知,ROH为强碱,MOH为弱碱,常温下,浓度为c0=0.1mol·L-1,错误。选项B, ![]() ,错误。选项C,x点处两种溶液的pH相等,均为b,故水电离出的c(H+)均为10-bmol·L-1,正确。选项D,升温可促进弱电解质的电离,故lg
,错误。选项C,x点处两种溶液的pH相等,均为b,故水电离出的c(H+)均为10-bmol·L-1,正确。选项D,升温可促进弱电解质的电离,故lg![]() 相同时,升温,c(R+)不变,c(M+)增大,则
相同时,升温,c(R+)不变,c(M+)增大,则![]() 减小,错误.
减小,错误.
8.C
解析:由图象可知,草酸(H2C2O4)为二元弱酸,则草酸的电离方程式:H2C2O4![]()
![]() 、
、![]()
![]()
![]() 。在草酸氢钾溶液中存在平衡:
。在草酸氢钾溶液中存在平衡: ![]()
![]()
![]() 、
、![]()
![]()
![]() ,A项正确;由图象可知pH=2.7时,
,A项正确;由图象可知pH=2.7时, ![]() ,又溶液中存在电荷守恒
,又溶液中存在电荷守恒![]() ,B项正确;将相同物质的量的KHC2O4和K2C2O4固体完全溶于水,根据物料守恒,所得混合液中
,B项正确;将相同物质的量的KHC2O4和K2C2O4固体完全溶于水,根据物料守恒,所得混合液中![]() ,假设混合液的pH=4.2,由图可知,此时
,假设混合液的pH=4.2,由图可知,此时![]() ,由电荷守恒知
,由电荷守恒知![]() ,根据上述关系式得2c(H+)+3c(H2C2O4)=2c(OH-),则c(H+)<c(OH-),这与pH =4.2矛盾,故所得混合液的pH不可能为4.2,C项错误;向pH=1.2的溶液中继续加KOH溶液,pH增大至4.2时,溶液中溶质由草酸和KHC2O4变为KHC2O4和K2C2O4,则水的电离程度增大,D项正确。
,根据上述关系式得2c(H+)+3c(H2C2O4)=2c(OH-),则c(H+)<c(OH-),这与pH =4.2矛盾,故所得混合液的pH不可能为4.2,C项错误;向pH=1.2的溶液中继续加KOH溶液,pH增大至4.2时,溶液中溶质由草酸和KHC2O4变为KHC2O4和K2C2O4,则水的电离程度增大,D项正确。
9.C
A.由图象知0.10mol·L-1的HX溶液中c(H+)=1×10-6mol·L-1,HX![]() H++X-,c(X-)=c(H+),c(HX)≈0.10mol·L-1,K(HX)=
H++X-,c(X-)=c(H+),c(HX)≈0.10mol·L-1,K(HX)=![]() =
=![]() =1×10-11,故A错误;
=1×10-11,故A错误;
B. a点时c(OH-)=c(H+),由电荷守恒原理知,c(Na+)=c(X-),故B错误;
C. c点时,酸碱恰好反应完全,体积变为原来的2倍,溶质为NaX,根据物料守恒知c(Na+)+c(HX)+c(X-)=0.10mol·L-1,故C正确;
D.b点时,反应生成的NaX的物质的量与剩余的HX的物质的量相等,由于此时混合溶液显碱性,说明X-水解程度大于HX电离程度,故D错误;
故选C
10.C
解析:根据a点信息,可知pH=4时, ![]() ,即
,即![]() ,所以
,所以![]() ;同理,根据b点信息,可得
;同理,根据b点信息,可得![]() ,所以
,所以![]() ,故A正确;根据a点信息,pH=4,溶液呈酸性,则
,故A正确;根据a点信息,pH=4,溶液呈酸性,则![]() ,
,![]() 则,c(A-)=c(HA),根据电荷守恒:c(A-)+c(OH-)=c(Na+)+c(H+),由c(H+)>c(OH-),可推出c(A-)>c(Na+),c(A-)=c(HA)>c(Na+)>c(H+)>c(OH-),故B正确;根据A项分析可知,Ka(HB)<Ka(HA),由
则,c(A-)=c(HA),根据电荷守恒:c(A-)+c(OH-)=c(Na+)+c(H+),由c(H+)>c(OH-),可推出c(A-)>c(Na+),c(A-)=c(HA)>c(Na+)>c(H+)>c(OH-),故B正确;根据A项分析可知,Ka(HB)<Ka(HA),由![]() 知,
知, ![]() ,相同浓度下,NaA溶液的pH小于NaB溶液的pH,故C错误;根据
,相同浓度下,NaA溶液的pH小于NaB溶液的pH,故C错误;根据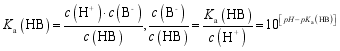 ,故D正确。
,故D正确。
11.D
12.C
13.C
解析:![]() 沉淀溶解平衡曲线起点的信息是
沉淀溶解平衡曲线起点的信息是![]() 、
、![]() (钨酸钙)的沉淀溶解平衡曲线起点的信息是
(钨酸钙)的沉淀溶解平衡曲线起点的信息是![]() 、
、![]() ,
,![]() ,故
,故![]() ,A项正确。a点时
,A项正确。a点时![]() 、
、![]() 或
或![]() ,故a点可表示
,故a点可表示![]() 悬浊液,B项正确。设饱和氢氧化钙溶液中钙离子浓度x,则氢氧根离子浓度为2x,
悬浊液,B项正确。设饱和氢氧化钙溶液中钙离子浓度x,则氢氧根离子浓度为2x,![]() ,即
,即![]() ,设饱和钨酸钙溶液中钙离子浓度为y,钨酸根离子也为y,则
,设饱和钨酸钙溶液中钙离子浓度为y,钨酸根离子也为y,则![]() ,C项不正确。氢氧化钙的溶解度随温度升高而降低,故加热饱和
,C项不正确。氢氧化钙的溶解度随温度升高而降低,故加热饱和![]() 溶液有白色氢氧化钙沉淀出现,D项正确。
溶液有白色氢氧化钙沉淀出现,D项正确。
14.B
解析:本题考查沉淀溶解平衡曲线。A项,a点到c点,c(R2-)不变,c(Fe2+)变大,而温度变化时,c(R2-)和c(Fe2+)是同时变化的,错误;B项,a、b是同一温度下的曲线上的两个不同的点,而相同温度下的相等,正确;C项,d点为不饱和溶液,不可能有沉淀析出,错误;D项,以b点数据计算,Ksp=2×10-9mol·L-1×1×10-9mol·L-1=2×10-18mol2·L-1,错误。
15.D
解析:由题意知,锌及其化合物的性质与铝及其化合物相似,则氢氧化锌是两性氢氧化物。由图可知,在a点,pH=7.0,lgc(Zn2+)=-3.0,所以c(OH-)=10-7mol/L、c(Zn2+)=10-3mol/L,Ksp[Zn(OH) 2]=10-17。当pH=8.0时,c(Zn2+)=  mol/L,当pH=12.0时,c(Zn2+)=
mol/L,当pH=12.0时,c(Zn2+)=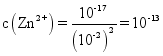 mol/L,所以pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108。A. 往ZnCl2溶液中加入过量氢氧化钠溶液,反应的离子方程式为Zn2++4OH-
mol/L,所以pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108。A. 往ZnCl2溶液中加入过量氢氧化钠溶液,反应的离子方程式为Zn2++4OH-![]() [Zn(OH)4]2-,A正确;B. 若要从某废液中完全沉淀Zn2+,由图像可知,通常可以调控该溶液的pH在8.0—12.0之间,B正确;C. pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108,C正确;D. 该温度时,Zn(OH)2的溶度积常数(Ksp)为1×l0-17,D不正确。本题选D。
[Zn(OH)4]2-,A正确;B. 若要从某废液中完全沉淀Zn2+,由图像可知,通常可以调控该溶液的pH在8.0—12.0之间,B正确;C. pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108,C正确;D. 该温度时,Zn(OH)2的溶度积常数(Ksp)为1×l0-17,D不正确。本题选D。
高考化学高频考点小题突破训练13物质的检验 含解析: 这是一份高考化学高频考点小题突破训练13物质的检验 含解析,共6页。试卷主要包含了白色固体混合物A,含有KCl,CuSO4和CaCO3,下列关于有机物的分离,由下列实验等内容,欢迎下载使用。
高考化学高频考点小题突破训练12离子反应 含解析: 这是一份高考化学高频考点小题突破训练12离子反应 含解析,共5页。试卷主要包含了下列化学过程及其表述正确的是等内容,欢迎下载使用。
高考化学高频考点小题突破训练10实验基础操作 含解析: 这是一份高考化学高频考点小题突破训练10实验基础操作 含解析,共8页。试卷主要包含了实验室中某些气体的制取,下列实验操作或装置正确的是等内容,欢迎下载使用。












