





2024年高考化学一轮总复习 第4单元 第1讲 碳、硅及无机非金属材料 课件
展开第1讲 碳、硅及无机非金属材料
复习目标1.了解C、Si单质及其重要化合物的制备方法、性质和用途。2.了解传统无机非金属材料的组成、性能及用途。3.了解新型无机非金属材料的性能及用途。
考点一 碳和硅的单质及其氧化物
半导体材料、硅芯片和硅太阳能电池
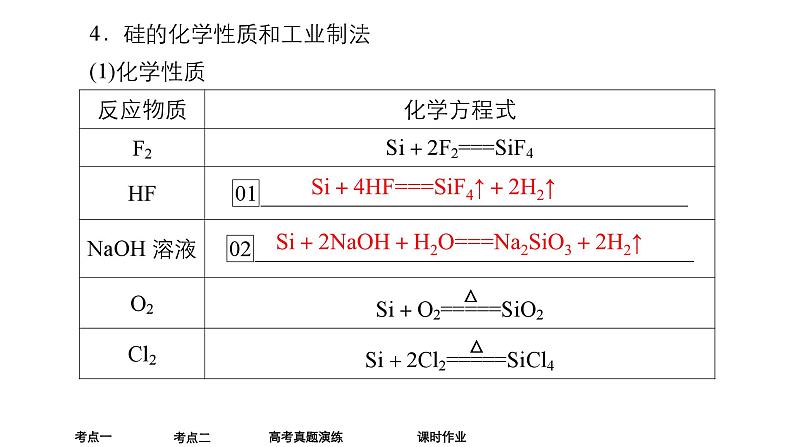
Si+4HF===SiF4↑+2H2↑
Si+2NaOH+H2O===Na2SiO3+2H2↑
SiO2+4HF===SiF4↑+2H2O
SiO2+2NaOH ===Na2SiO3+H2O
CO2+NaOH===NaHCO3
Na2SiO3+CO2↑
CaSiO3+CO2↑
H2SiO3↓+Na2CO3
H2SiO3↓+2NaHCO3
Na2O+CO2===Na2CO3
请指出下列各说法的错因(1)石墨转变为金刚石的反应属于氧化还原反应。错因:___________________________________________________(2)向CaCl2溶液中通入CO2气体,溶液变浑浊,继续通入CO2至过量,浑浊消失。错因:___________________________________________________(3)向空气中排放二氧化碳会形成酸雨。错因:___________________________________________________
同素异形体之间的转化,化合价不变,不是氧化还原反应。
由于盐酸的酸性比碳酸强,CO2与CaCl2溶液不反应。
pH<5.6的雨水才是酸雨,CO2不能形成酸雨。
在高温条件下生成CO而不是CO2。
SiO2能与氢氟酸反应。
Si不能用于制造光导纤维。
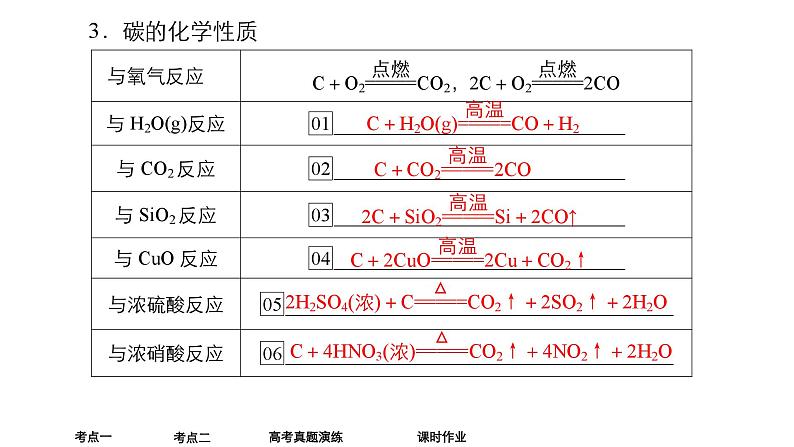
1.硅单质的特殊性(1)非金属单质跟碱液作用一般无H2放出,但Si与碱液作用却放出H2:Si+2NaOH+H2O===Na2SiO3+2H2↑。(2)非金属单质一般不跟非氧化性酸作用,但Si能与HF作用:Si+4HF===SiF4↑+2H2↑。(3)非金属单质大多为非导体,但Si为半导体。
角度一 碳及其重要化合物1.材料新秀——石墨烯和氧化石墨烯已成为物理、化学、材料科学研究的国际热点课题。其结构模型如图所示。下列有关说法正确的是( )A.石墨烯是一种新型化合物B.氧化石墨烯即石墨烯的氧化物C.二者和石墨都是碳的同素异形体D.氧化石墨烯具有一定的亲水性
2.下列关于碳及其氧化物的说法不正确的是( )A.过度排放CO2会导致“温室效应”,应提倡“低碳生活”B.CO、CO2、葡萄糖都属于有机物C.金刚石和石墨都是碳单质,但原子排列方式不同,物理性质也不同D.一氧化碳易与血液中的血红蛋白结合
角度二 硅和二氧化硅3.有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法,不正确的是( )A.高纯度的硅广泛用于制作计算机中的芯片B.硅可由二氧化硅还原制得C.低温时,硅与水、空气和一般酸不反应,但能与氢氟酸反应D.自然界中硅的储量丰富,自然界中存在大量的单质硅
5.常温下,下列各组物质不发生反应的是( )①硅与NaOH溶液 ②硅与盐酸 ③硅与氢氟酸 ④二氧化硅与碳酸钠 ⑤二氧化硅与浓硝酸 ⑥二氧化硅与NaOH溶液A.①②④ B.②④⑤C.②⑤⑥ D.③④⑥
硅及其化合物之间的转化
考点二 无机非金属材料
H2SiO3+2NaOH===Na2SiO3+2H2O
Na2SiO3+2HCl===2NaCl+H2SiO3↓
Na2SiO3+CO2+H2O===H2SiO3↓+Na2CO3
Na2SiO3、CaSiO3、SiO2
3.特殊功能的含硅物质(1)碳化硅具有类似金刚石结构,可用作磨料。(2)含硅元素4%的硅钢具有导磁性。(3)硅橡胶具有既耐高温又耐低温的性质。4.新型无机非金属材料(1)高温结构陶瓷:耐高温、耐磨蚀、抗氧化等优良性能。(2)超导陶瓷:有超导性,可用于电力、交通、医疗等领域。(3)压电陶瓷:具有压电效应。
请指出下列各说法的错因(1)生产水泥的原料主要是纯碱、石灰石和二氧化硅。错因:_________________________________________(2)玻璃容器可长期盛放各种酸。错因:_________________________________________(3)浓硫酸可刻蚀石英制艺术品。错因:_________________________________________(4)石英只能用于生产光导纤维。错因:_________________________________________(5)合成纤维和光导纤维都是新型无机非金属材料。错因:_________________________________________
生产水泥的原料主要是黏土和石灰石。
玻璃容器不能存放氢氟酸。
刻蚀石英制艺术品应该用氢氟酸。
石英可用于生产光导纤维、玻璃等。
一、常见的无机非金属材料、金属材料与复合材料
二、硅酸盐组成的表示通常用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成:1.氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔开。2.各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。如硅酸钠(Na2SiO3)可表示为Na2O·SiO2,长石(KAlSi3O8)可表示为K2O·Al2O3·6SiO2。
角度一 无机非金属材料1.“九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘我国古代精美的青瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法中正确的是( )A.硅酸盐制品的性质稳定、熔点较高B.玻璃是人类最早使用的硅酸盐制品C.制水泥的原料为纯碱、石灰石和石英D.沙子和黏土的主要成分均为硅酸盐
(1)用作半导体材料的是晶体硅,用于制作光导纤维的是SiO2,计算机芯片的成分是晶体硅。(2)水晶、石英、玛瑙、硅石的主要成分是SiO2。
角度二 硅酸盐组成的表示3.古瓷中所用颜料成分大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2Ox,铜为+2价)。下列关于硅酸铜钡的说法不正确的是( )A.x等于6B.性质稳定,不易脱色C.易溶解于强酸和强碱D.可用氧化物形式表示为BaO·CuO·2SiO2
4.中国科学院空天信息创新研究院根据玉兔二号提供的一个暗绿色闪光的“石块”信息进行分析,发现石块主要由约45%的斜长石(CaAl2Si2O8)、7%的辉石XYAl2-2nSi2O6(X、Y为单核离子,0
2.(2022·湖北高考)C60在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列关于该碳玻璃的说法错误的是( )A.具有自范性B.与C60互为同素异形体C.含有sp3杂化的碳原子D.化学性质与金刚石有差异
解析自范性是晶体性质,碳玻璃为非晶态,所以没有自范性,A错误。
4.(2021·山东高考)有利于实现“碳达峰、碳中和”的是( )A.风能发电 B.粮食酿酒C.燃煤脱硫 D.石油裂化
6.(2019·全国卷Ⅰ)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是( )A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
课时作业建议用时:40分钟
选择题(每小题只有1个选项符合题意)1.(2022·辽宁省大连市高三期末模拟)化学与生活、生产、社会可持续发展密切相关。下列有关化学知识的说法错误的是( )A.碳纳米管表面积大,可用作新型储氢材料B.我国发射的“北斗组网卫星”所使用的碳纤维,是一种非金属材料C.高纯二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路”D.我国发射的嫦娥五号探测器的太阳能电池帆板的材料是SiO2
2.有关碳、硅两种元素的说法中,不正确的是( )A.它们的原子都既不易得到电子也不易失去电子,主要形成四价的化合物B.碳元素在自然界中存在游离态,而硅元素在自然界中只有化合态C.它们的单质在空气中加热时都可以发生化学反应D.它们的单质都能和氢氧化钠溶液反应
3.下列说法不正确的是( )A.SiO2能与HF反应,因此可用HF刻蚀玻璃B.向Na2SiO3溶液中逐滴加入稀盐酸制备硅酸凝胶C.石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能D.氮化硅是一种重要的结构陶瓷材料,化学式为Si3N4
4.《本草纲目》中对玻璃有如下叙述:“本作颇黎。颇黎,国名也。其莹如水,其坚如玉,故名水玉,与水精(即水晶,主要成分为SiO2)同名……有酒色、紫色、白色,莹澈与水精相似”。下列说法错误的是( )A.文中所描述的玻璃颜色,来自某些金属氧化物B.玻璃质地坚硬,不易破碎C.将石灰石、纯碱、石英砂在高温下熔融,可制得普通玻璃D.不能用带有磨口玻璃塞的玻璃试剂瓶盛放NaOH溶液
解析该反应不能比较C、Si的非金属性,A错误;SiO2是H2SiO3的酸酐,B错误;两性氧化物是指和酸、碱反应生成盐和水的氧化物,二氧化硅和氢氟酸反应是其特殊性质,不能和其他酸发生反应,二氧化硅和碱溶液反应生成盐和水,是酸性氧化物,C错误。
6.科技的进步为二氧化碳资源化利用提供了广阔的前景。下列说法错误的是( )A.CO2是自然界碳循环中的重要物质B.CO2加氢转化为乙烯,CO2被还原C.CO2与环氧丙烷可合成可降解塑料D.CO2电催化时,在阳极转化为燃料
解析CO2在阴极得电子转化为燃料,D错误。
8.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
9.实验室用H2还原SiHCl3(沸点:31.85 ℃)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是( )A.装置Ⅱ、Ⅲ中依次盛装的是浓硫酸、冰水B.实验时,应先加热管式炉,再打开活塞KC.为鉴定制得的硅中是否含有微量铁单质,需要用到的试剂为盐酸、双氧水、KSCN溶液D.该实验中制备氢气的装置也可用于饱和食盐水与电石反应制备乙炔
11.SiO2是一种化工原料,可以制备一系列物质(如图)。下列说法错误的是( )A.图中所涉及反应都需在高温下进行B.纯净的二氧化硅和单晶硅都是信息产业的重要基础材料C.用盐酸可除去石英砂(主要成分为SiO2)中少量的碳酸钙D.制玻璃和陶瓷都需用SiO2
硅及其化合物在自然界广泛存在并被人类应用。氮化硅可用作高温陶瓷复合材料,在航空航天、汽车发动机、机械等领域有着广泛的应用。由石英砂合成氮化硅粉末的路线如图所示:其中—NH2中各元素的化合价与NH3相同。请回答下列问题:
第15讲 碳、硅及无机非金属材料(课件)-2024年高考化学一轮复习(新教材新高考): 这是一份第15讲 碳、硅及无机非金属材料(课件)-2024年高考化学一轮复习(新教材新高考),共60页。PPT课件主要包含了复习目标,网络构建,知识梳理题型归纳,真题感悟,内容索引,考情分析,PARTONE等内容,欢迎下载使用。
人教版高考化学一轮复习第4章非金属及其化合物第1讲碳硅及无机非金属材料课件: 这是一份人教版高考化学一轮复习第4章非金属及其化合物第1讲碳硅及无机非金属材料课件
高考化学一轮复习第4章非金属及其重要化合物第4讲碳硅及无机非金属材料课件: 这是一份高考化学一轮复习第4章非金属及其重要化合物第4讲碳硅及无机非金属材料课件,共60页。PPT课件主要包含了半导体,石灰石,石英砂,酸碱性,低残留,天然药物,合成药物等内容,欢迎下载使用。












