
2022-2023学年北京市第四中学高三(下)零模化学试卷含答案
展开绝密★启用前
2022-2023学年北京市第四中学高三(下)零模
化学试卷
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
3.考试结束后,本试卷和答题卡一并交回。
第I卷(选择题)
一、单选题(本大题共14小题,共14.0分)
1. 近年来,我国航空航天事业成果显著。下列成果所涉及的材料为金属材料的是( )
A. “天宫二号“航天器使用的质量轻强度高的材料钛合金
B. “北斗三号”导航卫星使用的太阳能电池材料砷化镓
C. “长征五号”运载火箭使用的高效燃料液氢
D. “”飞机身使用的复合材料碳纤维和环氧树脂
2. 下列物质的应用中,利用了氧化还原反应的是( )
A. 用石灰乳脱除烟气中的
B. 用明矾处理污水
C. 用盐酸去除铁锈主要成分
D. 用消毒液有效成分杀灭细菌
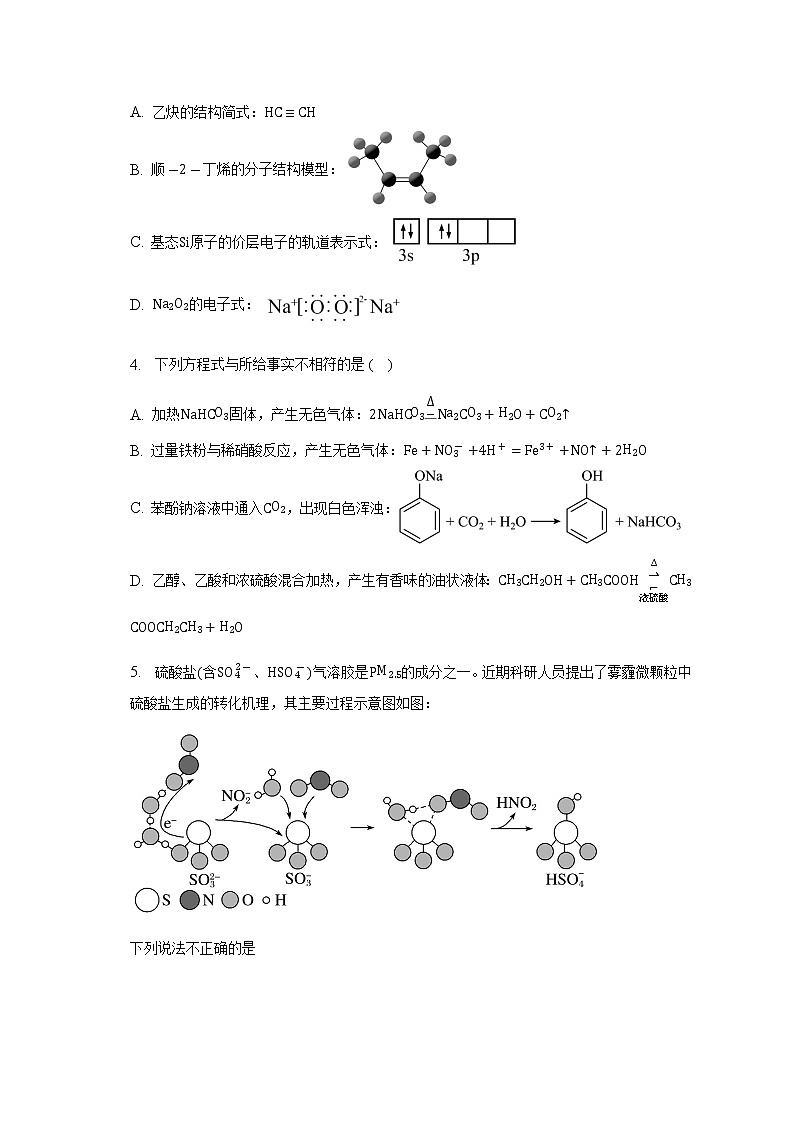
3. 下列化学用语或图示表达不正确的是( )
A. 乙炔的结构简式:
B. 顺丁烯的分子结构模型:
C. 基态原子的价层电子的轨道表示式:
D. 的电子式:
4. 下列方程式与所给事实不相符的是( )
A. 加热固体,产生无色气体:
B. 过量铁粉与稀硝酸反应,产生无色气体:
C. 苯酚钠溶液中通入,出现白色浑浊:
D. 乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:
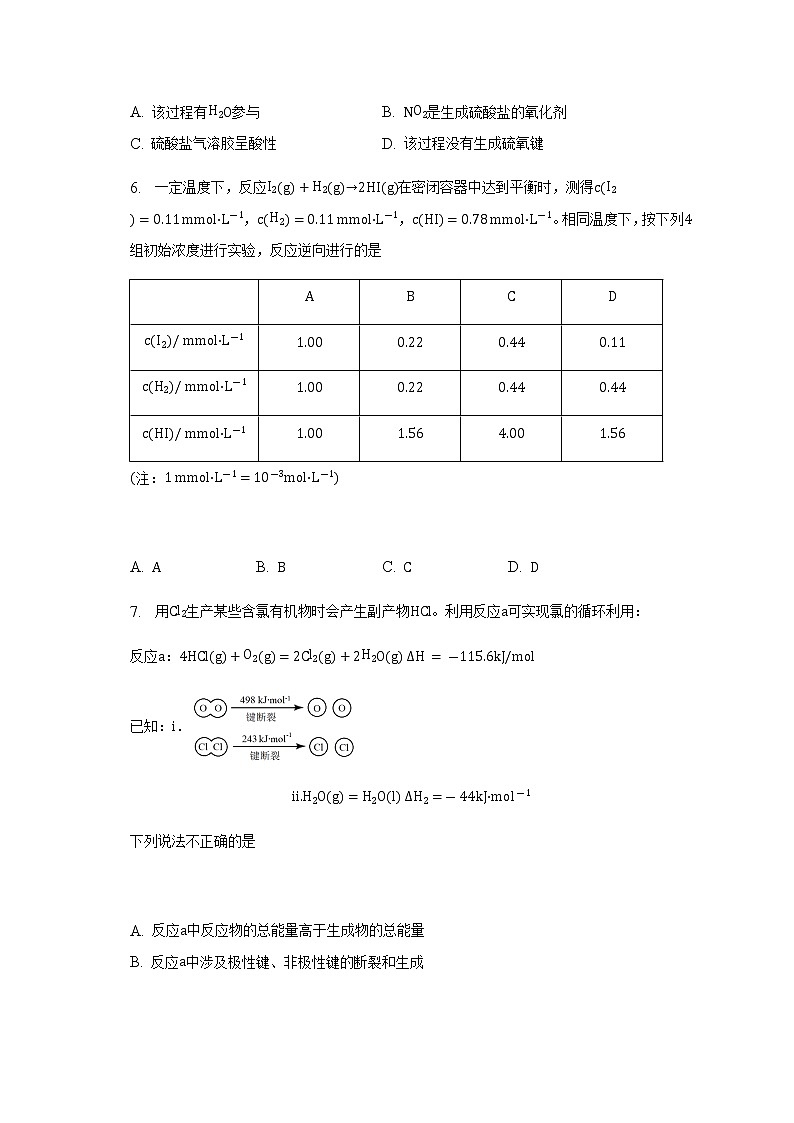
5. 硫酸盐含、气溶胶是的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是
A. 该过程有参与 B. 是生成硫酸盐的氧化剂
C. 硫酸盐气溶胶呈酸性 D. 该过程没有生成硫氧键
6. 一定温度下,反应在密闭容器中达到平衡时,测得,,。相同温度下,按下列组初始浓度进行实验,反应逆向进行的是
| ||||
注:
A. B. C. D.
7. 用生产某些含氯有机物时会产生副产物。利用反应可实现氯的循环利用:
反应:
已知:.
下列说法不正确的是
A. 反应中反应物的总能量高于生成物的总能量
B. 反应中涉及极性键、非极性键的断裂和生成
C.
D. 断开 键与断开 键所需能量相差约为
8. 下列实验结果不能作为相应定律或原理的证据之一的是阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子( )
| ||||
定律或原理 | 勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 |
实验方案 | ||||
结果 | 左球气体颜色加深,右球气体颜色变浅 | 烧瓶中冒气泡,试管中出现浑浊 | 测得为、的和 | 与的体积比约为 |
A. B. C. D.
9. 聚脲具有防腐、防水、耐磨等特性,合成方法如下:
下列说法不正确的是
A. 和通过加成反应形成聚脲 B. 一定条件下聚脲能发生水解反应
C. 苯环上的一氯代物有种 D. 与互为同系物
10. 锂电池具有广泛应用。用废铝渣含金属铝、锂盐等获得电池级的一种工艺流程如下部分物质已略去:
下列说法不正确的是
A. 中加热后有生成
B. 生成的离子方程式:
C. 由推测溶解度:
D. 中不宜通入过多,否则会造成产率降低
11. 我国科研人员将单独脱除的反应与的制备反应相结合,实现协同转化。
单独制备:,不能自发进行
单独脱除:,能自发进行
协同转化装置如图在电场作用下,双极膜中间层的解离为和,并向两极迁移。下列分析不正确的是
A. 反应释放的能量可以用于反应
B. 产生 的电极反应:
C. 反应过程中不需补加稀
D. 协同转化总反应:
12. 实验和实验中,均有气体产生。
下列分析不正确的是
A. 溶液中:
B. 中有生成
C. 中产生白色沉淀
D. 和中溶液的均增大
13. 以、为原料合成涉及的主要反应如下:
的平衡转化率、的选择性随温度、压强变化如下:
已知:
下列分析不正确的是
A.
B. 左右,体系发生的反应主要是
C. 由图可知,,
D. 初始、,平衡后、,若只发生、,则的平衡转化率为
14. 时,分别向支小试管中滴加滴溶液,再分别向其中滴加溶液,边滴加边振荡,实验数据及现象如下表:
试管编号 | ||||
滴加溶液的量 | 滴 | 滴 | 滴 | 滴 |
立即观察沉淀的颜色 | 浅绿色 | 浅绿色 | 蓝色 | 蓝色 |
酒精灯加热浊液后沉淀的颜色 | 浅绿色 | 浅绿色 | 黑色 | 黑色 |
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量溶液,产生大量白色沉淀。取蓝色沉淀重复上述实验,无白色沉淀。经检验,试管、中黑色沉淀中含有。
下列说法不正确的是
A. 由实验现象可知浅绿色沉淀中可能含有碱式硫酸铜
B. 溶液与溶液反应时,其相对量不同可以得到不同的产物
C. 试管、中的固体在加热过程中发生了反应:
D. 取浅绿色沉淀再滴加适量溶液后加热仍不会变黑
第II卷(非选择题)
二、实验题(本大题共1小题,共10.0分)
15. 某小组探究溶液、溶液与碱的反应,探究物质氧化性和还原性的变化规律。将一定浓度溶液,饱和混合溶液加入适量氨水,产生红褐色沉淀,经检验,红褐色沉淀含
分析产生的原因:氧化所致。
验证:向溶液中滴入氨水,生成的白色沉淀迅速变为灰绿色,一段时间后有红褐色沉淀生成。
生成白色沉淀的离子方程式是___________。
产生红褐色沉淀:。电极反应式:还原反应:。氧化反应:___________。
提出问题:产生的原因可能是氧化所致。
验证如下溶液:饱和溶液溶液;已排除空气的影响:
序号 | 实验 | 试剂 | 现象 |
氨水 | 生成沉淀,一段时间后,产生红褐色沉淀和灰黑色固体物质 | ||
水 | 溶液无明显变化 |
中可能产生,运用氧化还原反应规律分析产生的合理性:___________。
检验:滤出中不溶物,用稀溶解,未检出。分析原因:
中未生成。
中生成了。由于___________用离子方程式表示,因此未检出。
设计实验确认的作用已排除空气的影响,装置示意图如下所示。
补全电化学装置示意图___________。经检验,实验中产生了、。
、中均含。中产生了,中未产生,试解释原因___________。
分别与溶液、银氨溶液混合并加热,与溶液混合物明显现象,但与银氨溶液混合能产生银镜。试解释原因:___________。
三、简答题(本大题共3小题,共15.0分)
16. 碳酸二甲酯是一种绿色化工原料。用于汽车、医疗器械等领域。以甲醇为原料生产碳酸二甲酯的反应过程如下。
碳酸二甲酯分子中羰基碳原子的杂化类型是_______。
中,基态的价电子排布式为_______,在生产碳酸二甲酯的反应过程中所起的作用是_______。
上述方法中,甲醇单位时间内的转化率较低。为分析原因,查阅如下资料。
甲醇单位时间内的转化率主要受Ⅰ价铜元素浓度的影响。
在甲醇中溶解度较小,且其中的易被氧化为难溶的。
加入甲基咪唑可与形成配合物,可提高甲醇的转化率。甲基咪唑中,号原子的孤电子对因参与形成大键,电子云密度降低。
请结合信息回答以下问题。
甲基咪唑中,号原子_______填“在”或“不在”同一平面上,_______填“”或“”号原子更容易与形成配位键。
加入甲基咪唑后,甲醇转化率提高,可能的原因是_______填序号。
Ⅰ配合物中的结构可增大其在甲醇中的溶解度
形成的Ⅰ配合物能增大反应的限度
配位原子提供孤电子对的能力是影响配体与之间配位键强度的一个重要因素。若用某结构相似的含配体与配位,所得配合物的稳定性比含配体低,可能的原因是_______。
的晶胞如图所示,金属离子与氧离子间的作用力为_______,的配位数是_______。一种立方钙钛矿结构的金属卤化物光电材料的组成为、和有机碱离子,其晶胞如图所示。其中与图中_______的空间位置相同,有机碱中,原子的杂化轨道类型是_______;若晶胞参数为,则晶体密度为_______列出计算式。
17. 从矿石中提取金是获取贵金属的主要来源。
俗话说“真金不怕火炼”,从化学性质角度解释其原因是_______。
用硫代硫酸盐在弱碱性条件下浸金是提取金的一种方法。
补全反应的离子方程式_______。
口口口_______口口_______
简述在金被氧化过程中的作用: _______。
工业上常用溶液、氨水和溶液为原料配制浸金液,其一种可能的浸金原理示意图如下。
上述原理可知,在浸金过程中起_______作用。
为了验证上述原理中的作用,进行如下实验。
实验现象:反应一段时间后,温度无明显变化,形管内液柱左高右低,锥形瓶中溶液蓝色变浅,打开瓶塞后
打开瓶塞后,_______填实验现象,证实了上述原理。
中现象对应反应的离子方程式是_______。
下图表示相同时间内,配制浸金液的原料中对浸金过程中消耗率和浸金量的影响其他条件不变。
已知:
结合图,解释图中浸金量先上升后下降的原因:_______。
18. 用零价铁去除含氮废水中的硝酸盐是环境修复的重要方法。一种去除的过程如下。
Ⅱ中充分反应后,分离混合物的方法是_______。
Ⅱ中反应的离子方程式是_______。
实验发现,在Ⅱ中补充一定量的可以明显提高的去除率。向两份含氮废水中均加入足量粉,做对比研究。
实验序号 | ||
所加试剂 | 粉 | 粉、 |
的去除率 |
分析中的去除率提高的原因:
直接还原了。
通过计算说明电子得、失数量关系:_______,证明该原因不合理。
研究发现:导电覆盖在铁粉表面;随着反应的进行,产生不导电,它覆盖在表面,形成钝化层,阻碍电子传输。
能与反应生成。
用做同位素示踪实验,证明该原因合理。
破坏钝化层。
将中的替换为 _______,的去除率约为,证明该原因不合理。
、中均能发生。该反应明显有助于中的去除,结合方程式解释原因: _______。
测定含量
步骤取含氮水样,加入催化剂、标准溶液过量,再加入稀。
步骤用标准溶液滴定剩余的被还原为,终点时消耗。
已知:
水样中的含量为 _______。
溶液中影响测定。向步骤中加入适量,产生驱赶,否则会使测定结果 _______填“偏大”或“偏小”。
四、推断题(本大题共1小题,共10.0分)
19. 香豆素类化合物在药物中应用广泛。香豆素类化合物的合成路线如图。
已知:
的化学方程式是_______。
的分子式是_______。
条件是_______。
的结构简式是_______。
可以生成,的结构简式是_____。
下列说法不正确的是_______填序号。
可以用酸性溶液鉴别和
可以发生加聚反应、还原反应和取代反应
最多可以和反应
为线型不稳定分子,经过两步反应,苯环上的一氯代物有种。
的结构简式是_______。
的化学反应类型是_______。
答案
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
溶液中发生了氧化还原反应,升价产物有,降价产物有是合理的
、
中的还原性较弱,不能将还原为;中,产生氢氧化亚铁,,碱性增强及产生更小的使亚铁盐的还原性增强,能将还原为
,加入氨水提高了的还原性,能与银氨溶液产生银镜
16.【答案】
;催化剂
在 ;
电负性:,对孤电子对吸引力强,使得作配体时配位能力弱
离子键 ; ; ; ;
17.【答案】在高温条件下不与反应
与形成配合物,提高的还原性
催化 锥形瓶中溶液蓝色复原 ; 当时,随着的增大, 的浓度增大,浸金速率增大;当时,游离的消耗 ,使 浓度减小,浸金速率减小
18.【答案】过滤
还原 所需电子:,最多提供的电子:。失去的电子数明显小于 所需电子数;
,破坏了钝化层
;偏大
19.【答案】
水溶液,
加成反应
2022-2023学年北京市第四中学高三(下)零模化学试卷含解析: 这是一份2022-2023学年北京市第四中学高三(下)零模化学试卷含解析,共26页。试卷主要包含了0分), 硫酸盐气溶胶是PM2,6kJ·ml−1, 锂电池具有广泛应用等内容,欢迎下载使用。
2022-2023学年北京师范大学附属实验中学高三(下)零模化学试卷(含解析): 这是一份2022-2023学年北京师范大学附属实验中学高三(下)零模化学试卷(含解析),共27页。试卷主要包含了0分)等内容,欢迎下载使用。
北京市西城区2022-2023学年高三下学期一模考试化学试卷(word版,含答案): 这是一份北京市西城区2022-2023学年高三下学期一模考试化学试卷(word版,含答案),共10页。试卷主要包含了6×10−12 Ksp=1,3,不同温度下反应的结果如图等内容,欢迎下载使用。












