



鲁科版 (2019)选择性必修2第4节 分子间作用力完整版ppt课件
展开冰山融化现象是物理变化还是化学变化?
冰山融化过程中有没有破坏其中的化学键?
那为什么冰山融化过程仍要吸收能量呢?
分子间存在着将分子聚集在一起的作用力,这种作用力称为分子间作用力.常见的为范德华力和氢键
二、范德华力: 是分子间普遍存在的,使许多物质聚集在一起且能以一定的凝聚态(固态,液态)存在的一种相互作用力。
分子间作用力范围很小,即分子充分接近时才有相互间的作用力。且是一类弱相互作用力
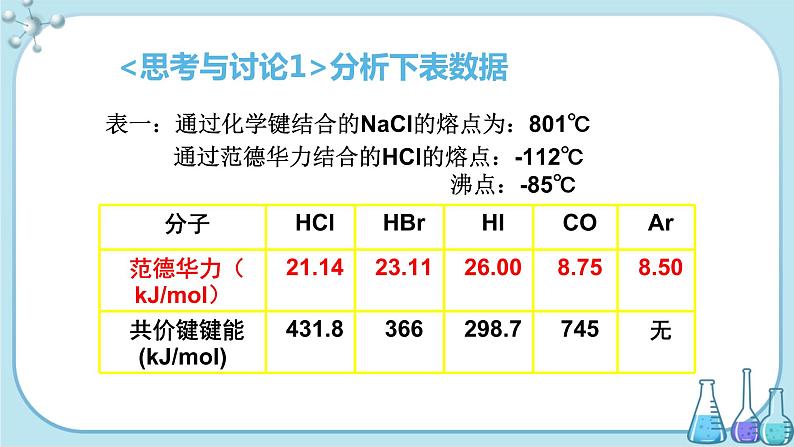
表一:通过化学键结合的NaCl的熔点为:801℃
通过范德华力结合的HCl的熔点:-112℃ 沸点:-85℃
<思考与讨论1>分析下表数据
(一)、范德华力及其影响因素
1、范德华力:分子之间的相互作用力,很弱. 比化学键小得很多, 化学键一般为100-600kJ/ml, 范德华力一般为2-20kJ/ml;只能在很小的范围内存在。不属于化学键。
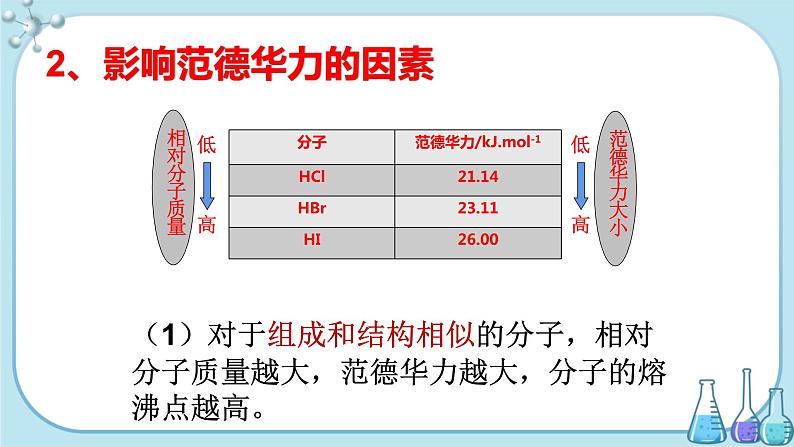
2、影响范德华力的因素
(1)对于组成和结构相似的分子,相对分子质量越大,范德华力越大,分子的熔沸点越高。
2.范德华力的影响因素
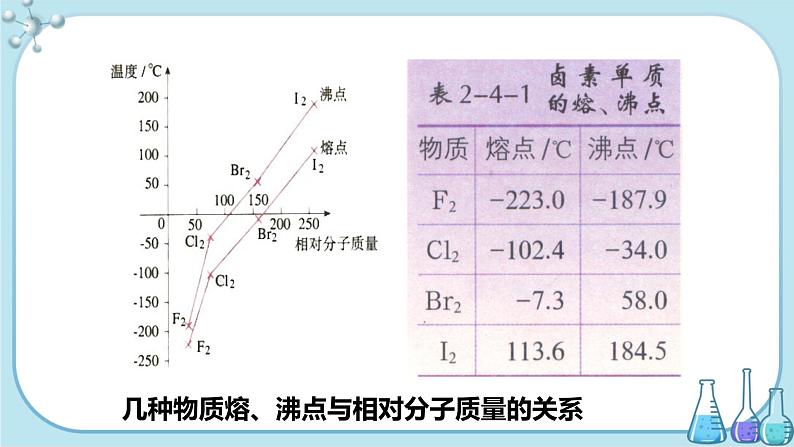
几种物质熔、沸点与相对分子质量的关系
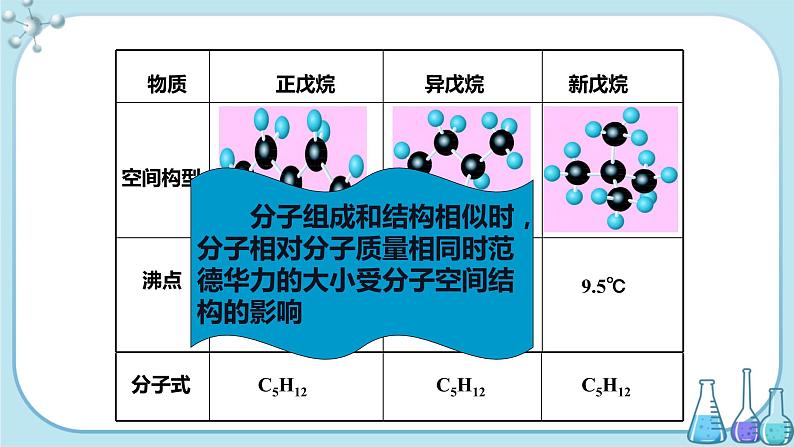
分子组成和结构相似时,分子相对分子质量相同时范德华力的大小受分子空间结构的影响
⑵相对分子质量相同或相近时,分子结构越不对称,分子的极性越大,范德华力就越大,熔沸点越高。
范德华力的大小对由分子构成的物质的物理性质有重要的影响,如熔点、沸点、溶解度等。
3、范德华力对分子构成的物质性质的影响
⑴、分子构成的物质,组成和结构相似,其相对分子质量越大,则范德华力越大,物质的熔沸点越高;相对分子质量相近,分子结构越不对称,分子极性越大,物质的熔沸点越高。
⑵、若溶质分子能与溶剂分子形成较强的范德华力,则溶质在该溶剂中的溶解度较大
(1)将干冰气化,破坏了CO2分子晶 体的 。
(2)将CO2气体溶于水,破坏了CO2 分子 。
(3)解释CCl4(液体)CH4及CF4是气体, CI4是固体的原因。
它们均是正四面体结构,它们的分子间作用力随相对分子质量增大而增大,相对分子质量越大,分子间作用力越大。
分子间作用力大小: CI4> CCl4 >CF4 >CH4
范德华力及其对物质性质的影响
1、范德华力:把分子聚集在一起的作用力。
范德华力很弱,约比化学键能小1-2数量级
(2) 范德华力与相对分子质量的关系
结构相似,相对分子质量越大,范德华力越大
(3)范德华力与分子的极性的关系
相对分子质量相同或相近时,分子的极性越大,范德华力越大
(4)范德华力对物质熔沸点的影响
结构相似的分子,相对分子质量越大,范德华力越大,分子的熔沸点越高。
分子间作用力范围很小,即分子充分接近时才有相互间的作用力。
分子间作用力主要影响物质的熔点、沸点、溶解性等物理性质,而化学键主要影响物质的化学性质。
比较下列物质的熔沸点H2O_ H2S _ H2Se _ H2TeH2O < H2S < H2Se < H2Te
非金属元素的氢化物在固态时是分子晶体,其熔沸点与其分子量有关.对于同一主族非金属元素而言,从上到下,分子量逐渐增大,熔沸点应逐渐升高.而HF、H2O、NH3却出现反常,为什么?
说明在HF、H2O、NH3分子间还存在除分子间作力之外的其他作用.这种作用就是氢键.
氢键是一种特殊的分子间作用力,它是由已经与电负性很强的原子(N、O、F)形成共价键的氢原子与另一分子中电负性很强的原子之间的作用力.
二、氢键及其对物质性质的影响
是一种静电作用,是除范德华力之外的另一种分子间作用力.
注意:只有分子充分接近时,氢键作用才明显,如固体和液体中;而气体中往往忽略
(1)分子中含有半径小、电负性大、带孤电子对的非金属原子(N、O、F)。
(2)分子中必须有一个与N(O或F)直接相连的H原子 。
(1)饱和性:一个X—H只能和一个Y原子结合;(2)方向性:X—H…Y尽可能在一条直线上
(1)氢键键能大小范围
不属于化学键,但也有键长、键能。氢键键能大小介于化学键与范德华力之间,一般不超过40kJ/ml
如F原子得电子能力最强,因而F-H…F是最强的氢键; 原子吸引电子能力不同,所以氢键强弱变化顺序为:
F-H…F > O-H…O > O-H…N > N-H…NC原子吸引电子能力较弱,一般不形成氢键。
与X和Y原子的电负性及半径大小有关, 电负性大,半径小,则氢键强。
(不属于分子间作用力)
某些物质在分子内也可形成氢键,例如当苯酚在邻位上有—CHO、—COOH、—OH和—NO2时,可形成分子内的氢键,组成“螯合环”的特殊结构.
氢键普遍存在于已经与N、O、F形成共价键的氢原子与另外的N、O、F原子之间。 如:HF、H2O、NH3 相互之间 C2H5OH、CH3COOH、H2O相互之间
(2)分子内氢键:
例如 (1)分子间氢键:
高中鲁科版 (2019)第2章 微粒间相互作用与物质性质第4节 分子间作用力多媒体教学ppt课件: 这是一份高中鲁科版 (2019)<a href="/hx/tb_c4002604_t3/?tag_id=26" target="_blank">第2章 微粒间相互作用与物质性质第4节 分子间作用力多媒体教学ppt课件</a>,共35页。PPT课件主要包含了相互作用,范德华力,相互作用力,凝聚态,小得多,电性作用,无饱和性,无方向性,相对分子质量,正电荷等内容,欢迎下载使用。
鲁科版 (2019)选择性必修2第4节 分子间作用力作业ppt课件: 这是一份鲁科版 (2019)选择性必修2<a href="/hx/tb_c4002604_t3/?tag_id=26" target="_blank">第4节 分子间作用力作业ppt课件</a>,共44页。PPT课件主要包含了NCSiNa,三角锥形,NH3,SiH4,sp杂化,直线形,NHO,NHN等内容,欢迎下载使用。
选择性必修2第4节 分子间作用力作业课件ppt: 这是一份选择性必修2<a href="/hx/tb_c4002604_t3/?tag_id=26" target="_blank">第4节 分子间作用力作业课件ppt</a>,共44页。PPT课件主要包含了NCSiNa,三角锥形,NH3,SiH4,sp杂化,直线形,NHO,NHN等内容,欢迎下载使用。













