




2024届高三化学高考备考一轮复习:卤代烃 醇与酚 醛与酮课件
展开1.根据碳卤键的极性,理解卤代烃的结构和性质,并关注卤代烃在有机合成中的桥梁作用。了解卤代烃对环境的影响。 2.能根据醇羟基和酚羟基的特点和反应规律推断含羟基有机物的化学性质,根据有关信息书写相应反应的化学方程式,能利用它们的主要性质进行鉴别。 3.能描述说明、分析解释醛、酮的重要反应,能书写相应的化学方程式。 4.认识醛、酮等物质对人类生活的影响及在生产、生活中的重要应用。
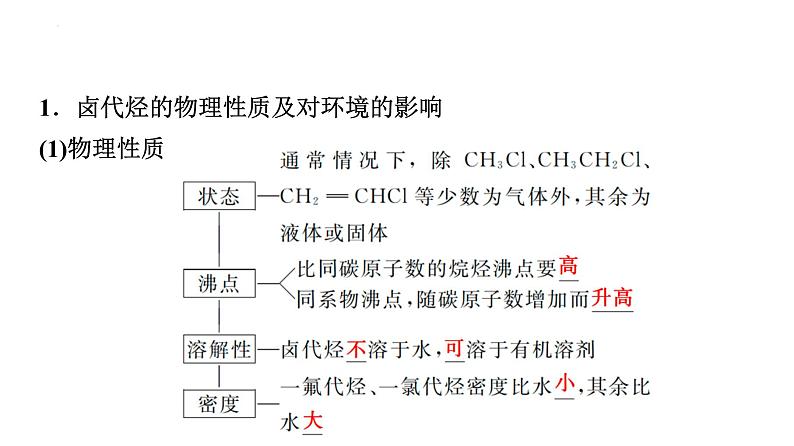
1.卤代烃的物理性质及对环境的影响(1)物理性质
(2)卤代烃对环境的影响氟氯代烷在大气平流层中会破坏臭氧层,是造成“臭氧空洞”的主要原因。
氢氧化钠的水溶液、加热
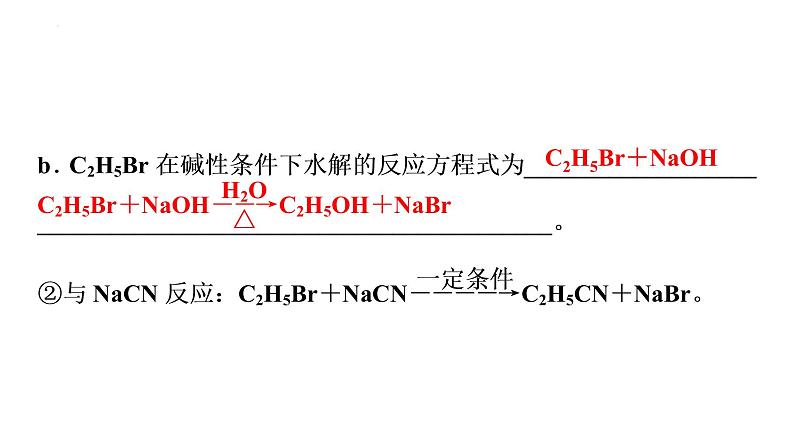
C2H5Br+NaOH
(2)消去反应①概念有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键(如碳碳双键或碳碳三键)的化合物的反应。②反应条件:____________________________________________。③溴乙烷发生消去反应的化学方程式:________________________ _______________________________________。
强碱(如NaOH或KOH)的醇溶液、加热
CH2===CH2↑+NaBr+H2O
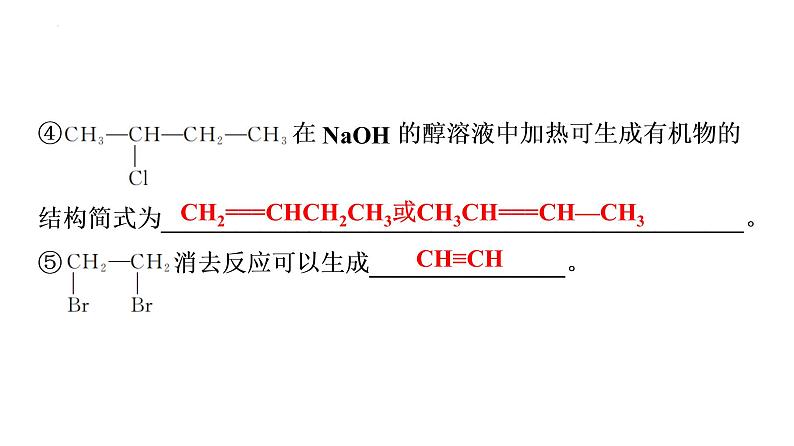
CH2===CHCH2CH3或CH3CH===CH—CH3
(2)不饱和烃的加成反应,如丙烯与Br2的反应:_________________ _____________________________。
CH3—CH===CH2
+Br2―→CH3—CHBr—CH2Br
3.卤代烃的获取方法(1)取代反应(写出化学方程式)①乙烷与Cl2生成一氯乙烷:________________________________ _______; ②苯与Br2:______________________________;③C2H5OH与HBr:____________________________________。
1.判断正误(正确的打“√”,错误的打“×”)(1)一氯甲烷、二氯甲烷、三氯甲烷在常温常压下均为液体。( )(2)所有卤代烃均可以燃烧。( )(3)CH3CH2Cl的沸点比CH3CH3的沸点高。 ( )(4)溴乙烷与NaOH的乙醇溶液共热生成乙烯。( )(5)在溴乙烷中加入AgNO3溶液,立即产生淡黄色沉淀。( )
(6)取溴乙烷的水解液,向其中加入AgNO3溶液,可观察到淡黄色沉淀。 ( )(7)所有卤代烃都能够发生水解反应和消去反应。( )[答案] (1)× (2)× (3)√ (4)√ (5)× (6)× (7)×
2.(1)2-氯丙烷发生消去反应和水解反应的化学方程式为_________ ________________________________________________________,________________________________________________________。(2)写出下列物质的加聚反应方程式①氯乙烯:______________________________________________,②四氟乙烯:____________________________________________。
卤代烃的性质与检验1.下列关于甲、乙、丙、丁四种有机物说法正确的是( )A.四种物质中分别加入氯水,均有红棕色液体生成B.四种物质中加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
C.四种物质中加入NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成D.乙发生消去反应得到两种烯烃B
2.某卤代烷烃C5H11Cl发生消去反应时,可以得到两种烯烃,则该卤代烃的结构简式可能为( )A.CH3CH2CH2CH2CH2Cl
卤代烃的水解反应和消去反应规律(1)水解反应规律①所有卤代烃在NaOH的水溶液中均能发生水解反应。②多卤代烃水解可生成多元醇。(2)消去反应规律①两类卤代烃不能发生消去反应a.与卤素原子相连的碳原子没有邻位碳原子。b.与卤素原子相连的碳原子有邻位碳原子,但邻位碳原子上无氢原子。
②有两种或三种邻位碳原子且碳原子上均带有氢原子时,发生消去反应可生成不同的产物。
卤代烃在有机合成中的桥梁作用3.根据下面的反应路线及所给信息填空。(1)A的结构简式是________,名称是________。(2)①的反应类型是______;③的反应类型是______。(3)反应④的化学方程式是__________________________________。
卤代烃在有机合成中的四大作用(1)桥梁作用
(3)改变官能团的位置
一、醇1.醇的组成、结构与分类(1)醇是脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基取代后的生成物。饱和一元醇的分子通式为___________________。(2)乙醇的结构
CnH2n+1OH(n≥1)
2.醇类物理性质的变化规律
3.常见的重要醇(1)甲醇:俗称木醇,无色具有挥发性的液体,有毒。(2)乙二醇:无色、无臭,具有甜味的黏稠液体,为二元醇,能与水以任意比互溶,作为汽车发动机防冻液的主要成分。(3)丙三醇:俗称甘油,无色、无臭,具有甜味的黏稠液体,能与水以任意比互溶,具有很强的吸水能力,丙三醇主要用于制造日用化妆品和三硝酸甘油酯(俗称硝化甘油)。
4.醇类的化学性质(1)根据结构预测醇类的化学性质醇的官能团羟基(—OH),决定了醇的主要化学性质,受羟基的影响,C—H的极性增强,在一定条件下也可能断键发生化学反应。(2)醇分子的断键部位及反应类型
完成下列条件下的化学方程式,并指明断键部位。a.与Na反应——断________键__________________________________________________________b.催化氧化——断________键 __________________________________________________________
2RCH2CH2OH+2Na―→2RCH2CH2ONa+H2↑
c.与HBr的取代——断________键 ________________________________________________________d.浓硫酸,加热,分子内脱水——断________键 ________________________________________________________e.与乙酸的酯化反应——断________键 _______________________________________________________
f.浓硫酸,加热,分子间脱水生成醚——断________键 _________________________________________________________ 醇与卤代烃均可以发生消去反应生成烯烃,但前者的反应条件是浓硫酸、加热至一定温度,后者反应条件为NaOH的醇溶液、加热。
二、酚1.酚的组成与结构(1)酚是羟基与苯环______相连而形成的化合物,最简单的酚为_________________,官能团名称为______。(2)苯酚的组成和结构结构简式:
3.酚的化学性质(1)弱酸性电离方程式为_______________________________,苯酚俗称石炭酸,但酸性很弱,不能使紫色石蕊试液变红。①与活泼金属反应:2C6H5OH+2Na―→____________________。
2C6H5ONa+H2↑
C6H5OH+NaOH―→C6H5ONa+H2O
C6H5ONa+CO2+H2O―→C6H5OH+NaHCO3
③与盐的反应:C6H5OH+Na2CO3===______________________。(2)取代反应苯酚与饱和溴水反应,产生白色沉淀,反应的化学方程式为 ________________________________________。该反应能产生白色沉淀,常用于苯酚的定性检验和定量测定。
C6H5ONa+NaHCO3
(3)显色反应苯酚与FeCl3溶液作用显___色,利用这一反应可检验苯酚的存在。(4)氧化反应苯酚易被空气中的氧气氧化而显______色;易被酸性高锰酸钾溶液氧化;容易燃烧。
苯酚的性质体现了基团之间的相互影响,苯环对羟基影响,使酚具有弱酸性,同样—OH对苯环影响,使酚易发生取代反应。
1.判断正误(正确的打“√”,错误的打“×”)(1)羟基与烃基相连形成的有机物为醇。( )(2)醇易溶于水的主要原因是醇与水分子形成氢键。( )
(5)2-丁醇发生消去反应只能生成2-丁烯。( )(6)所有酚在一定条件下均与浓溴水发生取代反应。( )[答案] (1)× (2)√ (3)× (4)× (5)× (6)×
2.写出下列反应的化学方程式(1)2-丙醇分子间脱水生成醚:________________________________(2)2-丙醇消去反应:________________________________________(3)苯酚钠溶液中通入少量CO2:______________________________
醇、酚的结构与性质1.中国茶文化源远流长。茶水中的儿茶素(如图)具有抗肿瘤、抗氧化等药理作用。下列有关儿茶素的说法错误的是( )A.可利用茶水检测补铁剂是否变质B.1 ml 儿茶素最多可与5 ml NaOH发生反应C.儿茶素可以发生消去反应D.1 ml 儿茶素最多与5 ml Br2发生反应
2.木质素是一种非糖类膳食纤维。其单体之一芥子醇的结构简式如图所示,下列有关芥子醇的说法正确的是 ( )A.芥子醇分子中有三种含氧官能团B.芥子醇分子中所有碳原子不可能在同一平面上C.1 ml芥子醇与足量浓溴水反应,最多消耗3 ml Br2D.芥子醇能发生的反应有氧化反应、取代反应、加成反应
3.分子式为C5H12O,既能发生催化氧化生成醛又能发生消去反应生成烯烃的醇结构简式:________________________(写键线式)。[答案]
醇、酚的性质规律(1)醇催化氧化规律醇类的催化氧化反应情况与跟羟基相连的碳原子上的氢原子个数有关。
(2)醇消去反应的规律醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,并且此相邻的碳原子上必须连有氢原子时,才可发生消去反应,生成不饱和键。表示为(3)酚与溴水反应的取代位置酚分子中与—OH处于邻、对位上的氢原子可以被—Br取代,而间位上的氢原子不可以被—Br取代。
废水中提取苯酚4.某工业废水(含苯酚)处理得到苯酚的实验方案如下:请回答下列问题:(1)设备①②中进行的分离操作为___________________________。(2)方案中的A、B物质分别是______________、______________(填化学式)。
(3)设备③中发生反应的化学方程式为__________________________ _______________________________________________________。(4)该方案中,能循环使用的物质有__________________________。
1.醛、酮的组成与结构
碳原子数相同的饱和一元醛和饱和一元酮互为同分异构体。
2.醛(R—CHO)的化学性质(1)羰基的加成反应①催化加氢——还原反应
RCOONH4+2Ag↓+3NH3
RCOONa+Cu2O↓+3H2O
①银氨溶液和新制的Cu(OH)2要现用现配,不能久置,二者均可以用于鉴别有机物中是否含—CHO。②配制银氨溶液时,先向洁净试管中加入AgNO3溶液,然后逐滴加入氨水,至沉淀刚好溶解为止。③配制新制的Cu(OH)2时要向NaOH溶液中滴加几滴CuSO4溶液,保证NaOH过量。
④做银镜实验时,a.试管不洁净;b.水浴加热温度控制不合理,或者用酒精灯直接加热;c.加热时振荡和摇动试管;d.乙醛用量太多,没有保持碱性环境等得不到光亮的银,而得到灰黑色的沉淀物。⑤银镜可以用稀硝酸洗涤。
1.判断正误(正确的打“√”,错误的打“×”)(1)凡是能发生银镜反应的有机物都是醛。( )(2)甲醛是常温下呈气态的烃的含氧衍生物。( )(3)丙醛和丙酮互为同分异构体,不能用核磁共振氢谱鉴别。( )(4)醛类物质发生银镜反应或与新制的Cu(OH)2的反应均需在碱性条件下。 ( )(5)醛类化合物既能发生氧化反应又能发生还原反应。( )(6)丙酮与水互溶的原因是丙酮与水分子间可以形成氢键。( )[答案] (1)× (2)√ (3)× (4)√ (5)√ (6)√
2.写出下列化学方程式。(1)苯甲醛与O2反应生成苯甲酸:___________________________,(2)苯甲醛的银镜反应:____________________________________,(3)苯甲醛与HCN的加成反应:_____________________________,(4)丙酮与H2的加成反应:_________________________________。
醛、酮的结构与性质及其检验1.下列有关醛的判断正确的是 ( )A.乙醛和丙烯醛( )不互为同系物,它们与氢气充分反应后的产物也不互为同系物B.1 ml HCHO发生银镜反应最多生成2 ml AgC.对甲基苯甲醛( )使酸性高锰酸钾溶液褪色,说明它含有醛基D.能发生银镜反应的有机物不一定是醛类,甲酸乙酯也可发生银镜反应
2.有机物A、B均为合成某种抗支气管哮喘药物的中间体,A在一定条件下可转化为B(如图所示),下列说法正确的是( )A.要检验B中含 ,可向其中加入溴水B.用FeCl3溶液可检验物质B中是否混有AC.物质B既能发生银镜反应,又能发生水解反应D.1 ml B最多可与5 ml H2发生加成反应
3.甲醛分子中可看作有两个醛基,按要求解答下列问题:(1)写出碱性条件下,甲醛与足量银氨溶液反应的离子方程式:________________________________________________________。(2)计算含有0.30 g甲醛的水溶液与过量银氨溶液充分反应,生成的银质量为________。
(1)醛基(—CHO)检验中的物质的量关系①定性检验
醛、酮在有机合成中的应用4.已知醛或酮可与格氏试剂(R′MgX)发生加成反应,所得产物经水解可得醇:若用此种方法制取HOC(CH3)2CH2CH3,可选用的醛或酮与格氏试剂是( )
5.已知:醛分子在稀碱溶液存在下,可发生羟醛缩合反应,生成羟基醛,如:试写出以乙烯为原料合成正丁醇的各步反应的化学方程式。
2024届高三化学一轮复习课件:烃的衍生物(一) 卤代烃 醇 酚 醛和酮: 这是一份2024届高三化学一轮复习课件:烃的衍生物(一) 卤代烃 醇 酚 醛和酮,共3页。PPT课件主要包含了卤素原子,碳卤键,ROH,浅黄色,溴原子,2苯酚的物理性质,被氧化,置换反应,取代反应,氧化反应等内容,欢迎下载使用。
2024届高三化学高考备考一轮复习专题:卤代烃 醇 酚课件: 这是一份2024届高三化学高考备考一轮复习专题:卤代烃 醇 酚课件,共46页。PPT课件主要包含了卤素原子,碳卤键,物理性质,化学性质,不饱和键,卤代烃的制备,课堂点拨,醇的概述,醇类的物理性质,醇类的化学性质等内容,欢迎下载使用。
2024届高三化学高考备考一轮复习专题:卤代烃、醇、酚、醛、酮和羧酸课件: 这是一份2024届高三化学高考备考一轮复习专题:卤代烃、醇、酚、醛、酮和羧酸课件,共57页。












