


高中化学人教版 (2019)选择性必修1第二节 电解池授课课件ppt
展开1. 了解电解饱和食盐水的工作原理。2. 了解电镀、电解精炼铜、电冶金的原理。
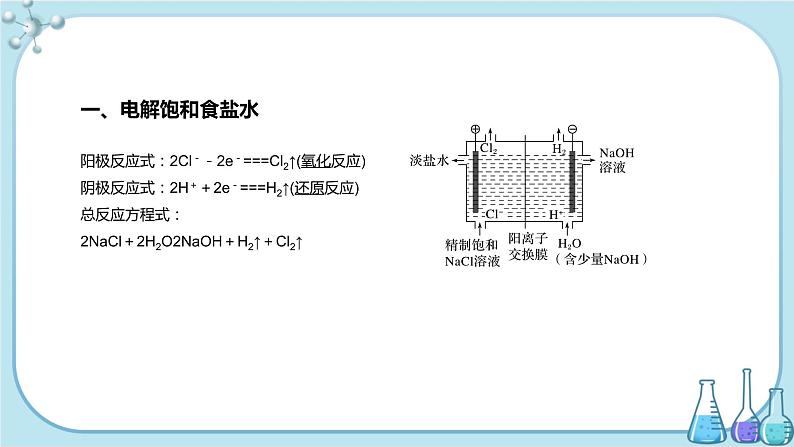
阳极反应式:2Cl--2e-===Cl2↑(氧化反应)阴极反应式:2H++2e-===H2↑(还原反应)总反应方程式:2NaCl+2H2O2NaOH+H2↑+Cl2↑
例1 氯碱工业的原理示意图如图。下列说法正确的是( )A. M为负极B. 通电使氯化钠发生电离C. 出口c收集的物质是氯气 D. 通电一段时间后,阴极区pH减小解析:A错,饱和食盐水从a口进入,在出口变为稀食盐水,则可以推出Cl-在左侧电极放电,则该电极为阳极,所以M为电源的正极。B错,氯化钠溶于水即发生电离,不需要通电。C对,Cl-在左侧放电,所以在出口c处收集的物质是Cl2。D错,右侧电极为阴极,该处产生OH-,则通电一段时间后,OH-浓度增大,所以pH增大。答案:C
例2 工业上常使用电解精炼法将粗铜提纯。在电解精炼时( )A.粗铜接电源负极B.纯铜作阳极C.杂质都将以单质形式沉积到池底D.纯铜片增重2.56 g,电路中通过电子数目为0.08 ml解析:A错,根据题意知电解精炼铜,粗铜作阳极,与电源正极相连。B错,根据题意知电解精炼铜,粗铜作阳极,纯铜作阴极。C错,根据题意知在阳极上,不参与放电的金属单质金、银等贵重金属会形成阳极泥沉积到池底,而锌等活泼金属以离子形式存在于溶液中。D对,根据题意知阴极反应为Cu2++2e- Cu,纯铜片增重2.56 g,即析出2.56 g铜,则电路中通过电子数目为 ×2=0.08 ml。答案:D
例3 利用如图所示装置模拟电解原理在工业生产中的应用。下列说法正确的是( )A.氯碱工业中,X电极上反应式是4OH--4e- 2H2O+O2↑B.电解精炼铜时,Z溶液中的Cu2+浓度不变C.在铁片上镀铜时,Y是纯铜D.制取金属镁时,Z是熔融的氯化镁解析:A错,氯碱工业中阳极是Cl-失电子生成Cl2。B错,电解精炼铜时阳极粗铜溶解,阴极Cu2+放电析出Cu,由于粗铜中含有锌、铁、镍等杂质,电解质溶液中Cu2+浓度减小。C错,铁片上镀铜时,阴极是铁片,阳极是纯铜。答案:D
人教版 (2019)选择性必修1第二节 电解池图文课件ppt: 这是一份人教版 (2019)选择性必修1第二节 电解池图文课件ppt,共41页。PPT课件主要包含了拓展延伸,方法技巧等内容,欢迎下载使用。
化学第二节 电解池图文ppt课件: 这是一份化学第二节 电解池图文ppt课件,共39页。PPT课件主要包含了拓展延伸,特别提醒等内容,欢迎下载使用。
高中人教版 (2019)第二节 电解池背景图课件ppt: 这是一份高中人教版 (2019)第二节 电解池背景图课件ppt,共43页。PPT课件主要包含了目录索引等内容,欢迎下载使用。













