

2022-2023学年福建省莆田第一中学高二上学期第一学段考试(月考)化学试题含答案
展开
莆田第一中学2022-2023学年高二上学期第一学段考试化学试卷
(时间:75分钟 满分97分+卷面分3分)
一、单项选择题(共15小题,每小题3分,满分45分)
1.下列分别是利用不同能源发电的实例,其中不属于新能源开发利用的是( )
2.以下过程在常温下都可以自发进行,可用焓判据来解释的是
- 硝酸铵自发地溶于水
- 湿的衣服经过晾晒变干
C.2N2O5(g)=4NO2(g)+O2(g) ΔH = + 56.7 kJ/mol
D.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol
3.为减缓钢铁设施在如图所示的情境中腐蚀速率,下列说法正确的是
A.此装置设计符合电解池的工作原理
B.金属的还原性应该比的还原性弱
C.当水体环境呈较强酸性时,钢铁设施表面会有气泡冒出
D.当水体环境呈中性时,发生的反应有
4. 室温下向的氨水中加水稀释后,下列说法正确的是
A.溶液中导电离子的数目减少
B.的电离程度增大,亦增大
C.溶液中增大
D.向氨水中加入固体,的电离平衡逆向移动,减小
5. 下列事实不能用勒夏特列原理解释的是( )
A. 新制的氯水在光照条件下颜色变浅
B. 合成氨工业中使用铁触媒作催化剂
C. 红棕色的NO2气体,加压后颜色先变深后变浅
D. 工业生产硫酸的过程中,通入过量的空气以提高二氧化硫的转化率
6. 可逆反应:2NO2(g)⇌2NO(g)+O2(g)在一固定容积的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时,生成2nmolNO
②单位时间内生成nmolO2的同时生成2nmolNO2
③用NO2、NO、O2物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
A.②④⑤ B.①④ C.②④ D.①②③④⑤
7. 化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度不断增加
B.乙:正极的电极反应式为Ag2O+2e-+H2O=== 2Ag+2OH-
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
8. 水的电离平衡曲线如图所示,下列说法不正确的是
A. 图中三点对应溶液中氢离子浓度关系:E<A<D
B. 若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性
C. 图中三点对应离子积关系:B>C>A
D. 若从A点到C点,可采用:温度不变在水中加少量NaOH固体
9. pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示。分别滴加NaOH溶液(c=0.1 mol/L)至恰好中和,消耗NaOH溶液的体积为Vx、Vy,则
A.x为弱酸,
B.x为强酸,
C.y为弱酸,
D.y为强酸,
10. 一种应用比较广泛的甲醇(CH3OH)燃料电池,电解液是酸性溶液,其工作原理如图所示,下列说法正确的是
A.M极为负极,发生还原反应
B.N极电极反应为O2+4H+-4e-=2H2O
C.甲池溶液pH增大,乙池溶液pH减小
D.若有1molCO2生成,则有6molH+从甲池通过交换膜进入乙池
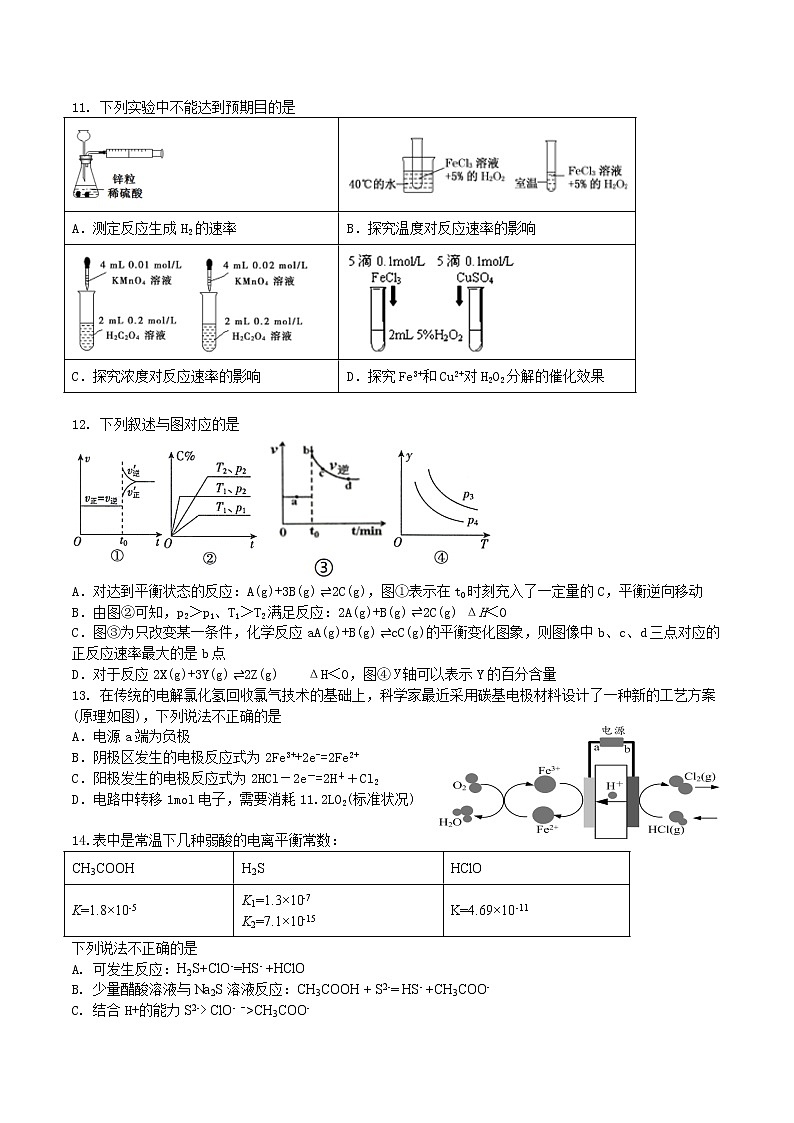
11. 下列实验中不能达到预期目的是
A.测定反应生成H2的速率 | B.探究温度对反应速率的影响 |
C.探究浓度对反应速率的影响 | D.探究Fe3+和Cu2+对H2O2分解的催化效果 |
12. 下列叙述与图对应的是
A.对达到平衡状态的反应:A(g)+3B(g) ⇌2C(g),图①表示在t0时刻充入了一定量的C,平衡逆向移动
B.由图②可知,p2>p1、T1>T2满足反应:2A(g)+B(g) ⇌2C(g) ΔH<0
C.图③为只改变某一条件,化学反应aA(g)+B(g) ⇌cC(g)的平衡变化图象,则图像中b、c、d三点对应的正反应速率最大的是b点
D.对于反应2X(g)+3Y(g) ⇌2Z(g) ΔH<0,图④轴可以表示Y的百分含量
13. 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案(原理如图),下列说法不正确的是
A.电源a端为负极
B.阴极区发生的电极反应式为2Fe3++2e-=2Fe2+
C.阳极发生的电极反应式为2HCl-2e-=2H++Cl2
D.电路中转移1mol电子,需要消耗11.2LO2(标准状况)
14.表中是常温下几种弱酸的电离平衡常数:
CH3COOH | H2S | HClO |
K=1.8×10-5 | K1=1.3×10-7 K2=7.1×10-15 | K=4.69×10-11 |
下列说法不正确的是
A. 可发生反应:H2S+ClO-=HS- +HClO
B. 少量醋酸溶液与Na2S溶液反应:CH3COOH + S2-= HS- +CH3COO-
C. 结合H+的能力S2-> ClO- ->CH3COO-
D. 同物质的量浓度的H2S、HClO、CH3COOH溶液,酸性最强的是CH3COOH
15. NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1NaHSO3(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如图所示。据图分析,下列判断不正确的是( )
A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中b、c两点对应的NaHSO3反应速率相等
C.图中a点对应的NaHSO3反应速率为5.0 ×10-5mol·L-1·s-1
D.温度高于40 ℃时,淀粉不宜用作该实验的指示剂
二、填空题(共4小题,满分52分)
16.((15分)参考下列图表和有关要求回答问题:
(1)图Ⅰ是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________,ΔH的变化是________(填“增大”、“减小”、“不变”)。请写出NO2和CO反应的热化学方程式:_________________________________。
(2)在一定体积的密闭容器中,进行如下化学反应:,其化学平衡常数K和温度t的关系如表所示:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数表达式为K=______。
②该反应为反应______(填“吸热”或“放热)。
③某温度下,平衡浓度符合下式:,试判断此时的温度为______℃。
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为,,,,则下一时刻,反应向______(填“正向”、“逆向”或“平衡”)进行。
(3)已知常温时红磷比白磷稳定,比较下列反应中的大小:______(填“>”或“<”)。
①
②
17.(13分)“绿水青山就是金山银山”,利用电池原理治理各种污染今后科研的重要课题。
(1) 硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化—化学耦合分解硫化氢的研究中获得新进展,相关装置如图(1)所示。请回答下列问题:
① a极为_________,其电极反应式为_____________。
② 请用离子方程式表示H2S气体去除的原理______________________________。
③ 请判断质子交换膜中H+的移动方向为___________。
(2) 碳排放是影响气候变化的重要因素之一。最近,科学家开发出一种新系统,“溶解”水中的二氧化碳,以触发电化学反应,生成电能和氢气,其工作原理如图(2)所示。
① 写出生成氢气的电极反应式__________________。
② 此电池的电池反应方程式____________________。
18. (12分)完成下列问题。
(1)某同学探究影响硫代硫酸钠与稀硫酸(Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O)反应速率的因素时,设计如下系列实验:
实验序号 | 反应温度/℃ | 溶液 | 稀 | |||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
② | 40 | 0.10 | 0.50 | |||
③ | 20 | 0.10 | 4.0 | 0.50 | ||
实验①、②可探究______对反应速率的影响,因此是______;实验①、③可探究______对反应速率的影响,因此是______。
(2)①I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将Ⅱ补充完整。
Ⅰ.SO2+4I-+4H+===S↓+2I2+2H2O
Ⅱ.I2+2H2O+__________===__________+__________+2I-
②探究Ⅰ、Ⅱ反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
ⅰ.B是A的对比实验,则a=________。
ⅱ.比较A、B、C,可得出的结论是_____________
A .I-可以作为SO2歧化反应的催化剂
B. 增强溶液酸性可以加快SO2的歧化反应
C. 氢离子单独存在对SO2歧化反应无明显影响
ⅲ.实验表明,SO2的歧化反应速率D>A。结合Ⅰ、Ⅱ反应速率解释原因:
___________________________________________________________________________________________。
19. (12分)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)CH4(g)+CO2(g) ⇌2CO(g)+2H2(g) ∆H1
b)CO2(g)+H2(g) ⇌CO(g)+H2O(g) ∆H2
c)CH4(g) ⇌C(s)+2H2(g) ∆H3
d)2CO(g) ⇌CO2(g)+C(s) ∆H4
e)CO(g)+H2(g) ⇌H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=___________(写出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
A.增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH4的平衡转化率
D.降低反应温度,反应a~e的正、逆反应速率都减小
(3)一定条件下,CH4分解形成碳的反应历程如图所示。该历程分___________步进行,其中,第___________步的正反应活化能最大。
(4)设为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100 kPa)。反应a、c、e的ln 随(温度的倒数)的变化如图2所示。
① 反应a、c、e中,属于吸热反应的有 (填字母)。
②反应c的相对压力平衡常数表达式为= 。
③在图2中A点对应温度下、原料组成为n(CO2)∶n(CH4)=1∶1、初始总压为100 kPa的恒容密闭容器中进行反应,体系达到平衡时H2的分压为40 kPa。计算CH4的平衡转化率 。
莆田一中2021-2022学年度上学期第一学段考试试卷答案
高二 化学
一、单项选择题(共15小题,每小题3分,满分45分)
题序 |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
答案 |
| C | D | C | C | B | C | A |
8 |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 |
D |
| B | D | A | B | D | C | B |
二、填空题(共4小题,满分52分)
16. ((15分)(1)减小((1分) 不变((1分)
NO2(g)+CO(g)=NO(g)+CO2(g) ΔH=-368 kJ·mol-1((3分)
(2) K=((2分) 吸热((2分) 8300C((2分 逆向 ((2分) <((2分)
17. (12分)
(1) ①负极(1分) Fe2+-e-Fe3+(2分)
② 2Fe3++H2S=2Fe2++S↓+2H+ (3分)
③从a极室移向b极室 (2分) (从右向左等其他合理答案均可得分)
(2)①2CO2+2H2O+2e-=2HCO3-+H2(2分)
②2Na+2CO2+2H20=2NaHCO3+H2(2分)
18. ((13分)
(1)温度 (1分) 0 (1分) 氢离子(或硫酸)浓度 (1分) 6.0(1分)
(2)①SO2 4H+ SO(3分,全对才得三分 配平错扣1分 微粒全对得两分)
②ⅰ.0.4(2分)
ⅱ. ABC(2分)(漏选一个扣一分)
ⅲ.反应Ⅱ比反应Ⅰ快,而且反应Ⅱ中生成了氢离子,也能加快反应Ⅰ的速率,从而使D的反应速率比A快(2分)(其他合理答案均可)
19. ((12分)【答案】 (1)ΔH3-ΔH4(或ΔH2+ΔH3-ΔH5) (2分)
(2)AD(2分)
(3)4(1分) 4(1分)
(4)①ac(2分) ②(2分)
③68%(2分)
2022-2023学年福建省莆田第一中学高一上学期第一学段考试化学试题含答案: 这是一份2022-2023学年福建省莆田第一中学高一上学期第一学段考试化学试题含答案,共18页。试卷主要包含了单选题,计算题,元素或物质推断题,实验题等内容,欢迎下载使用。
2022-2023学年福建省莆田第一中学高二下学期第二学段(期中)考试化学试题含答案: 这是一份2022-2023学年福建省莆田第一中学高二下学期第二学段(期中)考试化学试题含答案,共9页。
2022-2023学年甘肃省天水市第一中学高二上学期第一学段检测(月考)化学试题PDF版含答案: 这是一份2022-2023学年甘肃省天水市第一中学高二上学期第一学段检测(月考)化学试题PDF版含答案,共8页。













