
2023年高考第一次模拟考试卷:化学(重庆A卷)(考试版)
展开2023年高考化学第一次模拟考试卷(重庆A卷)
高三化学
本卷满分100分,考试时间75分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23 P 31 S 32 Fe 56
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列说法正确的是
A.明矾常用作净水剂,是因为明矾具有杀菌消毒的功能
B.从碘水中萃取碘,可以选择裂化汽油作萃取剂
C.“酸雨”“臭氧层空洞”“光化学烟雾”都可能与氮氧化物有关
D.在海轮外壳上嵌入钠块,可减缓船体的腐蚀速率
2.反应可应用于解决冬季开采石油井下结蜡难题。下列说法正确的是
A.的空间构型为三角锥型 B.中仅含离子键
C.仅为氧化产物 D.该反应的
3.能正确表示下列反应的离子方程式的是
A.溶液中通入少量:
B.溶液中通入少量:
C.向稀溶液中加入盐酸:
D.碳酸氢铵溶液与足量的溶液混合后加热:
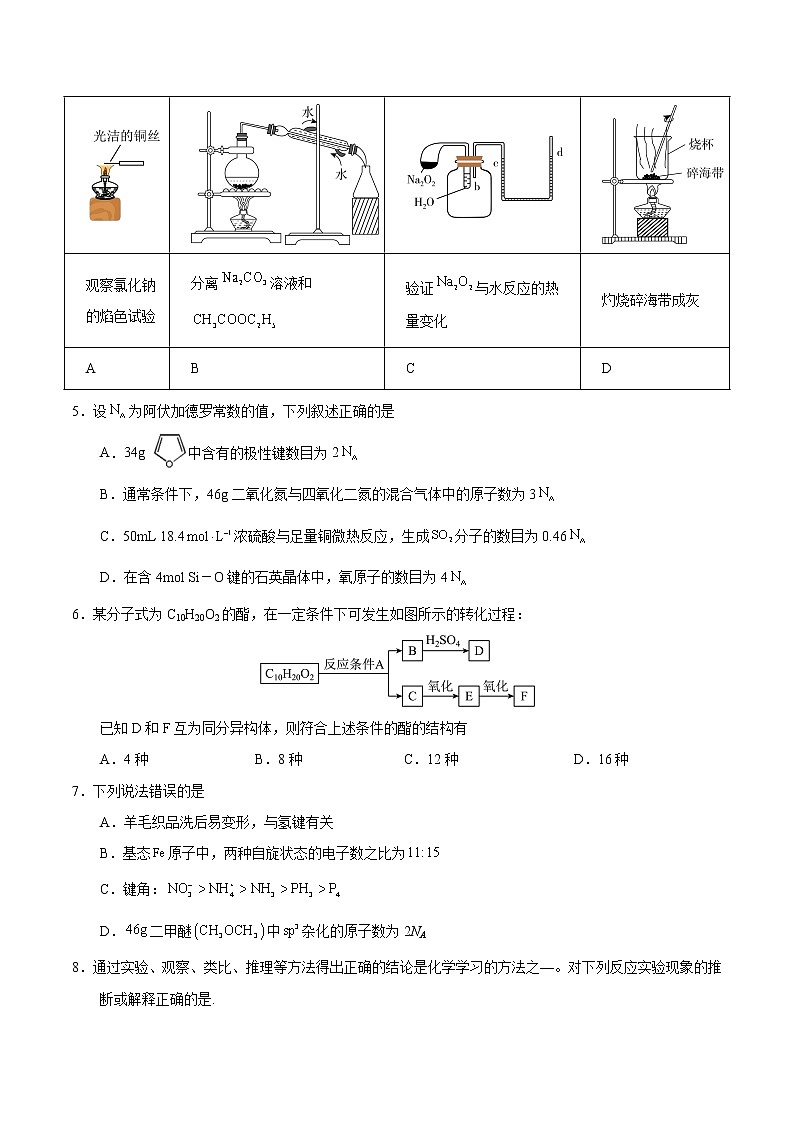
4.下列实验仪器或装置的选择正确的是
观察氯化钠的焰色试验 | 分离溶液和 | 验证与水反应的热量变化 | 灼烧碎海带成灰 |
A | B | C | D |
5.设为阿伏加德罗常数的值,下列叙述正确的是
A.34g 中含有的极性键数目为2
B.通常条件下,46g二氧化氮与四氧化二氮的混合气体中的原子数为3
C.50mL 18.4浓硫酸与足量铜微热反应,生成分子的数目为0.46
D.在含4mol Si-O键的石英晶体中,氧原子的数目为4
6.某分子式为C10H20O2的酯,在一定条件下可发生如图所示的转化过程:
已知D和F互为同分异构体,则符合上述条件的酯的结构有
A.4种 B.8种 C.12种 D.16种
7.下列说法错误的是
A.羊毛织品洗后易变形,与氢键有关
B.基态原子中,两种自旋状态的电子数之比为
C.键角:
D.二甲醚中杂化的原子数为2NA
8.通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之—。对下列反应实验现象的推 断或解释正确的是.
选项 | 操作 | 实验现象 | 解释 |
A | 向某钾盐中滴加浓盐酸,产生气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为K2SO3或KHSO3 |
B | 铝热剂溶于足量稀盐酸再滴加KSCN溶液 | 出现血红色 | 铝热剂中一定含有氧化铁 |
C | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 | 下层液体呈紫色 | 氧化性:Br2>I2 |
D | 将足量过氧化钠固体投入紫色石蕊试液中 | 溶液变成蓝色 | 过氧化钠与水反应生成氢氧化钠,溶液呈碱性 |
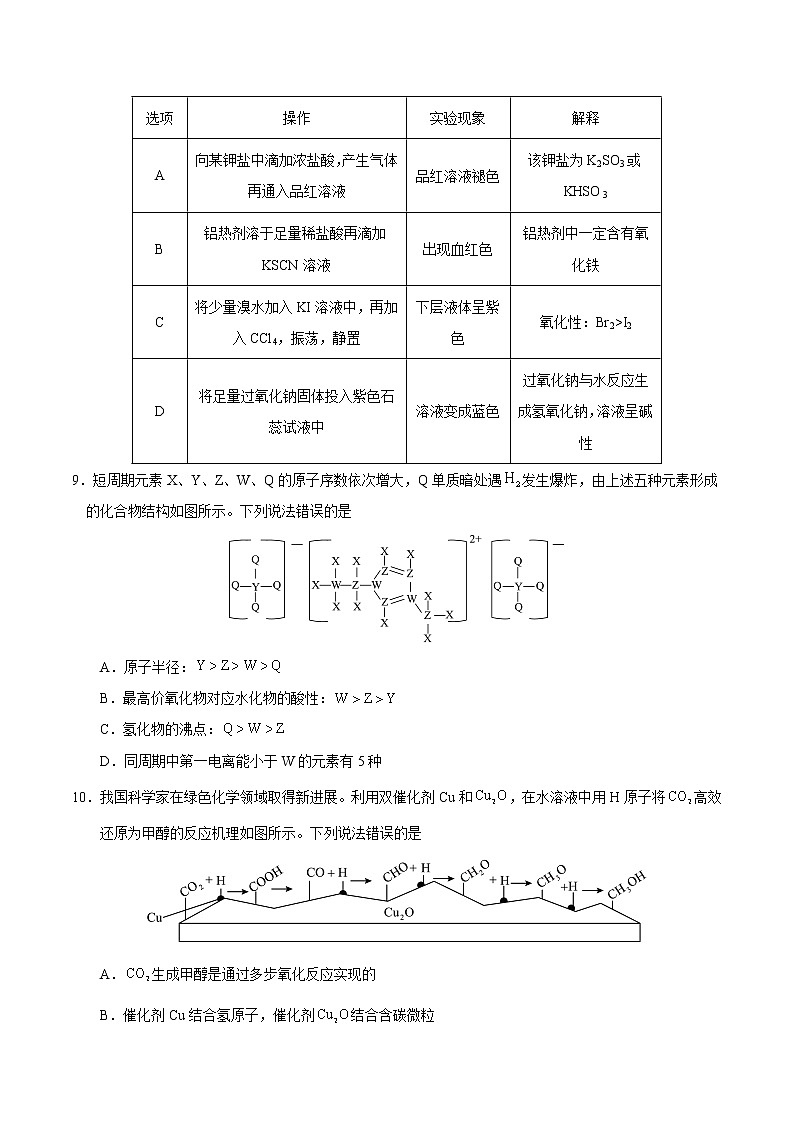
9.短周期元素X、Y、Z、W、Q的原子序数依次增大,Q单质暗处遇发生爆炸,由上述五种元素形成的化合物结构如图所示。下列说法错误的是
A.原子半径:
B.最高价氧化物对应水化物的酸性:
C.氢化物的沸点:
D.同周期中第一电离能小于W的元素有5种
10.我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和,在水溶液中用H原子将高效 还原为甲醇的反应机理如图所示。下列说法错误的是
A.生成甲醇是通过多步氧化反应实现的
B.催化剂Cu结合氢原子,催化剂结合含碳微粒
C.该催化过程中既涉及化学键的形成,又涉及化学键的断裂
D.有可能通过调控反应条件获得甲醛等有机物
11.废旧锌锰电池处理后的废料[含MnO2、MnOOH、Zn(OH)2、 Fe等]制备Zn和MnO2的一种工艺流程如 下:
已知:Mn的金属活动性强于Fe,Mn2+在pH大于5.5时易被氧化。
下列说法不正确的是
A.“还原焙烧”时Mn元素被还原
B.“酸浸” 过程中适当加热,主要目的是加快浸取速率
C.“净化”时MnCO3的作用是调节溶液的pH,使Fe3+形成Fe(OH)3沉淀而除去
D.“电解”时阳极反应式为Mn2+-2e-+4OH-=MnO2+2H2O
12.二氧化氯()是一种黄绿色、易溶于水的气体,常用于污染物的处理。工业上通过惰性电极电解氯化 铵和盐酸的方法制备的原理如图所示。下列说法正确的是
A.a极与电源的负极连接,Y溶液是稀盐酸
B.a极上发生的反应为
C.二氧化氯发生器内发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为1∶6
D.当0.6mol阴离子通过离子交换膜时,理论上二氧化氯发生器中产生标准状况下
13.温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1molNO2,发生反应: 2C(s)+2NO2(g)N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如 图所示。
下列说法不正确的是
A.T℃时,该反应的化学平衡常数为Kc=mol·L-1
B.由图可知,c点V正>V逆
C.向a点平衡体系中充入一定量的NO2,达到平衡时,NO2的转化率比原平衡小
D.容器内的压强:pa∶pb=6∶7
14.常温下:常见弱酸的电离平衡常数如下
HClO | ||
以下说法正确的是
A.少量通入到NaClO溶液中生成
B.等浓度等体积的NaOH与混合后,溶液中水的电离程度比纯水小
C.等浓度等体积的与NaHS混合,
D.NaOH溶液与溶液混合,当溶液的时,离子浓度大小关系为:
二、非选择题:本题共4小题,共58分。
15.(14分)钇(Y)是稀土元素中含量丰富的元素之一,钇及其化合物在航天、电子、超导等方面有着广泛的应用。湖北应山-大悟地区含有较为丰富硅铍钇矿[],工业上通过如下生产流程可获得氧化钇。
已知:元素与元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
(1)在自然界中,钇只有一种稳定同位素,Y位于元素周期表的第_______周期第ⅢB族。硅铍钇矿[]中Y的化合价为+3价,的化合价为_______。
(2)焙烧的目的是将矿石中的Y元素转化为,并将元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是 。硅铍钇矿与熔融氢氧化钠焙烧后含铁元素的产物是_______(写化学式)。
(3)“萃取分液”实验需要的玻璃仪器有 。
(4)滤液Ⅱ中的 (填物质名称)可参与循环使用。
(5)反应过程中,测得Y的沉淀率随的变化情况如图所示。当草酸用量过多时,钇的沉淀率 下降的原因是 。
(6)“焙烧”过程生成的化学方程式为 。
16. (15分)乳酸亚铁固体{[CH3CH(OH)COO]2Fe,相对分子质量234}常用于治疗缺铁性贫血,易溶于水, 难溶于乙醇。制备乳酸亚铁固体并测定其纯度的实验如下,回答下列问题:
I.制备碳酸亚铁
实验步骤:
第1步:组装仪器,检查装置气密性,加入试剂;
第2步:控制开关并制取氢气,排尽装置内的空气;
第3步:一段时间后,启动电磁搅拌器,并控制开关,制备FeCO3;
第4步:抽滤,洗涤干燥。
(1) 仪器a名称 ;实验中所用蒸馏水均需经煮沸后快速冷却,目的是 。
(2)第3步中“控制开关”的具体操作是 。
(3)装置B中Na2CO3溶液可用NaHCO3溶液代替,反应的离子方程式为 。
II.制备乳酸亚铁
向制得的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。
(4)该反应的化学方程式为 。反应结束后,从所得溶 液中获得乳酸亚铁晶体的方法是低温蒸发、冷却结晶、过滤、 、干燥。
III.乳酸亚铁晶体纯度的测量
(5)用铈量法测定产品中Fe2+的含量。称取3.9g样品配制成250mL溶液,取25.00mL,用 0.10mol·L-1(NH4)4Ce(SO4)4标准溶液滴定(Ce元素被还原为Ce3+),重复滴定2~3次,平均消耗标准 液 15.00mL。
①称取3.9g样品配制成250mL溶液时,除用到托盘天平、烧杯、玻璃棒、量筒外,还用到的玻璃仪器有 。
②产品中乳酸亚铁晶体的纯度为 。
17.(14分)含氨污染物的有效去除和含碳资源的充分利用是重要研究课题。回答下列问题:
(1)利用工业尾气与反应制备新型硝化剂,过程中涉及以下反应:
I.
II.
III.
平衡常数K与温度T的函数关系为,,,其中x、y、z 为常数,则反应I的活化能(正)______(逆)(填“>”或“<”),的数值范围是______。(填标号)
A. B.~0 C.0~2 D.>2
(2)与重整是利用的研究热点之一。该重整反应体系有以下反应:
I.
II.CO2(g)+H2(g)CO(g)+H2O(g)
III. (只在高温下自发进行)
①在一定压强和催化剂的条件下,将等物质的量的和通入重整反应器中,平衡时,、 的物质的量分数及转化率随温度变化的关系如图所示。平衡时的物质的量分数随温度变化的曲 线是______(填标号)。温度高于1300K后,曲线d超过曲线c的可能原因为__________________。
②在p MPa时,将和按物质的量之比为1∶1充入密闭容器中,分别在无催化剂和催化 下反应相同时间,所得的转化率与温度的关系如图所示。a点转化率相等的原因 是 。
③设为相对压力平衡常数,用相对分压代替浓度即可得相对压力平衡常数的表达式[气体的相对分压 等于其分压(单位为kPa)除以标准压强]。某温度下反应Ⅲ的,向恒容密闭容器 中按充入原料气,初始总压为150kPa,发生反应I、II、Ⅲ,体系达到平衡时 的分压为b kPa,则的平衡转化率为______。(用含b的代数式表示)
- (15分)阿司匹林是常用的解热镇痛药。一种制备阿司匹林的路线如下:
请回答下列问题:
(1)E的俗名叫水杨酸,其化学名称是_______;
(2)B→C的反应类型是: ;
(3)D中的官能团的名称是 。
(4)E→阿司匹林的化学方程式为 。
(5)在E的同分异构体中,同时具备下列条件的结构有_______种。
①遇FeCl3溶液显紫色; ②能发生银镜反应。
其中,在核磁共振氢谱上有4组峰,峰的面积比为1∶2∶2∶1且能发生水解反应的结构简式 为: 。
2023年高考第二次模拟考试卷-化学(重庆B卷)(考试版): 这是一份2023年高考第二次模拟考试卷-化学(重庆B卷)(考试版),共12页。
2023年高考第二次模拟考试卷-化学(重庆A卷)(考试版): 这是一份2023年高考第二次模拟考试卷-化学(重庆A卷)(考试版),共12页。
2023年高考第一次模拟考试卷:化学(重庆B卷)(全解全析): 这是一份2023年高考第一次模拟考试卷:化学(重庆B卷)(全解全析),共11页。试卷主要包含了B【详解】A,A【详解】A,C【详解】A,D【详解】A等内容,欢迎下载使用。












