

2022-2023学年北京市西城区高二上学期期末考试化学试卷(Word版含答案)
展开北京市西城区2022—2023学年度第一学期期末试卷
高二化学 2023.1
本试卷共9页,100分。考试时长90分钟。考生务必答案答在答题卡上,在试卷上作答无效。考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 S 32
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.下列装置或过程能实现电能转化为化学能的是( )
A.火力发电 | B.碱性锌锰电池 | C.电解饱和食盐水 | D.氢氧燃料电池 |
2.下列物质中,属于强电解质的是( )
A.NaOH B. C. D.
3.关于化学反应速率增大的原因,下列分析不正确的是( )
A.有气体参加的化学反应,增大压强使容器容积减小,可使单位体积内活化分子数增多
B.增大反应物的浓度,可使活化分子之间发生的碰撞都是有效碰撞
C.升高温度,可使反应物分子中活化分子的百分数增大
D.使用适宜的催化剂,可使反应物分子中活化分子的百分数增大
4.下列化学用语书写不正确的是( )
A.的结构示意图:
B.NaCl的电子式:
C.基态铜原子()的价层电子排布式:
D.基态氧原子的轨道表示式:
5.下列用于解释事实的化学用语书写不正确的是( )
A.电解精炼铜的阳极反应:
B.用溶液清洗油污的原因:
C.用饱和溶液处理锅炉水垢中的:
D.将纯水加热至较高温度,水的:
6.下列说法正确的是( )
A.2p、3p、4p能级的轨道数依次增多
B.所有非金属元素都分布在p区
C.最外层电子数为2的元素都分布在s区
D.元素周期表中从第ⅢB族到第ⅡB族的10个纵列的元素都是金属元素
7.下列事实不能用化学平衡移动原理解释的是( )
A.实验室收集氯气时,常用排饱和食盐水的方法
B.配制溶液时,常将晶体溶于较浓的盐酸中
C.工业合成氨,采用400℃~500℃的高温条件
D.工业制备:,加入大量水,同时加热
8.用0.100 0 HCl溶液滴定0.100 0 左右的NaOH溶液。下列说法不正确的是( )
A.在使用滴定管前,首先要检查活塞是否漏水,在确保不漏水后方可使用
B.锥形瓶盛装0.100 0 左右的NaOH溶液前必须保持干燥
C.酸式滴定管在盛装0.100 0 HCl溶液前要用该溶液润洗2~3次
D.用酚酞作指示剂,达到滴定终点时,溶液颜色从粉红色刚好变为无色,且半分钟内不变色
9.Ni单原子催化剂具有良好的电催化性能,催化转化的历程示意图如下:
下列说法不正确的是( )
A.该转化过程中被还原
B.②→③中断裂的与生成的化学键都是极性共价键
C.生成1 mol CO,需要转移2 mol
D.Ni原子在催化转化的过程中降低了该反应的焓变
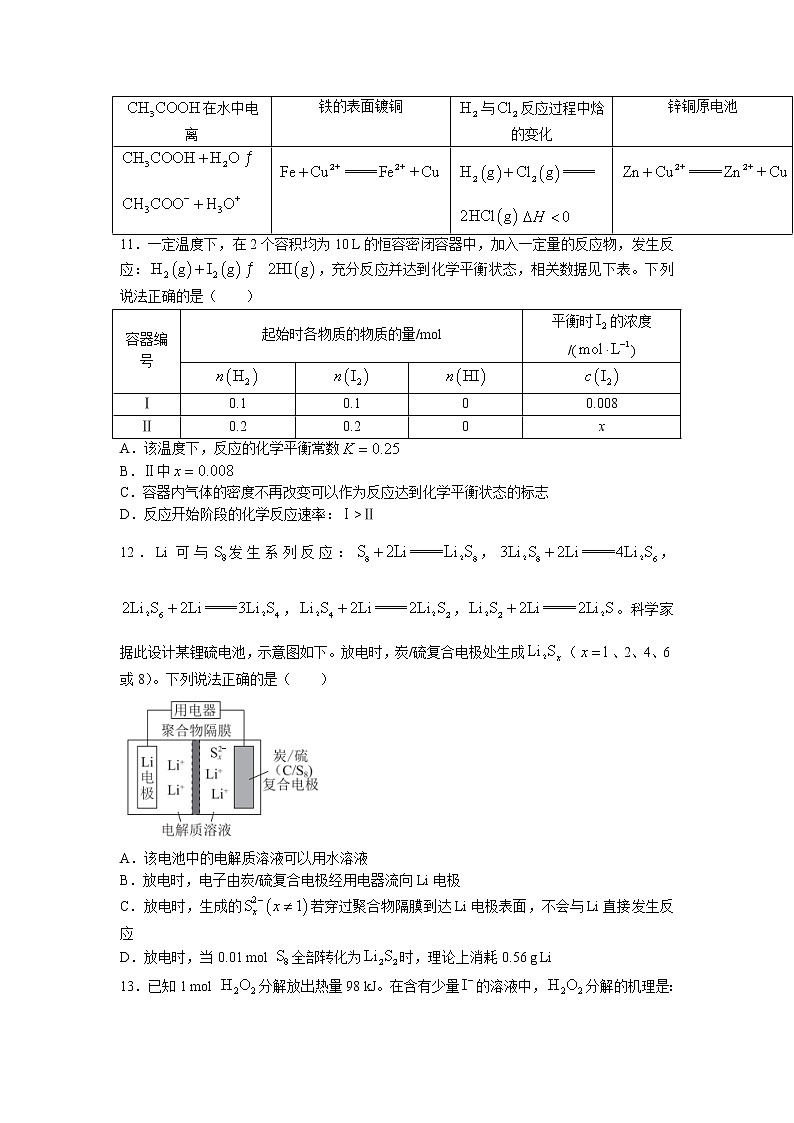
10.下列图示与化学用语表述内容不相符的是( )
A | B | C | D |
在水中电离 | 铁的表面镀铜 | 与反应过程中焓的变化 | 锌铜原电池 |
11.一定温度下,在2个容积均为10 L的恒容密闭容器中,加入一定量的反应物,发生反应:,充分反应并达到化学平衡状态,相关数据见下表。下列说法正确的是( )
容器编号 | 起始时各物质的物质的量/mol | 平衡时的浓度/() | ||
Ⅰ | 0.1 | 0.1 | 0 | 0.008 |
Ⅱ | 0.2 | 0.2 | 0 | x |
A.该温度下,反应的化学平衡常数
B.Ⅱ中
C.容器内气体的密度不再改变可以作为反应达到化学平衡状态的标志
D.反应开始阶段的化学反应速率:Ⅰ>Ⅱ
12.Li可与发生系列反应:,,,,。科学家据此设计某锂硫电池,示意图如下。放电时,炭/硫复合电极处生成(、2、4、6或8)。下列说法正确的是( )
A.该电池中的电解质溶液可以用水溶液
B.放电时,电子由炭/硫复合电极经用电器流向Li电极
C.放电时,生成的若穿过聚合物隔膜到达Li电极表面,不会与Li直接发生反应
D.放电时,当0.01 mol 全部转化为时,理论上消耗0.56 g Li
13.已知1 mol 分解放出热量98 kJ。在含有少量的溶液中,分解的机理是:ⅰ.,ⅱ.。分解过程中能量变化如图。下列说法正确的是( )
A.①表示加催化剂后反应过程中的能量变化
B.①的活化能等于98
C.ⅰ和ⅱ均为放热反应
D.ⅰ的化学反应速率比ⅱ的小
14.某实验小组研究经打磨的镁条与1 溶液()的反应。室温时,用传感器检测生成的气体,并测定反应后溶液的pH。实验如下表:
实验装置 | 编号 | 锥形瓶中的试剂 | 实验现象 | 锥形瓶内的浓度变化 |
① | 6.0 g 1 溶液 | 有极微量气泡生成,15 min后测得溶液的pH无明显变化 | ||
② | 6.0 g 1 溶液和 0.1 g镁条 | 持续产生大量气泡(净化后可点燃),溶液中有白色浑浊生成。15 min后测得溶液的pH上升至9.0 | ||
③ | 6.0 g (滴有酚酞溶液)和0.1 g镁条 | 镁条表面有微量气泡,一段时间后,镁条表面微红 |
下列说法不正确的是( )
A.由①可知,室温时,在溶液中可分解产生
B.由①②可知,②中产生的大量气体中可能含有
C.②中的反应比③中的剧烈,是因为溶液中更大
D.由②③可知,的作用可能是破坏了覆盖在镁条表面的镁与反应生成的
第二部分
本部分共6题,共58分。
15.(8分)我国科学家成功合成了世界上首个全氮阴离子盐,使氮原子簇化合物的研究有了新的突破。
(1)基态N原子中有______个未成对电子,电子占据的最高能级的符号是______。
(2)第二周期元素原子的第一电离能介于B、N之间的是______。
(3)以氮化镓(GaN)等为代表的第三代半导体材料具有优异性能,基态原子的简化电子排布式为______。
16.(9分)已知:25℃时,和的电离平衡常数近似相等。
(1)关于0.1 溶液,回答下列问题。
①25℃时,测得0.1 溶液的,则由水电离出的的浓度为______。
②溶液显______(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因:______。
(2)关于0.1 氨水,回答下列问题。
①的电离方程式为______,的电离平衡常数表达式:______。
②25℃时,0.1 氨水的______。
③25℃时,向10 mL 0.1 氨水中加入同体积同浓度的盐酸。下列说法正确的是______。
a.
b.
17.(10分)的捕获和转化可减少排放并实现资源的利用。在催化剂作用下,消耗和,生成合成气(、CO),主要发生反应ⅰ,可能发生副反应ⅱ、ⅲ:
ⅰ.
ⅱ.
ⅲ.
(1)______。
(2)反应ⅰ为可逆反应。从化学平衡的角度分析,利于生成合成气的条件是______。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(3)经研究发现,添加碱性助剂(如CaO)可以促进的吸附与活化。反应过程如图1。反应Ⅰ完成后,以为载气,将恒定组成、恒定流速的、混合气通入盛有足量的反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2。反应过程中始终未检测到,催化剂表面有积炭。
①反应Ⅱ的化学方程式为______。
②,,且生成的速率不变,可能发生的副反应是______(填序号“ⅱ”或“ⅲ”)。
③t3时,生成CO的速率为0,是因为反应Ⅱ不再发生,可能的原因是______。
18.(10分)某小组同学设想利用燃料电池和电解池组合,设计一种制备硫酸和氨的装置,相关的物质及工作原理示意图如下。a、b、c、d均为惰性电极,电解池中d上有可催化放电的纳米颗粒,固体氧化物电解质只允许在其中迁移。
(1)燃料电池制备硫酸。
①a为______(填“正极”或“负极”),电极反应式为______。
②H+的迁移方向为______(填“”或“”)。
③电池总反应的化学方程式为______。
(2)电解池制备氨。
下列关于电解过程的说法正确的是______。
A.d上,被还原
B.c的电极反应:
C.固体氧化物中的迁移方向为
(3)燃料电池中每消耗48 g ,在电解池中,理论上产生的在标准状况下的体积为______L。
19.(8分)三氧化二砷()是重要的化工原料,某以含砷废水制备三氧化二砷的流程如下。
资料:
ⅰ.含砷废水的主要成分:(亚砷酸)、、、(硫酸铋)。
ⅱ.相关难溶电解质的溶度积:
难溶电解质 | ||
(1)纯化
①当溶液中剩余离子的浓度小于时,认为该离子已被完全除去。常温下,若纯化过程中控制溶液的,______(填“能”或“不能”)将和完全除去。
②充分反应后,分离出精制含砷废水的方法是______。
(2)还原浸出
①补全还原浸出过程发生主要反应的化学方程式:
②其他条件相同时,还原浸出60 min,不同温度下砷的浸出率如下图。随着温度升高,砷的浸出率先增大后减小的原因是______。
③还原渣经过充分氧化处理,可返回______工序,循环利用。
a.纯化 b.沉砷 c.还原
(3)测定产品纯度
取a g 产品,加适量硫酸溶解,以甲基橙作指示剂,用b溶液滴定,终点时生成和,消耗c mL 溶液。产品中的质量分数是______。(的摩尔质量为198 )
20.(13分)某小组探究含Cr元素的化合物间的转化,进行如下实验。
资料:
ⅰ.含Cr元素的常见粒子:(橙色)、(黄色)、(溶于水,蓝紫色,不稳定)、(绿色)、(蓝灰色,难溶于水,可溶于强酸、强碱)、(亮绿色)。
ⅱ.在碱性环境中比在酸性环境中分解速率快。
ⅲ.在碱性环境中,不能氧化+3价铬元素。
实验操作及现象如下:
装置 | 步骤 | 操作 | 现象 |
2 mL 0.0125 溶液 | Ⅰ | 先滴入稀硫酸至,再滴入5滴5%溶液,振荡 | 溶液橙色加深。滴入溶液后迅速变为蓝紫色,有气泡生成。稍后,无明显气泡时,溶液由蓝紫色完全变为绿色 |
Ⅱ | 继续缓慢滴入10滴2 NaOH溶液,边滴,边振荡 | 又有气泡生成,溶液最终变为黄色 |
(1)已知。请用化学平衡移动原理解释Ⅰ中滴入稀硫酸后溶液橙色加深的原因:______。
(2)Ⅰ中,溶液由橙色变为绿色的总反应的离子方程式是______。
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是______。
(4)Ⅱ中,继续滴入NaOH溶液后,预测有沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被氧化。
①甲同学设计实验证明假设成立:
取少量Ⅰ中的绿色溶液,在滴入NaOH溶液前增加一步操作:______。然后滴入NaOH溶液,有蓝灰色沉淀生成,继续滴入NaOH溶液,沉淀溶解,溶液变为______色。
②乙同学进一步研究碱性环境对+3价铬元素的还原性或的氧化性的影响,设计如图实验。
右侧烧杯的溶液中,氧化剂是______。
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
ⅰ.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为______。
ⅱ.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为______。
(5)由上述实验,与、与的氧化性强弱(填“>”或“<”):
酸性条件下,______;碱性条件下,______。 北京市西城区2022—2023学年度第一学期期末试卷
高二化学答案及评分参考2023.1
第一部分(共14题,每题3分,共42分)
题号 | l | 2 | 3 | 4 | 5 | 6 | 7 |
答案 | C | A | B | C | A | D | C |
题号 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
答案 | B | D | B | A | D | D | C |
第二部分(共6题,共58分)其他合理答案均可给分
15.(8分,每空2分)
(1)3 2p
(2)Be、C、O
(3)[Ar]3d104s24p1
16.(9分)
(1)①110−11(1分)
②碱性(1分)CH3COO− + H2OCH3COOH + OH−(2分)
(2)①NH3 •H2ONH+ 4+ OH−(2分)
(1分)
②11(1分)
③b(1分)
17.(10分,每空2分)
(1)+247.0 kJ·mol−1 (2)B
(3)①CaCO3 + CH4=======CaO + 2CO + 2H2
②ⅱ
③积炭包裹催化剂,使反应Ⅱ不再发生,生成CO的化学反应速率为0
18.(10分)
(1)①负极(2分) SO2 + 2H2O-2e− == SO2− 4+ 4H+(2分)
②a→b(1分)
③2SO2 + O2 + 2H2O == 2H2SO4(2分)
(2)ABC(2分)
(3)11.2(1分)
19.(8分)
(1)①能(1分)②过滤(1分)
(2)①3Cu(AsO2)2 + 3SO2 + 6H2O== Cu3(SO3)2·2H2O + 6HAsO2 + H2SO4(2分)
②温度升高,化学反应速率增大;温度升高,SO2的溶解度降低,SO2的浓度降低,化学反应速率减小。T<60℃时,温度升高使化学反应速率增大的程度大于SO2的浓度降低使化学反应速率减小的程度。T>60℃时,温度升高使化学反应速率增大的程度小于SO2的浓度降低使化学反应速率减小的程度(2分)
③b(1分)
(3)(1分)
20.(13分)
(1)Cr2O2− 7(橙色)+ H2O2CrO2− 4(黄色)+ 2H+,滴入稀硫酸,c(H+)增大,平衡向左移动,c(Cr2O2− 7)增大,溶液橙色加深(2分)
(2)Cr2O2− 7+ 8H+ + 3H2O2== 2Cr3+ + 3O2↑+ 7H2O(2分)
(3)H2O2在碱性环境中比在酸性环境中分解速率快(1分)
(4)①将试管放入沸水浴中加热,至无气泡,冷却(1分) 亮绿色(1分)
②H2O2(1分)
ⅰ.Cr(OH)3 + 5OH−-3e−== CrO2− 4+ 4H2O(2分)
ⅱ.2H2O2== 2H2O + O2↑(1分)
(5)>(1分)<(1分)
北京市延庆区2023-2024学年高二上学期期末考试化学试卷(Word版含答案): 这是一份北京市延庆区2023-2024学年高二上学期期末考试化学试卷(Word版含答案),共9页。
北京市西城区2022-2023学年高三下学期一模考试化学试卷(word版,含答案): 这是一份北京市西城区2022-2023学年高三下学期一模考试化学试卷(word版,含答案),共10页。试卷主要包含了6×10−12 Ksp=1,3,不同温度下反应的结果如图等内容,欢迎下载使用。
北京市西城区2022-2023学年高三化学上学期1月期末考试试卷(Word版附答案): 这是一份北京市西城区2022-2023学年高三化学上学期1月期末考试试卷(Word版附答案),共11页。试卷主要包含了2~10等内容,欢迎下载使用。












