

所属成套资源:2023年中考化学高频考点突破(含答案解析)
2023年中考化学高频考点突破--化学元素
展开
这是一份2023年中考化学高频考点突破--化学元素,共14页。试卷主要包含了单选题,填空题,综合题等内容,欢迎下载使用。
2023年中考化学高频考点突破--化学元素
一、单选题
1.下列符号中,既能表示某种元素及该元素的一个原子,还能表示某种物质的是( )
A.Al3+ B.H C.Fe D.N2
2.下列物质中,由阴、阳离子构成的是( )
A.二氧化碳 B.氯化钠晶体 C.氢气 D.银
3.原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小。如图为镁、锶两种元素在元素周期表中的信息及它们的原子结构示意图,下列说法错误的是( )
A.两种元素均属于金属元素
B.锶的金属活动性比镁的金属活动性强
C.两种元素的化学性质相似
D.锶的相对原子质量是87.62g
4.元素、原子、分子等概念之间有点联系和区别,下列的描述中正确的( )
A.化学变化中元素种类、分子个数都保持不变
B.分子可以再分,原子不能再分
C.分子、原子都在不停地运动
D.分子可直接构成物质,而原子却不能。
5.下列说法正确的是( )
A.在实验室可以用筒量作反应容器
B.用托盘天平可以称量5.65g食盐
C.铁、氮气、氯化钠分别是由分子、原子、离子构成的
D.水和过氧化氢的化学性质不同主要是因为分子的构成不同
6.推理是一种重要的化学思维方法,以下推理合理的是( )
A.有机物都含碳元素,所以含碳元素的化合物一定是有机物
B.均一稳定的混合物是溶液,碘酒均一稳定,则碘酒属于溶液
C.化学变化伴随有能量变化,则有能量变化的变化一定是化学变化
D.同种元素的粒子质子数相同,则质子数相同的粒子一定属于同种元素
7.2014年5月7日在南京丢失的放射源铱﹣192,于5月10日安全回收.铱﹣192常用于肿瘤治疗.下图是铱﹣192在元素周期表中的信息,有关铱的说法错误的是( )
A.铱的元素符号是Ir B.铱元素是非金属元素
C.铱原子的原子序数为77 D.铱元素的相对原子量为192.2
8.2014年5月7日在南京丢失的放射源铱﹣192,于5月10日安全回收.铱﹣192是高危放射源,会危害人体健康.据图判断,有关铱的说法错误的是( )
A.铱元素是非金属元素 B.铱的元素符号是Ir
C.铱原子的原子序数为77 D.铱元素的相对原子质量为192.2
9.下列物质中含有氧分子的是( )
A.SO2 B.KClO3 C.MnO2 D.空气
10.属于同素异形体的一组物质是 ( )
A.一氧化碳和二氧化碳 B.水和双氧水
C.金刚石和石墨 D.氧气和液氧
11.下列说法正确的是( )
A.吹灭燃着的蜡烛,其灭火原理是使蜡烛与空气隔绝
B.不同种元素的本质区别是它们的核电荷数不同
C.合金是混合物,一定含金属元素,一定不含非金属元素
D.碱有一些相似的化学性质,是因为它们的溶液中都含有金属离子
12.下列符号既能表示一种元素,又能表示一个原子,还能表示这种物质的是()
A.O B.Mg2+ C.Ar D.N
二、填空题
13.从微观角度看,汞是由 (填具体粒子)构成,二氧化碳是由 (填具体粒子)构成,氯化钠是由 (填具体粒子)构成.
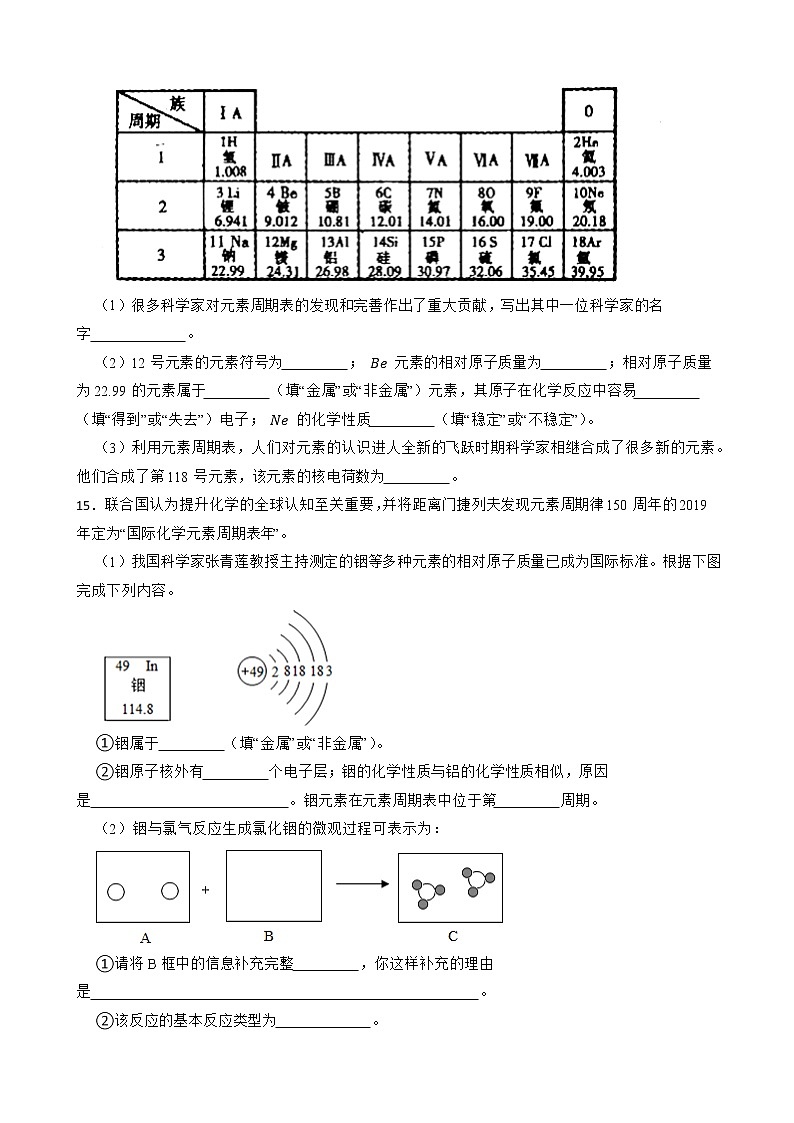
14.下表是元素周期表的一部分:
(1)很多科学家对元素周期表的发现和完善作出了重大贡献,写出其中一位科学家的名字 。
(2)12号元素的元素符号为 ; Be 元素的相对原子质量为 ;相对原子质量为22.99的元素属于 (填“金属”或“非金属”)元素,其原子在化学反应中容易 (填“得到”或“失去”)电子; Ne 的化学性质 (填“稳定”或“不稳定”)。
(3)利用元素周期表,人们对元素的认识进人全新的飞跃时期科学家相继合成了很多新的元素。他们合成了第118号元素,该元素的核电荷数为 。
15.联合国认为提升化学的全球认知至关重要,并将距离门捷列夫发现元素周期律150周年的2019年定为“国际化学元素周期表年”。
(1)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。根据下图完成下列内容。
①铟属于 (填“金属”或“非金属”)。
②铟原子核外有 个电子层;铟的化学性质与铝的化学性质相似,原因是 。铟元素在元素周期表中位于第 周期。
(2)铟与氯气反应生成氯化铟的微观过程可表示为:
①请将B框中的信息补充完整 ,你这样补充的理由是 。
②该反应的基本反应类型为 。
16.化学与生活、生产关系密切.请回答下列问题:
①如图为某抗酸药的实物图.该图标示的物质中,含有的金属元素是 (写出一种即可).
②沾染了油污的衣物用洗洁精就可以洗干净,这是利用了洗洁精的 作用.
③生产加碘盐通常是在食盐中加入碘酸钾(KIO3),碘酸钾中碘元素的化合价为 价.
④某种抗酸药的主要成分是三硅酸镁(Mg2Si3O8),能与盐酸发生复分解反应,则反应后产物中含镁的化合物是 (写化学式)
三、综合题
17.“嫦娥五号”上使用的记忆合金、SiC颗粒增强铝基复合材料、高性能芳纶纤维等材料引起了全世界的关注。
(1)下列属于有机合成材料的是 (填序号)。
A.记忆合金 B.羊毛 C.芳纶纤维
(2)硬度非常大的SiC,其结构类似金刚石,则构成SiC的基本粒子为 (填序号)。
A.分子 B.原子 C.离子
18.核电荷数为1~18的元素原子结构示意图等信息如图,
回答下列问题:
(1)氧元素与硫元素化学性质相似,主要是因为 。
(2)写出由8号,13号元素组成的化合物的化学式 。
(3)从表中可知金属锂的活动性比钠的金属活动性 ,锂与水反应生成碱和氢气,写出其反应方程式 。
19.在宏观、微观与符号之间建立联系、是化学学科的特点。
按如图所示。回答下列问题。
(1)图1中两种微粒属于不同种元素是因为 不同。
(2)图2中反应物 和 的微粒个数比为 ,其属于基本反应类型中的 。
(3)从微观角度分析,“ ”和“ ”两种物质化学性质不同的原因是 。
20.元素周期表是学习和研究化学的重要工具,它的内容十分丰富.如图是元素周期表的一部分:
试根据上表回答下列问题:
(1)地壳中含量最多的元素的原子序数是 .
(2)属于第4周期的元素有(填元素名称) (写出一种即可).
(3)妍妍同学考查后发现,第3周期开头的是 元素(填“金属”或“非金属”,下同),靠近尾部的是 元素.
(4)每一周期的元素从左向右排列所遵循的一条规律是 ;则表中x= ;若某种钙原子的相对原子质量为40,则它的中子数为 .
(5)利用元素周期表,人们对元素的认识进入全新时期.最近科学家宣布人工制得了第118号元素,此元素的核电荷数为 .
答案解析部分
1.【答案】C
【知识点】元素的符号及其意义
【解析】【解答】A.表示铝离子,A不符合题意
B.即表示氢元素,也表示一个氢原子,B不符合题意
C.表示铁元素、一个铁原子、铁单质,C符合题意
D.表示氮气和一个氮分子,D不符合题意
故答案为:C
【分析】一般情况下,元素符号一般表示两层含义,元素和一个原子,金属、固态非金属和稀有气体元素还可以表示单质,据此分析
2.【答案】B
【知识点】分子、原子、离子、元素与物质之间的关系
【解析】【解答】A、二氧化碳由二氧化碳分子构成,A不符合题意;
B、氯化钠晶体由带正电的钠离子和带负电的氯离子构成,B符合题意;
C、氢气由氢分子构成,C不符合题意;
D、银由银原子直接构成的单质,D不符合题意。
故答案为:B。
【分析】物质有微粒构成,构成物质的微粒有原子、分子、离子是那种,金属、稀有气体由原子构成;常见气体由分子构成;碱和盐由离子构成。
3.【答案】D
【知识点】原子结构示意图与离子结构示意图;元素周期表的特点及其应用
【解析】【解答】A. 镁、锶,都带“钅”字旁,都属于金属元素,故正确,不符合题意;
B. 锶元素核外电子层数比镁元素多,最外层电子数相等,因此锶的金属活动性比镁的金属活动性强,故正确,不符合题意;
C. 元素的化学性质与最外层电子数密切相关,由此可知,锶和镁的化学性质一定极为相似,是因为它们最外层电子数相等,故正确,不符合题意;
D. 由元素周期表的信息可知,锶元素的相对原子质量为87.62,单位是“1”,省略不写,不是g,故错误,符合题意。
故答案为:D。
【分析】A、根据元素名称的字旁,确定元素的种类。
B、根据锶元素核外电子层数比镁元素多,锶的金属活动性比镁的金属活动性强分析。
C、原子的最外层电子数相等,元素的化学性质相似。
D、根据元素周期表的信息,汉字下面的数字表示相对原子质量。
4.【答案】C
【知识点】分子、原子、离子、元素与物质之间的关系
【解析】【分析】A、化学反应前后元素的种类不变,但是分子的个数不一定不变,可以据此解答该题;
B、在化学变化中,分子可以再分,原子不能再分,忽略化学变化前提就是错误的,可以据此解答该题;
C、分子、原子都在不停地运动着,可以据此解答该题;
D、分子、原子或离子都可以直接构成物质,可以据此解答.
【解答】A、化学反应前后元素的种类不变,但是分子的个数不一定不变,故A错误;
B、在化学变化中,分子可以再分,原子不能再分,如果不指明化学变化中直接说原子不能再分是错误的,故B错误;
C、分子、原子都在不停地运动着,故C正确;
D、分子、离子、原子都是构成物质的微粒,表示物质的微观构成,故D错误.
故选C.
【点评】本题难度不是很大,主要考查了对分子、原子及元素的理解,培养学生对这些知识的理解能力.
5.【答案】D
【知识点】实验室常见的仪器及使用;分子的定义与分子的特性;分子、原子、离子、元素与物质之间的关系
【解析】【解答】A、量筒不能加热,也不能作反应容器,故说法错误,A不符合题意;
B、托盘天平的准确度是0.1g,不能称取5.65g食盐,故说法错误,B不符合题意;
C、铁是由铁原子构成的,氮气是由氮分子构成的,氯化钠是由离子构成的,故说法错误,C不符合题意;
D、水和过氧化氢化学性质不同是因为分子构成不同,故说法正确,D符合题意.
故答案为:D.
【分析】A、量筒不能作为反应容器,据此判断;
B、托盘天平可以精确到0.1g,据此判断;
C、根据构成物质微粒进行分析判断;
D、根据分子构成不同进行分析判断.
6.【答案】B
【知识点】溶液的组成及特点;元素的概念;物质发生化学变化时的能量变化;有机物的特征、分类及聚合物的特性
【解析】【解答】A. 有机物都含碳元素,但含碳元素的化合物不一定是有机物,例如,二氧化碳、碳酸钙等,虽然含有碳元素,但它们的性质与无机物相似,属于无机物,故不符合题意;
B. 均一稳定的混合物是溶液,碘酒均一稳定,则碘酒属于溶液,故符合题意;
C. 化学变化伴随有能量变化,有能量变化的变化不一定是化学变化,可以是电能转化为热能,例如,灯泡通电发光发热,故不符合题意;
D. 同种元素的粒子质子数相同,质子数相同的粒子不一定属于同种元素,例如,一个氨气分子和一个水分子中,所含的质子数相同,但它们不是属于同种元素,故不符合题意。
故答案为:B。
【分析】A、根据有机物的概念,进行分析。
B、具有均一性、稳定性的混合物是溶液。
C、化学变化伴随有能量变化。
D、根据元素的概念,进行分析。
7.【答案】B
【知识点】元素周期表的特点及其应用
【解析】【解答】A、根据元素周期表中的一格可知,字母表示该元素的元素符号,铱的元素符号是Ir,说法不符合题意;
B、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是铱,属于金属元素,说法符合题意;
C、根据元素周期表中的一格可知,左上角的数字为77,表示原子序数为77,说法不符合题意;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为192.2,说法不符合题意。
故答案为:B。
【分析】从元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量。
8.【答案】A
【知识点】元素周期表的特点及其应用
【解析】【解答】A、根据铱元素的汉字名称“铱”的偏旁“金”可知,为金属元素,不符合题意;
B、根据右上角的字母可知,其元素符号为:Ir,符合题意;
C、在原子中,原子序数=核电荷数=质子数=核外电子数,由元素周期表中左上角的数字77可知,其原子序数为77,符合题意;
D、根据元素周期表中的信息可知,下方的数字192.2为该元素的相对原子质量,符合题意。
故答案为:A。
【分析】根据元素周期表左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量分析。
9.【答案】D
【知识点】物质的构成和含量分析
【解析】【解答】A、二氧化硫是由二氧化硫分子构成的,不含氧分子,A不符合题意。
B、氯酸钾固体是由钾离子和氯酸根离子构成的,B不符合题意。
C、二氧化锰中含有氧元素,而无氧分子,C不符合题意。
D、空气中含有氧气,氧气是由氧分子构成的,D符合题意。
故答案为:D。
【分析】根据含有某分子的的只能是某物质或含有某物质的混合物分析
10.【答案】C
【知识点】同素异形体和同素异形现象
【解析】【分析】同素异形体的概念:同种元素形成的不同单质.判断同素异形体的关键把握两点:①同种元素形成,②不同单质.
【解答】判断同素异形体的关键把握两点:①同种元素形成,②不同单质.
A、CO和CO2是化合物,不是单质,故A错;
B、水和双氧水分别是H2O和H2O2,都是化合物,而不是单质,故B错;
C、金刚石和石墨都是由C元素形成的,又都是单质,符合概念,故C正确;
D、液氧和氧气是O2的两种不同的存在形式,属于同一种物质,而不属于不同的单质,故D错;
故选C.
【点评】判断同素异形体的关键把握两点:①同种元素形成,②不同单质.
11.【答案】B
【知识点】合金与合金的性质;元素的概念;灭火的原理和方法;酸、碱、盐的概念
【解析】【解答】A. 吹灭燃着的蜡烛,是吹走了因燃烧产生的较高温度得到气体,使蜡烛降温至着火点以下,达到灭火的目的,并没有隔绝空气,故不符合题意;
B. 元素是质子数(即核电荷数)相同的一类原子的总称,所以不同种元素的本质区别是它们的质子数(核电荷数)不同,故符合题意;
C. 合金是指金属与金属或非金属熔合而成具有金属特征的混合物,所以可能含非金属元素,故不符合题意;
D. 碱在水中都会解离出氢氧根离子和金属阳离子或铵根离子,碱溶液中都有氢氧根离子是碱具有通性的主要原因,故不符合题意。
故答案为:B。
【分析】A、根据灭火的原理、方法分析。
B、根据元素的概念分析。
C、根据合金的概念分析。
D、根据碱的概念分析。
12.【答案】C
【知识点】元素的符号及其意义
【解析】【解答】A.O可表示氧元素,表示一个氧原子,但不能表示一种物质,A不符合题意;
B.该符号是镁离子符号,不是元素符号,B不符合题意;
C.Ar于可表示氩元素,表示一个氩原子,还能表示氩气这一单质,C符合题意;
D.N可表示氮元素,表示一个氮原子,但不能表示一种物质,D不符合题意,
故答案为:C。
【分析】根据金属、固态非金属、稀有气体元素可以表示元素、单质和一个原子分析
13.【答案】汞原子;二氧化碳分子;钠离子和氯离子
【知识点】物质的构成和含量分析
【解析】【解答】解:汞属于金属单质,是由汞原子直接构成的;二氧化碳是由二氧化碳分子构成的;氯化钠是由钠离子和氯离子构成的.
故答案为:汞原子;二氧化碳分子;钠离子和氯离子.
【分析】根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠,进行分析解答即可.
14.【答案】(1)门捷列夫
(2)Mg;9.012;金属;失去;稳定
(3)118
【知识点】元素周期表的特点及其应用
【解析】【解答】(1)根据1869年以门捷列夫为代表的科学家发现了元素周期表,因此元素周期表的发现,其中一位科学家的名字:门捷列夫,故答案为:门捷列夫;
(2)根据元素周期表提供的信息可知:12号元素符号为Mg,故答案为:Mg;
Be元素的相对原子质量为9.012,故答案为:9.012;
相对原子质量为22.99的元素是钠,钠是金字旁,所以属于金属元素,故答案为:金属;
钠原子的核外电子排布最外层电子数是1个,小于4个,其原子在化学反应中容易失去电子,故答案为:失去;
Ne原子的最外层电子数是8个,已经达到稳定结构,在化学反应中既不容易得电子也不容易失电子,化学性质稳定,故答案为:稳定;
(3)根据在原子中,原子序数=质子数=核电荷数=核外电子数,可知第118号元素的核电荷数为118,故答案为:118。
【分析】(1)根据元素周期表的发现史进行解答。
(2)根据元素周期表提供的信息可知:左上角的数字表示原子序数,原子序数=原子的质子数;右上角的符号表示元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示原子的相对原子质量。
根据元素的名称,判断元素的种类。
原子的核外电子排布最外层电子数小于4个,其原子在化学反应中容易失去电子。
原子的最外层电子数是8个,已经达到稳定结构,化学性质稳定。
(3)根据在原子中,原子序数=原子的质子数-核电荷数。
15.【答案】(1)金属;5;原子的最外层电子数相同;五
(2);化学反应前后原子的种类、个数不变(质量守恒定律);化合反应
【知识点】原子结构示意图与离子结构示意图;元素周期表的特点及其应用;微粒观点及模型图的应用
【解析】【解答】(1)① 根据铟的元素名称写法,带有“钅”字旁,所以铟属于金属元素。
② 根据铟的原子结构示意图可知,一条弧线表示一个电子层,所以其原子核外有5个电子层;一般情况下,原子的最外层电子数相同化学性质相似,铟和铝的原子最外层电子数相同都是3,所以铟的化学性质与铝的化学性质相似;电子层数与元素所在的周期数相等,铟元素的原子有5个电子层,所以铟元素在元素周期表中位于第五周期。
(2)① 图中反应前A框中白球代表的原子个数为2,反应后C框中黑球和白球代表的原子个数分别为6和2,根据反应前后原子种类和个数守恒,所以B框中有6个黑色小球;又因为A框中物质是由原子直接构成的物质,所以A框中物质为铟(金属都是由原子构成的物质),B框中的物质表示氯气,每个氯气分子由两个氯原子构成,所以B框中应补充的是: ;这样补充的理由是:化学反应前后原子种类、个数不变(或质量守恒定律)。
② 该反应是两种物质生成一种物质,符合化合反应的特征,故该反应的基本反应类型为化合反应。
【分析】(1)① 根据元素名称,确定元素种类。
② 根据原子结构示意图可知原子核外的电子层数。
原子的化学性质与原子的最外层电子数有关。
元素的周期数=原子的电子层数。
(2)① 根据铟与氯气反应生成氯化铟,结合质量守恒定律,补充完整的图像。
② 根据反应的特点,进行分析。
16.【答案】Al;乳化;+5;MgCl2
【知识点】乳化现象与乳化作用;酸的化学性质;元素的简单分类;物质的元素组成;有关元素化合价的计算
【解析】【解答】解:(1)铝箔中含有金属元素铝,其符号为:Al;塑料属于有机合成材料;(2)洗洁精具有乳化作用,所以能洗涤油污;(3)钾元素显+1价,氧元素显﹣2价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,则x=+5价.(4)由于三归酸镁是和稀盐酸发生的反应是复分解反应,因此生成的盐应该是氯化物,及生成的含镁的化合物应是氯化镁,故答案为:MgCl2;故答案为:(1)Al;(2)乳化;(3)+5;(4)MgCl2.
【分析】(1)根据铝箔中含有金属元素铝以及有机合成材料的定义进行解答;(2)根据洗洁精的乳化作用进行解答;(3)根据在化合物中正负化合价代数和为零,结合碘酸钾(KIO3)的化学式进行解答本题;(4)复分解反应是两种化合物相互交换成分的反应,即一种化合物中的正价部分和另一种化合物中的负价部分相结合的反应.
17.【答案】(1)C
(2)B
【知识点】合成材料的使用及其对人和环境的影响;分子、原子、离子、元素与物质之间的关系
【解析】【解答】(1)A、记忆合金是一种合金,属于金属材料,不符合题意;
B、羊毛是一种天然纤维,不属于有机合成材料,不符合题意;
C、芳纶纤维是一种合成纤维,属于有机合成材料,符合题意,
故答案选:C。
(2)SiC的结构与金刚石类似,金刚石是由碳原子直接构成的,所以 构成SiC的基本粒子为原子,故答案选:B。
【分析】(1)根据合成材料包括塑料、合成纤维、合成橡胶分析; (2)根据金刚石是由碳原子直接构成分析。
18.【答案】(1)原子的最外层电子数相同
(2)Al2O3
(3)弱;2Li + 2H2O = 2LiOH + H2↑
【知识点】元素周期表的特点及其应用
【解析】【解答】(1)氧元素与硫元素化学性质相似,主要是因为原子的最外层电子数相同,都是6;
(2)8号元素为氧元素,通常显-2价,13号元素为铝元素,通常显+3价,故形成化合物的化学式为:Al2O3;
(3)元素的性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小,越活泼,故金属锂的活动性比钠的金属活动性弱;锂与水反应生成氢氧化锂和氢气,该反应的化学方程式为: 2Li+2H2O=2LiOH+H2↑ 。
【分析】(1)原子的最外层电子数相同,元素化学性质相似。
(2)先分析元素的名称。化合价,再写出化合物的化学式。
(3)根据元素周期表,同一纵行,从上到下,金属性越来越强。
19.【答案】(1)质子数(或核电荷数)
(2)2:1;化合反应
(3)分子构成不同
【知识点】分子的定义与分子的特性;元素的概念;反应类型的判定
【解析】【解答】(1)元素是质子数相同的一类原子的总称,故图1中两种微粒属于不同种元素是因为质子数不同;
(2)由图可知,该反应是一氧化氮和氧气在一定条件下反应生成二氧化氮,该反应的化学方程式为: 2NO+O2一定条件__2NO2 ;反应物 和 的微粒个数比为2:1,该反应符合“多变一”的特点,属于化合反应;
(3)分子是保持物质化学性质的最小粒子,一氧化氮由一氧化氮分子构成,二氧化氮由二氧化氮分子构成,分子构成不同,故化学性质不同。
【分析】(1)根据决定元素种类的是质子数进行分析
(2)根据反应的特点进行分析
(3)根据物质的结构决定物质的性质进行分析
20.【答案】(1)8
(2)钾或钙
(3)金属;非金属
(4)原子序数依次增加;20;20
(5)118
【知识点】元素周期表的特点及其应用
【解析】【解答】解:(1)地壳中各元素及含量由多到少的顺序是氧、硅、铝、铁、钙、钠、钾、镁、氢;所以含量最多的非金属元素为氧元素;故填:8;(2)元素周期表中每一个横行叫做一个周期,第4横行即为第4周期,钾(K)和钙(Ca)都属于该周期的元素,故填:钾或钙;(3)从元素名称的偏旁可以判断元素的类别,第3周期开头的元素是钠,元素名称中有“钅”字旁,它是金属元素;靠近尾部的是元素磷、硫、氯,元素名称中有“石”字旁或“气”字头,它们是非金属元素;故填:金属;非金属;(4)同一周期中元素的原子序数从左向右递增;由前面钾元素的原子序数,不难确定钙元素的原子序数(x)为20.而原子序数与原子中的质子数在数值上相等,所以钙原子中的质子数也为20.因质子数+中子数≈相对原子质量,故相对原子质量为40的钙原子中含有40﹣20=20个中子.故填:原子序数依次增加;20;20;(5)元素的核电荷数等于原子序数.故填:118.
【分析】(1)根据地壳中各元素的含量解答.地壳中氧元素含量最多;(2)根据元素周期表的信息来分析;(3)根据元素的汉字名称来分析其元素种类;(4)根据元素周期律以及相对原子质量=质子数+中子数来分析;(5)根据元素序数等于核电荷数来分析.
相关试卷
这是一份2023年中考化学高频考点突破--溶液,共15页。试卷主要包含了单选题,填空题,综合题等内容,欢迎下载使用。
这是一份2023年中考化学高频考点突破--溶解,共15页。试卷主要包含了单选题,填空题,综合题等内容,欢迎下载使用。
这是一份2023年中考化学高频考点突破--空气,共14页。试卷主要包含了单选题,填空题,综合题等内容,欢迎下载使用。









