

山东省烟台市重点中学2022-2023学年高一上学期期末调研化学试题(Word版含答案)
展开烟台市重点中学2022-2023学年高一上学期期末调研
化学
需要的相对原子质量:Na 23 S 32 O 16 Al 27 Cu 64
一、单项选择题(每题2分,共20分)
1. 化学与人类生活、生产密切相关。下列说法正确的是
A. 二氧化硫有毒,严禁将其添加到任何食品和饮料中
B. 维生素C具有还原性,食用维生素C含量较高的食物不利于人体对铁元素的吸收
C. 农村推广风力发电、光伏发电有利于“碳达峰、碳中和”
D. 酒精和84消毒液混合用作环境消毒能提高对新型冠状病毒的预防效果
2. 设为阿伏加德罗常数的值,下列说法正确的是
A. 100g46%的乙醇溶液中含有氧原子数为4
B. 标准状况下,22.4L由O2与O3组成的混合气体含有的氧原子数目为
C. 常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3
D. 常温常压下,含2molH2SO4的浓硫酸与足量铜共热,转移的电子数为2
3. 危险品氰化钾(KCN)有剧毒。KCN具有还原性,可用次氯酸钠做无害化处理,反应方程式为2CN-+2OH-+5ClO- =N2(g)+5Cl-+H2O+2CO。下列说法错误的是
A. 反应中氧化产物是N2和CO
B. 1mol还原剂参加反应失去电子的物质的量为5mol
C. 转移0.6mol电子可生成2.24L N2
D. 处理相同量的KCN,消耗O3的物质的量少
4. 某固体混合物可能由、、、、、中若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
A. 气体A中一定含有
B. 固体中可能含有
C. 该固体混合物中和至少有其中一种
D. 该固体混合物一定含有、、
5. 对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
选项 | 陈述I | 陈述II | 判断 |
A | 电泳实验表明 Fe(OH)3胶体是带电荷的 | 胶体能够比较稳定存在 | I对,II对,有关系 |
B | 二氧化硫使含有酚酞的氢氧化钠溶液褪色 | SO2具有漂泊性 | I对,II对,有关系 |
C | 铝粉可以与氧化镁组成铝热剂 | 铝粉有强还原性 | I对,II对,有关系 |
D | 将体积相同的Na和K 分别投入冷水中,K与H2O反应更剧烈 | 金属还原性:K>Na | I对,II对,有关系 |
A. A B. B C. C D. D
6. Cu与浓硝酸反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶液中得到NaNO3和NaNO2的混合溶液,反应过程及有关数据如图(已知:标准状况下N2O4为液态)。下列有关判断正确的是
A. 常温下,Cu遇浓硝酸发生钝化,所以二者需要在加热条件下才能反应
B. 若消耗铜片质量为44.8g,则生成0.3molNaNO3
C. 标准状况下收集的氮氧化物为20.16L
D. 可以通过加水稀释的方法消除浓硝酸的黄色
7. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
| 粒子组 | 判断和分析 |
A | Na+、Fe3+、Cl-、NH3·H2O | 不能大量共存,因发生反应:Fe3++3OH-=Fe(OH)3 |
B | H+、K+、ClO-、SO | 不能大量共存,因发生反应:2H++SO=H2O+SO2 |
C | H+、Fe2+、SO、H2O2 | 不能大量共存,因发生反应:2Fe2++H2O2+2 H+=2Fe3++2H2O |
D | H+、Na+、Cl-、MnO | 能大量共存,粒子间不反应 |
A. A B. B C. C D. D
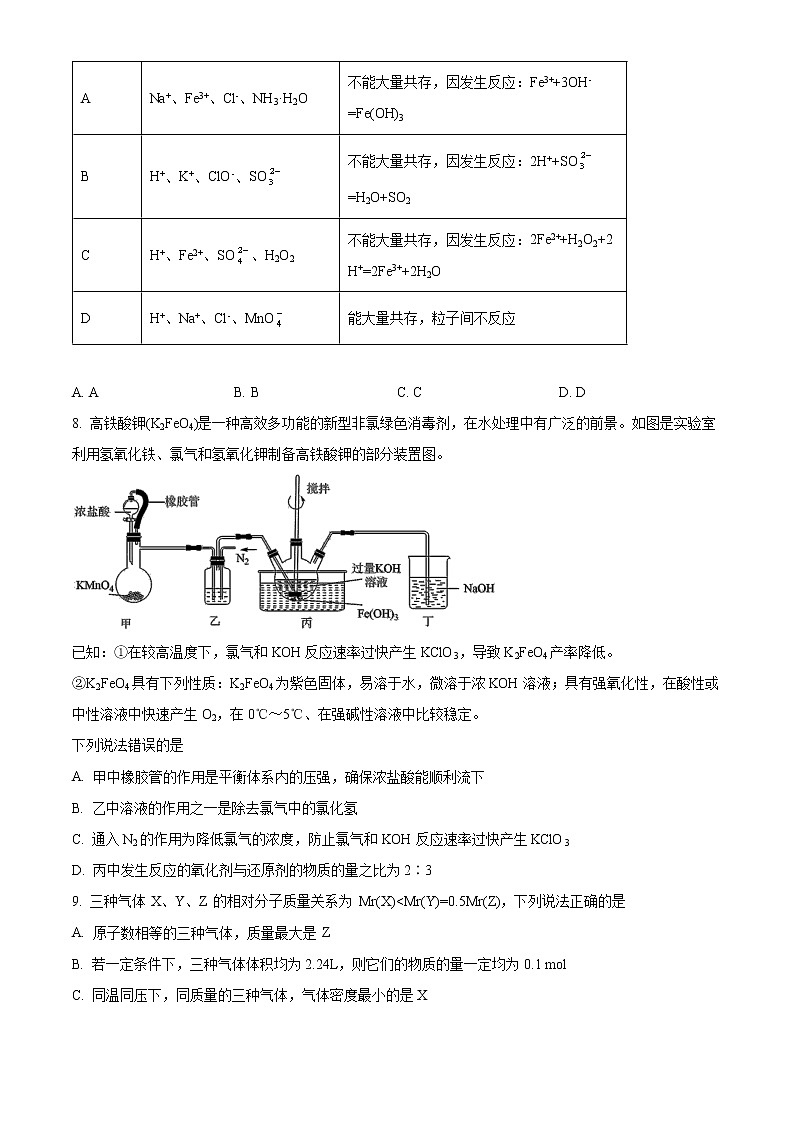
8. 高铁酸钾(K2FeO4)是一种高效多功能的新型非氯绿色消毒剂,在水处理中有广泛的前景。如图是实验室利用氢氧化铁、氯气和氢氧化钾制备高铁酸钾的部分装置图。
已知:①在较高温度下,氯气和KOH反应速率过快产生KClO3,导致K2FeO4产率降低。
②K2FeO4具有下列性质:K2FeO4为紫色固体,易溶于水,微溶于浓KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、在强碱性溶液中比较稳定。
下列说法错误的是
A. 甲中橡胶管的作用是平衡体系内的压强,确保浓盐酸能顺利流下
B. 乙中溶液的作用之一是除去氯气中的氯化氢
C. 通入N2的作用为降低氯气的浓度,防止氯气和KOH反应速率过快产生KClO3
D. 丙中发生反应的氧化剂与还原剂的物质的量之比为2∶3
9. 三种气体 X、Y、Z 的相对分子质量关系为 Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
A. 原子数相等的三种气体,质量最大是 Z
B. 若一定条件下,三种气体体积均为2.24L,则它们的物质的量一定均为0.1 mol
C. 同温同压下,同质量的三种气体,气体密度最小的是X
D. 同温下,体积相同的两容器分别充agY气体和2agZ气体,则压强之比为1:2
10. 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是
A. 该实验可以探究SO2的还原性
B. 为防止环境污染,装置C和E中的试剂均取用饱和氢氧化钙溶液
C. 关闭K2,打开 K1,则装置 B 中每消耗 1.5molNa2O2,转移电子数为1.5NA
D. 关闭 K1,打开 K2,试剂 X 是 K2Cr2O7溶液,颜色由橙红色变成绿色(生成 Cr3+ ),氧化剂与还原剂的物质的量之比是 3:1
二、不定项选择,每题1-2个正确选项(每题4分,漏选得2分,错选不得分)
11. 以菱镁矿(主要成分为MgCO3,含少量FeCO3、SiO2)为原料制备耐火材料MgO和副产品硫铵的流程如图所示。下列说法正确的是
A. 滤渣2加热分解可以制备磁性氧化铁 B. 在实验室中“灼烧”可在蒸发皿中进行
C. 氧化剂R可以是双氧水或氯水 D. 滤液1中的主要成分含有(NH4)2SO4
12. 已知 c、d、e、f、h 均是二元化合物,a为黑色固体单质,d能使品红溶液褪色,e是液体,上述物质的转化关系如图所示(个别产物略去)。下列说法错误的是
A. a与b的反应体现了b的强氧化性和酸性 B. f中阴阳离子个数比为1:2
C. h也可以由两种单质直接化合而成 D. d可用作食品添加剂
13. 过氧化钙(CaO2)是一种白色固体,能潮解,难溶于水,不溶于醇类。一种工业生产过氧化钙过程如下图所示。
下列说法错误的是
A. “冷水浴反应”中 H2O2的作用是氧化剂
B. 母液经处理后可返回“冷水浴反应”循环利用
C. 操作2需要用到坩埚、酒精灯、玻璃棒
D. 过氧化钙可用作杀菌消毒剂
14. 用如图所示装置(夹持装置已省略)进行下列实验,不能得出相应实验结论是
选项 | ① | ② | ③ | 实验结论 | |
A | 浓盐酸 | 高锰酸钾 | 碘化钾-淀粉溶液 | 氯气具有氧化性 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀硫酸 | Na2CO3 | CaCl2溶液 | CO2可与氯化钙反应 | |
D | 浓硫酸 | 铜片 | 酸性高锰酸钾溶液 | SO2具有还原性 |
A. A B. B C. C D. D
15. 向含有1 mol HNO3和1 mol H2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断不正确的是
A. a表示Fe3+的关系曲线
B. n1=0.75
C P点时,n(Fe2+)=0.562 5 mol
D. 向P点溶液中加入铜粉,最多可溶解12.2 g
三、非选择题
16. 回答下列问题:
(1)含1.0molFe3+的Fe2(SO4)3中所含SO的物质的量是______。
(2)等质量的N2、NH3、NO2、Cl2四种气体中,在相同温度和压强下,体积最大的是______。
(3)某混合溶液中含有Na+、Al3+、Cl-、SO,测得Na+、Al3+和Cl-的物质的量浓度比为3∶2∶1,则Al3+与SO的微粒个数比为______。
(4)实验室常用KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取少量氯气。若转移电子数目为NA,则产生Cl2的体积为______(标准状况),被氧化的HCl的物质的量为______。
(5)黑火药是我国古代四大发明之一,其化学反应方程式为:S+2KNO3+3C=K2S+3CO2↑+N2↑。
①上述反应所涉及到的物质中属于非电解质的是_____。
②上述反应中被氧化的元素是_____(填元素符号);氧化剂是______(填化学式)。
③收集上述反应生成的气体0.4mol,通入100mL4mol•L-1的氢氧化钠溶液中,最终所得溶液中的溶质是______(填化学式)。
(6)我国古代常用绿矾FeSO4•7H2O来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为______。
17. 铁基颜料铁黄(FeOOH)在高档涂料、油墨等领域有着广泛的应用。某同学设计了利用黄铁(主要成分:FeS2和SiO2,SiO2不参与反应)为主要原料制备绿矾(FeSO4·7H2O),并用得到的绿矾制备铁黄(FeOOH),流程如下:
已知:①FeSO4·7H2O溶于水,不溶于乙醇。
②“焙烧”方程式为4FeS2 +11O22Fe2O3+ 8SO2
③FeOOH为一种不溶于水的黄色固体。
回答下列问题:
(1)将黄铁矿进行粉碎,其目的是___________。
(2)“酸浸”后溶液呈黄色,试剂b若选用铁粉,“还原”步骤中是向溶液逐步加入铁粉,直至稍有气体生成,溶液变为浅绿色,写出主要反应的离子方程式___________。试剂b 若选用SO2,则该过程涉及的离子方程式有___________。
(3)检验“还原”是否完全的实验方案:取少量还原后的滤液于试管中,依次滴入KSCN溶液和氯水,若实验现象依次为___________,则证明含有Fe2+,不含Fe3+,“还原”完全。写出该检验过程中属于氧化还原反应的离子方程式___________。
(4)向“FeSO4溶液”中加入乙醇即可析出FeSO4·7H2O晶体,乙醇的作用是___________。已知绿矾溶解度曲线如图所示,则从“FeSO4溶液”中获得晶体的另一种方法是:蒸发浓缩(得到60℃饱和溶液)、___________、过滤、用冰水洗涤,低温干燥。
18. 二氧化硫在我们的生活中有利有弊。二氧化硫在食品添加剂中可作为“漂白剂、抗氧化剂、防腐剂”来使用。二氧化硫也是造成大气污染的有害气体之一、某小组同学在实验室中用浓硫酸与亚硫酸钠反应制取二氧化硫,并对二氧化硫的性质进行探究。已知: Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
回答下列问题:
(1)装置A应选择下列___________装置(填序号),装置③中a的仪器名称是___________。
(2)装置B中发生反应的离子方程式为___________。
(3)装置C中现象是___________; 该反应中氧化产物与还原产物的质量比为___________。
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:___________。
(5)该小组同学观察到装置D中溶液由棕黄色变成浅绿色,认为SO2与FeCl3溶液发生氧化还原反应,生成了SO。向D试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO。该做法是否合理,理由是___________
19. NaOH、、等含钠化合物在生产、生活中应用广泛。一种制备的流程如下:
已知:步骤Ⅱ中发生反应:
回答下列问题:
(1)“步骤I”发生反应的离子方程式为_______,该反应涉及物质中有_______种电解质。
(2)欲证明“步骤II”中溶液与尿素发生了反应,可选用的试剂为_______。
(3)“步骤Ⅳ”是先向溶液中通入制备溶液,然后滴加溶液与反应至约为10时,停止滴加,加热浓缩溶液至有大量晶体析出。测得溶液中、、等含硫微粒的物质的量分数[,x代表、或]随溶液的变化如图所示。
已知:与水反应生成亚硫酸(),其酸性强于碳酸。
①当溶液pH约为_______时停止通,溶液中的含量最高。
②当滴加NaOH溶液至pH等于7时,溶液中主要含硫微粒有_______,此时理论上通入的与消耗NaOH的物质的的量之比为_______。
20. 锰酸锂离子蓄电池是第二代锂离子动力电池,性能优良。工业上用某软锰矿(主要成分为MnO2,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂(LiMn2O4)。流程如图:
(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为______。
(2)滤渣II的主要成分是______;“精制”中加入H2O2的量比理论值大得多,其主要原因是_____。
(3)“沉锰”得到是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为MnO2,若控温氧化时溶液的pH随时间的变化如图,其中pH下降的原因是______(用化学方程式表示)。
(4)工业上也可以将“精制”后的滤液加入K2S2O8来合成MnO2。K2S2O8中S的化合价为价,加入K2S2O8溶液合成MnO2发生反应的离子方程式为______。
(5)“锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是_____。
(6)为测定成品锰酸锂的纯度,实验室可通过连续滴定法测定锰酸锂中锰元素的平均价态。
进行如下实验:
步骤1:取少量成品锰酸锂(假设为LiMnxOy)分成两等份,分别置于两只锥形瓶中;
步骤2:向一只锥形瓶中加入稀硝酸和双氧水,完全反应后,LiMnxOy中Mn元素转化为Mn2+,除去过量的双氧水。调节pH,滴加指示剂,用浓度为0.300mol•L-1的EDTA标准溶液滴定,终点时消耗EDTA标准溶液20.00mL(已知:Mn2+与EDTA反应的化学计量数之比为1∶1);
步骤3:向另一锥形瓶中加入1.340gNa2C2O4和足量硫酸,充分反应后,用0.100mol•L-1KMnO4标准溶液滴定,到达滴定终点时消耗KMnO4标准溶液20.80mL。
已知:LiMnxOyMn2+,则此成品锰酸锂LiMnxOy中Mn元素的平均化合价为______。
烟台市重点中学2022-2023学年高一上学期期末调研
化学答案
一、单项选择题(每题2分,共20分)
【1题答案】
【答案】C
【2题答案】
【答案】A
【3题答案】
【答案】C
【4题答案】
【答案】C
【5题答案】
【答案】D
【6题答案】
【答案】B
【7题答案】
【答案】C
【8题答案】
【答案】D
【9题答案】
【答案】C
【10题答案】
【答案】A
二、不定项选择,每题1-2个正确选项(每题4分,漏选得2分,错选不得分)
【11题答案】
【答案】D
【12题答案】
【答案】AC
【13题答案】
【答案】A
【14题答案】
【答案】C
【15题答案】
【答案】CD
三、非选择题
【16题答案】
【答案】(1)1.5mol
(2)NH3 (3)1:2
(4) ①. 13.44L ②. 1mol
(5) ①. CO2 ②. C ③. S、KNO3 ④. NaHCO3
(6)
【17题答案】
【答案】(1)增加其表面积加快焙烧速率
(2) ①. 2Fe3+ +Fe=3Fe2+ ②. 2Fe3+ +SO2 +2H2O=2Fe2+ + SO + 4H+
(3) ①. 滴加KSCN,溶液不变色,滴加氯水后溶液变成血红色 ②. 2Fe2+ + Cl2 =2Fe3+ + 2Cl-
(4) ①. 降低FeSO4·7H2O溶解度,有利于晶体析出 ②. 降温结晶
【18题答案】
【答案】(1) ①. ③ ②. 锥形瓶
(2)5SO2+2MnO+2H2O=2Mn2++5SO+4H+
(3) ①. 无色溶液中出现黄色浑浊 ②. 2:1
(4)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色
(5)不合理,HNO3可以将SO2氧化成H2SO4,干扰实验
【19题答案】
【答案】(1) ①. ②. 4
(2)溶液、稀硝酸
(3) ①. 4 ②. 、 ③. 2:1
【20题答案】
【答案】(1)
(2) ①. 、 ②. 因和能催化分解,原料利用率不高
(3)
(4)
(5)、
(6)+3.5
山东省烟台市2022-2023学年高二下学期7月期末考试化学试题(Word版含答案): 这是一份山东省烟台市2022-2023学年高二下学期7月期末考试化学试题(Word版含答案),文件包含山东省烟台市2022-2023学年高二下学期7月期末考试化学试题docx、2023年山东烟台高二下学期期末考试化学答案docx等2份试卷配套教学资源,其中试卷共14页, 欢迎下载使用。
精品解析:山东省烟台市2022-2023学年高一上学期期末考试化学试题(解析版): 这是一份精品解析:山东省烟台市2022-2023学年高一上学期期末考试化学试题(解析版),共18页。试卷主要包含了 关于下列仪器说法错误的是, 下列离子方程式书写正确的是等内容,欢迎下载使用。
山东省临沂重点中学2022-2023学年高一上学期期末化学试题(解析版): 这是一份山东省临沂重点中学2022-2023学年高一上学期期末化学试题(解析版),共25页。试卷主要包含了 下列化学用语不正确的是,5g等内容,欢迎下载使用。












