

黑龙江省鸡西市英桥高级中学2022-2023学年高二上学期期中考试化学试题(Word版无答案)
展开
这是一份黑龙江省鸡西市英桥高级中学2022-2023学年高二上学期期中考试化学试题(Word版无答案),共6页。试卷主要包含了5 Cu, 13mL 稀盐酸,67g NaOH,9 一 1, 写出下列物质的水解离子方程式,0 kJ ·ml- 1, 如下图所示的原电池, 8×10-5等内容,欢迎下载使用。
英桥高中高二期中考试化学试卷班级:___________ 姓名:____________ 考号:____________卷面分值:100 分可能用到的相对原子质量:H :1 N:14 O :16 Na:23 P :31 S :32 Cl:35.5 Cu:64 Fe:56 Zn:65 Ag:108 I:127 Pb :207一、选择题 (1-15 每小题只有一个选项符合题意,共 30 分)1 .下列物质的水溶液常温下 PH 小于 7 的是 ( )A .NaCl B .CH3COONa C .NH4Cl D .NaHCO32 .某学生的实验报告所列出的下列数据中合理的是 ( )A .用 10mL 量筒量取 7. 13mL 稀盐酸B .用托盘天平称量 2.67g NaOHC .用广泛 pH 试纸测得某溶液的 pH 为 3D .用 25mL 滴定管做中和滴定时,用去某浓度的碱溶液 21mL3 .通常人体胃液的 pH 大约是0.9 一 1.5 , 胃液的酸碱性为 ( )A .碱性 B .酸性 C .无法判定 D .中性4.在自然界中,原生铜的硫化物转变成CuSO4 后遇到地壳深层的 ZnS 和 PbS 便慢慢转变为 CuS。 由此可知,下列物质中溶解度最小的是( )A . CuSO4 B .ZnS C .PbS D .CuS5 .改变下列条件,能使水的电离平衡向正方向移动的是 ( )A .通入 HCl 气体 B .加入 NaOH 固体C .升高温度 D .加入 NaCl 固体6 .下列电离方程式不正确的是 ( )A .CH3COOHCH3COO-+H+ B .NH4ClNH+Cl-
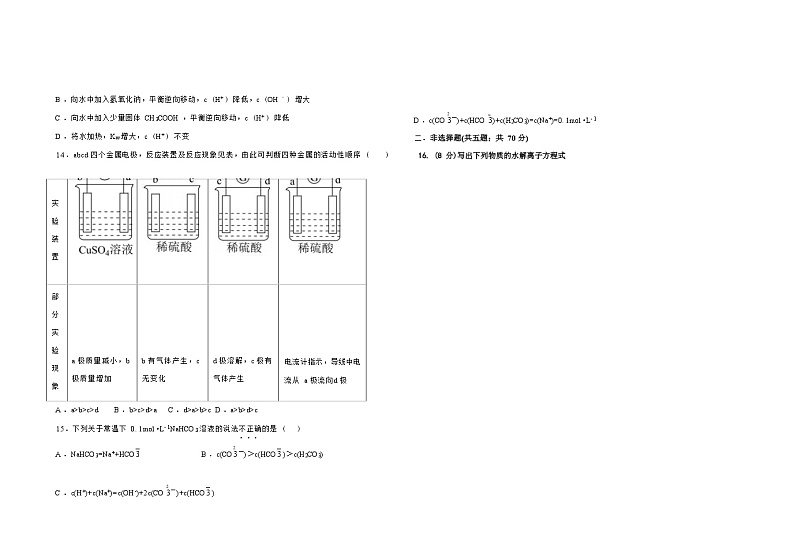
C .NaOH=Na++OH- D .K2SO4=2K++SO42一7 .CH4-CO2 催化重整反应为 CH4(g)+CO2(g)=2CO(g)+2H2(g) △H>0 有利于提高 CH4 平衡转化率的条件是 ( )A .高温低压 B .低温高压 C .高温高压 D .低温低压8 .下列物质用途或操作正确且与盐类水解无关的一组是 ( )A.用热饱和硫酸铵溶液清洗铁器表面的铁锈B.在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁C.刻蚀印刷电路板用氯化铁作腐蚀液D.用泡沫灭火器灭火9 .能说明醋酸是弱电解质的事实是 ( )A .醋酸水溶液能使湿润的蓝色石蕊试纸变红B .醋酸和碳酸钠溶液反应放出二氧化碳C .醋酸溶液的导电性比盐酸弱D .0. 1mol ·L-1 的醋酸溶液中,氢离子浓度约为 0.01mol ·L-110.能够使 CH3COONa 溶液 pH 增大且水解程度也增大的条件是 ( )A .加水 B .升温 C .加压 D .加 CH3COONa 固体11 、一定温度下,在密闭容器中进行反应:4A(s )+3B(g) 2C(g)+D(g) ,经 2min 后,B 的浓 度减少 0.6mol •L ﹣ 1 .对此反应的反应速率的表示,正确的是 ( )①在 2min 内,用 C 表示的反应速率是 0. 1mol •L﹣ 1•min ﹣ 1②反应的过程中,只增加 A 的量,反应速率不变③2 分钟内,D 的物质的量增加 0.2 mol ④分别用 B 、C 、D 表示的反应速率其比值为 3:2:1A .①② B .③ C .① D .②④12.同浓度的①(NH4)2CO3 ②(NH4)2SO4 ③(NH4)2Fe(SO4)2 ④NH4Cl ⑤NH4HSO4 溶液中 c(NH4 +)由大到小顺序为 ( )A .③②①④⑤ B .③②①⑤④C .①②③④⑤ D .②③①④⑤13.25℃时,水的电离达到平衡:H2OH++OH- △H>0 ,下列叙述正确的是 ( )A .向水中加入少量固体硫酸氢钠,c (H+ ) 增大,Kw 变大
B .向水中加入氢氧化钠,平衡逆向移动,c (H+ ) 降低,c (OH ﹣ ) 增大C .向水中加入少量固体 CH3COOH ,平衡逆向移动,c (H+ ) 降低D .将水加热,Kw 增大,c (H+ ) 不变14.abcd 四个金属电极,反应装置及反应现象见表,由此可判断四种金属的活动性顺序 ( ) 实 验 装 置部 分 实 验 现 象 a 极质量减小,b 极质量增加 b 有气体产生,c 无变化 d 极溶解,c 极有 气体产生 电流计指示,导线中电 流从 a 极流向d 极A .a>b>c>d B .b>c>d>a C .d>a>b>c D .a>b>d>c15.下列关于常温下 0. 1mol •L- 1NaHCO3 溶液的说法不正确的是 ( )A .NaHCO3=Na++HCO3一 B .c(CO32一 )>c(HCO3一 )>c(H2CO3) C .c(H+)+c(Na+)=c(OH-)+2c(CO 32一 )+c(HCO3一 ) D .c(CO 32一 )+c(HCO 3一 )+c(H2CO3)=c(Na+)=0. 1mol •L- 1二.非选择题(共五题;共 70 分)16. (8 分)写出下列物质的水解离子方程式
(1)CH3COONa:__________________(2)NaHCO3 : ___________________(3)FeCl3 : ___________________(4)NaCN: ____________________17.(6 分) (1) 已知两个氢气燃烧生成水的热化学方程式:H2(g)+O2(g)===H2O(l) ΔH=a kJ ·mol-12H2(g)+O2(g)===2H2O(l) ΔH=b kJ ·mol-1请回答下列问题:① 反应热的关系:a________(填“>”“<”或“=”)b。② 若已知 H2(g)+O2(g)===H2O(g) ΔH=-242 kJ ·mol-1,且氧气中 1 mol O==O 完全断裂时吸 收热量 496 kJ ,水蒸气中 1 mol H—O 形成时放出热量 463 kJ ,则氢气中 1 mol H—H 断裂时吸 收的热量为_______________。(2) 肼(N2H4)是一种用于火箭或燃料电池的原料,已知:①2H2O(g)+O2(g)=2H2O2(l) ΔH1= +108.0 kJ ·mol- 1②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2= -534.0 kJ ·mol- 1则③N2H4(l)+2H2O2(l)=N2(g)+4H2O(l) ΔH3=___________kJ ·mol- 1。18. (24 分) 下列化合物:①HCl ②NaOH ③CH3COOH ④NH3 ·H2O ⑤CH3COONa ⑥NH4Cl。( 1)溶液呈碱性的有______________(填序号)。(2)常温下 0.05 mol/L H2 SO4 溶液的 pH=__________ ;0.01 mol/L NaOH 溶液的 pH=________;pH= 10 的 CH3COONa 溶液中由水电离产生的 c(OH-)=_____________mol/L_ 。 (3)将等体积的 pH=3 的溶液③与④加水分别稀释 1 000 倍后,所得溶液 PH③: _______;④:________。(4)用盐类的水解知识解释热的纯碱去油污原理______________。(5)写出 1mol/LNH4Cl 的溶液中的电荷守恒表达式:_____________________________; 写出 1mol/LNaHCO3 溶液的物料守恒表达式:_________________________.
(6)NH4Cl 的水溶液呈________(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_________;(7)不断加热 FeCl3 溶液蒸干其水分并灼烧,得到的固体是___________。19. (14 分) 如下图所示的原电池:当电解质溶液为稀 H2 SO4 时,回答下列问题: ( 1)Zn 电极是_______极(填“正”或“负”)极(2)负极反应为_______(填“氧化”或 “还原”) ,电极反应式_______ 。正极反应为_______(填“氧化”或“还原”) ,电极反应式_______。,(3)电子移动方向_______ ,溶液中氢离子向_______(填“正”或“负”)极移动。20. (18 分) I.化学实验是中学化学学习中必不可少的一环。根据要求,回答下列问题: ( 1)在测定中和反应的反应热时,如图所示:①仪器 a 的名称为_______。②某同学每次分别取 0.50mol ·L- 150mLNaOH 溶液和 0.50mol ·L- 130mL 硫酸进行实验,通过多次 实验测定中和热的测量值为 53.5kJ ·mol- 1 ,与 57.3kJ ·mol- 1 有偏差,产生偏差的原因可能是 _______(填字母)。a.实验装置保温、隔热效果差b.用金属搅拌器代替玻璃搅拌器c.一次性快速把 NaOH 溶液倒入盛有硫酸的小烧杯中d.用温度计测定 NaOH 溶液起始温度后直接测定硫酸溶液的温度
(2)在进行酸碱中和滴定实验时:① 滴定管的使用。在使用滴定管前,要_______。② 用 0. 1000mol ·L- 1NaOH 溶液滴定未知浓度的 HCl 溶液,用酚酞溶液作指示剂,达到滴定终点 时的现象是_______。③ 排出碱式滴定管中气泡的方法应采用如图所示操作中的______,然后轻轻挤压玻璃球使尖嘴部分充满碱液。④ 读取盛装 0. 1000mol/LNaOH 溶液的_______(填仪器名称)的初始读数。 如果液面位置如图所 示,则此时的读数为_______mL。II.常温下,有关 4 种溶液的信息如下: 编号①②③④溶液氨水氢氧化钠溶液醋酸盐酸pH111133已知:NH3 ·H2O 与 CH3COOH 的电离常数都约为 1. 8×10-5。请回答下列问题:(3)取等体积的溶液①与④混合后,所得溶液呈_______性(填“酸”“中”或“碱”)。(4)将 aL 溶液②与 bL 溶液④混合后,若所得溶液的 pH=4(忽略溶液混合的体积变化) ,则 a: b=_______。
相关试卷
这是一份黑龙江省鸡西市密山市高级中学2023-2024学年高三上学期1月期末化学试题(Word版附答案),共6页。试卷主要包含了考试期间,注意考试时间,禁止在试卷上乱写乱画,3mlNO则生成的中键数目为0,4g能消除CO的数目为0等内容,欢迎下载使用。
这是一份2022-2023学年上海市新中高级中学高二上学期期中考试化学试题(无答案),共8页。试卷主要包含了有机物的制备等内容,欢迎下载使用。
这是一份2022-2023学年黑龙江省饶河县高级中学高二上学期期中考试化学试题 Word版,共9页。试卷主要包含了单选题,不定项选择题等内容,欢迎下载使用。









